1��ѡ���� ijNa2CO3��NaAlO2�Ļ����Һ����μ���1mol��L-1�����ᣬ�����Һ�е�CO32-��HCO3-��AlO2-��Al3+�����ʵ��������������Һ������仯��ϵ��ͼ��ʾ��������˵������ȷ����
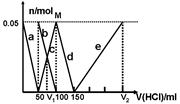
A��M��ʱ���ɵ�CO2Ϊ0mol
B��ԭ�����Һ�е�CO32-��AlO2-�����ʵ���֮��Ϊ1��2
C��V1��V2=1��4
D��a���߱�ʾ�����ӷ���ʽΪ��AlO2- +H+ + H2O��Al(OH)3��
�ο��𰸣�B
���������Na2CO3��NaAlO2�Ļ����Һ����μ���1mol?L-1�����ᣬ���ȣ�������ӦAlO2-+H++H2O�TAl��OH��3����a�߱�ʾAlO2-����ͼ��֪AlO2-��Ӧ��ϣ���������50mL�����ݷ���ʽ��֪n��AlO2-��=n��H+��=0.05mol��1mol/L=0.05mol���ڶ��Σ�AlO2-��Ӧ��ϣ�������ӦCO32-+H+�THCO3-��b�߱�ʾCO32-��c�߱�ʾHCO3-����ͼ��֪CO32-��Ӧ��ϣ��ýμ�������100mL-50mL=50mL�����ݷ���ʽ��֪n��CO32-��=n��H+��=0.05mol��1mol/L=0.05mol�������Σ�CO32-��Ӧ��ϣ�������ӦHCO3-+H+�TCO2��+H2O��d�߱�ʾHCO3-����ͼ��֪HCO3-��Ӧ��ϣ��ýμ�������150mL-100mL=50mL�����ݷ���ʽ��֪n��HCO3-��=n��H+�������ĽΣ�������ӦAl��OH��3+3H+�TAl3++3H2O��e�߱�ʾAl3+����ͼ��֪Al��OH��3��Ӧ�������������0.05mol�����ݷ���ʽ��֪n��H+��=3n[Al��OH��3]=3��0.05mol=0.15mol���ýμ����������Ϊ150mL��A��������������֪M��ʱ��Һ��CO32-��ȫת��ΪHCO3-��û��CO2���ɣ���ȷ�� B��������������֪��ԭ�����Һ�е�CO32-��AlO-2�����ʵ���֮��Ϊ1��1������C��ԭ��Һ��n��CO32-��=0.05mol��V1ʱ��Һ��̼��������ӵ���̼�������Ϊ0.025ml���ɷ�ӦCO32-+H+�THCO3-��֪����Ҫ����Ϊ0.025mol����������Ϊ25mL����V1=50mL+25mL=75mL��������������֪��V2=150mL+150mL=300mL����V1��V2=75mL��300mL=l��4����ȷ��D��������������֪��a���߱�ʾ�����ӷ���ʽΪ��AlO-2+H++H2O=Al��OH��3������ȷ��
�����Ѷȣ�һ��
2��ѡ���� ����NaOH��BaCl2��Al2(SO4)3���ֹ�����ɵĻ��������������ˮ�У�����ܽ⣬������Һ�еμ�1mol��L-1��ϡ���ᣬ����ϡ�������������ɳ�����������ϵ��ͼ��ʾ�������й��жϲ���ȷ����
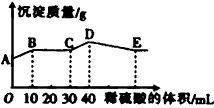
[? ]
A. AB�η�����Ӧ�ĵ����ӷ���ʽΪ��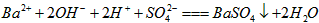
B. BC�η�����Ӧ�����ӷ���ʽΪ��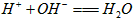
C. D���ʾ�ij����Ļ�ѧʽΪAl(OH)3��BaSO4
D. E���ʾ����Һ������
�ο��𰸣�D
���������
�����Ѷȣ�һ��
3��ѡ���� ��ij��Һ�м���������H2���������ڸ���Һ��һ���ܴ������ڵ���������
A.K+��Na+��Cl-��NO3-
B.OH-��CO32-��Cl-��K+
C.Fe2+��Na+��SO42-��NO3-
D.Cu2+��NO3-��NH4+��Cl-
�ο��𰸣�A
�������������������H2����������Һ���д�����H+��OH-��Bѡ���е�OH-��CO32-������H+�������森Cѡ���е�Fe2+����OH-�����ɳ����������Ի����лᱻNO3-������Dѡ���е�Cu2+��NH4+������OH-�������森
�����Ѷȣ���
4��ѡ���� ����������ˮ��Һ�еĵ��뷽��ʽ��ȷ����
A.NaHSO4=Na++H++SO42��
B.KClO3=K++Cl5++3O2��
C.Ba(OH)2=Ba2++(OH)22��
D.H2SO4=H2++SO42��
�ο��𰸣�A
������������������NaHSO4��ˮ��Һ����ȫ�����Na+��H+��SO42����B��KClO3=K++ ClO3��
ClO3����ԭ���Ų��ܲ�д��Ba(OH)2= =Ba2++2OH-��ԭ�������ŵ����½DZ꣬��ʾԭ���ŵĸ�����Ҳ���ǵ����ԭ���ŵĸ�������Mg(NO3)2=Mg2++ 2NO3-��H2SO4=2H++SO42����
���㣺��������ʵ��뷽��ʽ����д����
�����Ѷȣ�����
5������� ��1��M�����ֶ�����Ԫ����ɣ�ÿ��M���Ӻ���18�����ӣ���������ģ����ͼ��ʾ�����M��Ħ������Ϊ32g/mol���������Ϊ2��ԭ�ӽṹʾ��ͼ��??��
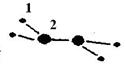
��2����֪1.0mol��L��1NaHSO3��Һ��pHΪ3.5��������ˮ������ҺpHѸ�ٽ��͡���ҺpH���͵�ԭ����?�������ӷ���ʽ��ʾ����
��3���ڳ��³�ѹ���������£�N2�ڴ�����TiO2��������H2O��Ӧ������1molNH3��O2ʱ�������仯ֵΪ382.5kJ���ﵽƽ���˷�ӦNH3���������¶ȵ�ʵ���������±�����÷�Ӧ���Ȼ�ѧ����ʽΪ?��
T/K
| 303
| 313
| 323
|
NH3������/��10��1mol��
| 4.3
| 5.9
| 6.0
|
?
��4������Һ�У�һ��Ũ�ȵ�NH4�����ܽⲿ��Mg(OH)2���壬��Ӧ���£�
2NH4+(aq) + Mg(OH)2(s) 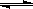 Mg2+(aq) +2NH3��H2O(aq)
Mg2+(aq) +2NH3��H2O(aq)
д��������Ӧ��ƽ�ⳣ������ʽ?
ij�о���ѧϰС��Ϊ̽��Mg2+��NH3��H2O��Ӧ�γɳ���������������������ʵ��
ʵ���
| �����1 mol/L��ˮ��0.1 mol/L MgCl2��Һ���
| ���ɰ�ɫ����
|
ʵ���
| �����0.1 mol/L��ˮ��1 mol/L MgCl2��Һ���
| ������
|
?
�����ʵ��١��ڲ�����ͬ�����ԭ��?��
��5���������£���ѧ��ӦI��(aq)+ ClO��(aq)=IO��(aq) + Cl��(aq)�ķ�Ӧ���ʼŨ�ȡ���Һ�е����������ӳ�ʼŨ�ȼ���ʼ���ʼ�Ĺ�ϵ���±���ʾ��
ʵ����
| I���ij�ʼŨ��
(mol��L��1)
| ClO���ij�ʼŨ��
(mol��L��1)
| OH���ij�ʼŨ��
(mol��L��1)
| ��ʼ����v
(mol��L��1�� s��1)
|
1
| 2 �� 10��3
| 1.5 �� 10��3
| 1.00
| 1.8 �� 10��4
|
2
| a
| 1.5 �� 10��3
| 1.00
| 3.6 �� 10��4
|
3
| 2 �� 10��3
| 3 �� 10��3
| 2.00
| 1.8 �� 10��4
|
4
| 4 �� 10��3
| 3 �� 10��3
| 1.00
| 7.2 �� 10��4
|
?
��֪���г�ʼ��Ӧ�������й�����Ũ�ȹ�ϵ���Ա�ʾΪv=" k" [I��?]1 [ClO��]b [OH��]c���¶�һ��ʱ��kΪ��������
�����ʵ��2��ʵ��4��Ŀ����?��
����ʵ����4������Ũ�Ȳ��䣬������Һ�����ֵ���ΪpH = 13����Ӧ�ij�ʼ����v=?��
�ο��𰸣���1��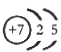 ? (2��)?��2��HSO3��+ Cl2 +H2O? = 3H+ + SO42��+ 2Cl��?��3�֣�
? (2��)?��2��HSO3��+ Cl2 +H2O? = 3H+ + SO42��+ 2Cl��?��3�֣�
��3��2N2(g) +6H2O(l) = 4NH3(g) + 3O2(g)?��H=+1530.0kJ/mol?��3�֣�
��4��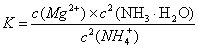 ?��2�֣�����ƽ�ⳣ������ʽ���Կ�������c(NH3��H2O)��c(Mg2+)�ı���ͬ�ij̶�ʱ��c2(NH3��H2O)�Գ������ɵ�Ӱ�����[�����c(Mg2+)?c2(OH��)��Ksp[Mg(OH)2]��������c(Mg2+)?c2(OH��)��Ksp[Mg(OH)2]���Ⱥ����𰸾���] ��2�֣�
?��2�֣�����ƽ�ⳣ������ʽ���Կ�������c(NH3��H2O)��c(Mg2+)�ı���ͬ�ij̶�ʱ��c2(NH3��H2O)�Գ������ɵ�Ӱ�����[�����c(Mg2+)?c2(OH��)��Ksp[Mg(OH)2]��������c(Mg2+)?c2(OH��)��Ksp[Mg(OH)2]���Ⱥ����𰸾���] ��2�֣�
��5����? ClO�� �Է�Ӧ���ʵ�Ӱ��?��2�֣�
��? 7.2 �� 10��4?��2�֣�
�����������1�����������ƶϣ�MΪN2H4����1��2�ֱ��ʾH��N����ԭ�ӵĺ˵����Ϊ+7��������Ӳ�ṹΪ25����2��������������ˮ����������ԭ��Ӧ������ǿ�ᣬ��ӦʽΪHSO3��+Cl2+H2O=3H++SO42��+2Cl������3��������֪�������¶ȣ�ƽ�����ƣ�˵������Ӧ�����ȷ�Ӧ������ԭ���غ��֪��1/2N2(g)+3/2H2O(l) NH3(g)+3/4O2(g)?��H=+382.5kJ/mol����2N2(g) +6H2O(l) = 4NH3(g) + 3O2(g)?��H=+1530.0kJ/mol����4���������ʲ���д��ƽ�ⳣ������ʽ����÷�Ӧ��ƽ�ⳣ��K=
NH3(g)+3/4O2(g)?��H=+382.5kJ/mol����2N2(g) +6H2O(l) = 4NH3(g) + 3O2(g)?��H=+1530.0kJ/mol����4���������ʲ���д��ƽ�ⳣ������ʽ����÷�Ӧ��ƽ�ⳣ��K=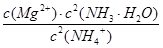 ����ƽ�ⳣ������ʽ���Կ�������c(NH3��H2O)��c(Mg2+)�ı���ͬ�ij̶�ʱ��c2(NH3��H2O)�Գ������ɵ�Ӱ�����[�����c(Mg2+)?c2(OH��)��Ksp[Mg(OH)2]��������c(Mg2+)?c2(OH��)��Ksp[Mg(OH)2]����5�����ݿ��Ʊ�����ƶԱ�ʵ��ԭ��ʵ��1��2��Ŀ����̽��I����Ũ�ȶԷ�Ӧ���ʵ�Ӱ�죬ʵ��2��4��Ŀ����̽��ClO����Ũ�ȶԷ�Ӧ���ʵ�Ӱ�죻��ʵ��1��3��֪��OH����Ũ�ȶ�������Ӱ�죬��ʵ��4�ı�pH��Ӧ������ʵ��4��ȣ���v="7.2" �� 10��4��
����ƽ�ⳣ������ʽ���Կ�������c(NH3��H2O)��c(Mg2+)�ı���ͬ�ij̶�ʱ��c2(NH3��H2O)�Գ������ɵ�Ӱ�����[�����c(Mg2+)?c2(OH��)��Ksp[Mg(OH)2]��������c(Mg2+)?c2(OH��)��Ksp[Mg(OH)2]����5�����ݿ��Ʊ�����ƶԱ�ʵ��ԭ��ʵ��1��2��Ŀ����̽��I����Ũ�ȶԷ�Ӧ���ʵ�Ӱ�죬ʵ��2��4��Ŀ����̽��ClO����Ũ�ȶԷ�Ӧ���ʵ�Ӱ�죻��ʵ��1��3��֪��OH����Ũ�ȶ�������Ӱ�죬��ʵ��4�ı�pH��Ӧ������ʵ��4��ȣ���v="7.2" �� 10��4��
�����Ѷȣ�����