1、选择题 实验室为标定一种烧碱样品的物质的量浓度,称取该烧碱样品4.0g配成1L溶液,取出20.00mL置于锥形瓶中,用0.10 mol・L-1 HCl标准溶液滴定,恰好完全中和时消耗标准盐酸19.00mL,若烧碱中只含有一种杂质,则不可能是(?)
A.NaCl
B.Ca(OH)2
C.Na2CO3
D.NaHCO3
2、填空题 在室温下,下列五种溶液:
①0.1mol/L NH4Cl
②0.1mol/L CH3COONH4
③0.1mol/L NH4HSO4
④0.1mol/L NH3・H2O和0.1mol/L NH4Cl的混合液
请根据要求填写下列空白:
(1)溶液①呈酸性,其原因是?_______________________________(用离子方程式表示)
(2)比较溶液②、③中c(NH4+)的大小关系是②?③(填“>”“=”或“<”)。
(3)在溶液④中,?离子的浓度为0.1mol/L;NH3・H2O和?离子的浓度之和为0.2 mol/L。
(4)室温下,测得溶液②的pH=7, CH3COO-与NH4+浓度的大小关系是:
c(CH3COO-)?c(NH4+)(填“>”“=”或“<”)。
3、选择题 已知酸H2B在水溶液中存在下列关系:①H2B = H++HB―,②HB―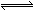 H++B2―,则下列说法中一定正确的是
H++B2―,则下列说法中一定正确的是
A.NaHB溶液一定呈酸性,Na2B溶液一定呈碱性
B.Na2B溶液一定呈碱性,NaHB溶液可能呈酸性也可能呈碱性
C.NaHB水溶液中一定有:c(Na )+c(H
)+c(H )=c(HB
)=c(HB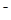 )+c(OH
)+c(OH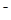 )+c(B
)+c(B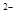 )
)
D.在Na2B溶液中一定有:c(OH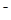 )=c(H
)=c(H )+c(HB
)+c(HB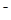 )
)
4、选择题 下列叙述正确的是(?)
A.浓度均为0.1 mol・L-1的CH3COOH与CH3COONa溶液等体积混合后溶液显酸性,
则:c(CH3COO-)<c(CH3COOH)
B.浓度均为0.1 mol・L-1的氨水与盐酸等体积混合后的溶液中:c(H+)=c(OH-) + c(NH3・H2O)
C.浓度均为0.1 mol・L-1的小苏打溶液和氢氧化钠溶液等体积混合:c(Na+)+ c(H+)= c(CO32-)+ c(OH-) + c(HCO3-)
D.用pH=3的盐酸滴定10 mL pH=11的氨水,达到滴定终点用去盐酸的体积小于10 mL
5、选择题 下列溶液中,各关系式正确的是()
A.等浓度、等体积的NaOH 和二元弱酸H2A 混和溶液中:
c(Na+) + c(H+) =c(HA-) + c(OH-) + c(A2-)
B.1 L 0.1 mol?L-1 CuSO4・(NH4)2SO4・6H2O 的溶液中:
c(SO42―) >c(NH4+)>c(Cu2+)>c(H+)>c(OH―)
C.已知两种弱酸HA、HB 的电离平衡常数Ka(HA)>Ka(HB),常温下0.1 mol?L-1的HA、HB、NaA、NaB 溶液中:pH(NaA)>pH(NaB)>pH(HA)>pH(HB)
D.物质的量浓度相等的Na2CO3和NaHCO3溶液等体积混合后的溶液中:
3c(H2CO3)+2c(H+)+c(HCO3―)=2c(OH―)+c(CO32―)