1、计算题 一定温度下的密闭容器中存在如下反应:CO(g)+H2O(g)  CO2(g)+H2(g),已知CO(g)和H2O(g)的起始浓度均为2mol・L-1,经测定该反应在该温度下的平衡常数K=1,试判断:
CO2(g)+H2(g),已知CO(g)和H2O(g)的起始浓度均为2mol・L-1,经测定该反应在该温度下的平衡常数K=1,试判断:
(1)当CO转化率为25%时,该反应是否达到平衡,若未达到,向哪个方向进行?
(2)达到平衡时,CO的转化率为多少?
(3)当CO的起始浓度仍为2mol・L-1,H2O(g)的起始浓度为6mol・L-1,求平衡时CO的转化率?
参考答案:(1)反应未达到平衡, 平衡正方向移动 (2分)
(2)50%?(3分)?(3)75%?(3分)
本题解析:
CO(g) + H2O(g)  CO2(g)+H2(g)
CO2(g)+H2(g)
起始? 2? 2? 0? 0
转化? 0.5? 0.5? 0.5? 0.5
平衡量? 1.5? 1.5? 0.5? 0.5
Q=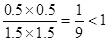 ?所以未达到平衡。
?所以未达到平衡。
(2)平衡时CO的物质的量浓度为1mol/L,所以转化率为50%。
(3)CO(g) + H2O(g)  CO2(g)+H2(g)
CO2(g)+H2(g)
起始? 2? 6? 0? 0
转化? x? x? x? x
平衡量? 2-x? 6-x? x? x
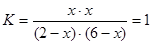 ?可知x=1.5?则平衡时CO的转化率为75%。
?可知x=1.5?则平衡时CO的转化率为75%。
本题难度:简单
2、选择题
达到平衡后,下列说法中一定正确的是
A.平衡时,用A的浓度变化表示的正反应速率是用B的浓度变化表示的逆反应速率的a/b倍
B.保持容器内气体压强不变,再通入稀有气体,平衡不移动
C.保持容器体积不变,再通入一定量的C,建立新的平衡状态时,A的体积分数与原平衡时相同
D.保持容器体积不变,增加B的物质的量,建立新的平衡状态时,A的转化率升高
参考答案:AD
本题解析:本题考查化学平衡有关知识,属中等难度。平衡状态时,υ(A)/υ(B)=a/b,故A正确。压强不变,通入稀有气体,则平衡体系的压强减小,由于a、b、c三者数值不确定,故无法判断是否发生移动,B错误。保持容器体积不变,再通入一定量的C,建立新的平衡状态与原平衡互为等效平衡,故A的体积分数与原平衡时相同,C正确。增加B的用量,平衡必向正反应方向移动,A的转化率升高,D正确。
本题难度:一般
3、选择题 某密闭容器中发生如下反应:X(g)+3Y(g) 2Z(g);△H<0,下图表示该反应的速率(v)随时间(t)变化的关系,t1、t3、t4时刻外界条件有所改变,但都没有改变各物质的初始加入量。下列说法中不正确的是
2Z(g);△H<0,下图表示该反应的速率(v)随时间(t)变化的关系,t1、t3、t4时刻外界条件有所改变,但都没有改变各物质的初始加入量。下列说法中不正确的是
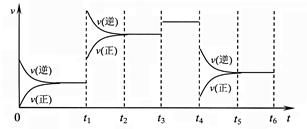
A.t1时升高了温度
B.t3时加入了催化剂
C.t5~t6时刻,Y转化率最小
D.在t3~t4时间内,X的体积分数最大
参考答案:D
本题解析:由图可知反应从逆向发生,根据影响化学反应速率的因素可知,t1时升温,t3时加入了催化剂,t5~t6时刻,Y转化率最小,在t5~t6时X体积分数最大
本题难度:一般
4、选择题 将4mol?A气体和2?mol?B气体在体积为2?L的密闭容器中混合,并在一定条件下发生如下反应:
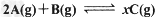 若经2?s后测得A的物质的量为2.8?mol,?C的浓度为0.6?mol/L。现有下列几种说法,其中正确的是?
若经2?s后测得A的物质的量为2.8?mol,?C的浓度为0.6?mol/L。现有下列几种说法,其中正确的是?
[? ]
①2s内用物质A表示的平均反应速率为0.3?mol/(L・s)
②2s内用物质B表示的平均反应速率为0.6?mol/(L・s)
③2s时物质B的转化率为70%
④x=2?
A.①③?
B.①④?
C.②③?
D.③④?
参考答案:B
本题解析:
本题难度:简单
5、选择题 已知常温常压和催化剂条件下,N2(g)和H2(g)生成2 mol NH3(g)放出92.4 kJ的热量。在上述条件下向密闭容器中通入1 mol N2和3 mol H2,达到平衡时放出热量为Q1 kJ;向另一体积相同的容器中通入0.9 mol N2、2.7 mol H2和0.2 mol NH3,相同条件下达到平衡时放出热量为Q2 kJ。则下列关系式正确的是(? )
A.2Q=Q1="92.4"
B.Q2<Q1<92.4
C.Q1<Q2<92.4
D.Q1=Q2=92.4
参考答案:B
本题解析:根据题意,每生成2 mol NH3放出92.4 kJ热量,1 mol N2和3 mol H2反应,达到平衡态,生成NH3小于2 mol,故放出热量小于92.4 kJ;另一容器中通入0.9 mol N2、2.7 mol H2和0.2 mol NH3,相同条件下达到平衡时与上述平衡是等效平衡,但由于充入了NH3,所以N2和H2反应生成的NH3比上述平衡少,故有Q2<Q1<92.4。
本题难度:简单