|
|
|
���л�ѧ֪ʶ����ɡ���Ӧ������ƽ����йؼ��㡷��Ƶ���㹮�̣�2017��ģ��棩(һ)
2018-03-17 06:32:10
��Դ:91������
����:www.91exam.org �� �� �� ��
|
1������� ij�¶�ʱ����һ��2L���ܱ������У�H2��N2��NH3�������ʵ����ʵ�����ʱ��ı仯������ͼ��ʾ������ͼ�����ݣ��ش��������⣺

��1��ͼ��X���ߴ���?���ѧʽ����
��2���ӿ�ʼ��2min��NH3��ƽ����Ӧ������?��
��3����4����ʱ����������ȷ����?��
A���÷�Ӧ��ֹͣ
B����λʱ���ڵ������������ʵ�����������������
C��3v(H2)=2v(NH3)
D��c(H2) ��c(N2) ��c(NH3) =" 7" ��9 ��2
| ��4������1 mol H��H����1 mol N��H����1 mol N��N���ֱ���Ҫ���յ�����Ϊ436 kJ��391 kJ��946 kJ����1 mol N2��3mol H2��Ӧ��ȫת��ΪNH3Ӧ_________����(����ա��ų���)??kJ��
2��ѡ���� �Կ��淴Ӧ2A(s)��3B(g) C(g)��2D(g)����H��0����һ�������´ﵽƽ�⣬�����й�������ȷ����(����) C(g)��2D(g)����H��0����һ�������´ﵽƽ�⣬�����й�������ȷ����(����)
������A������ƽ��������Ӧ�����ƶ�?
�������¶ȣ�ƽ�����淴Ӧ�����ƶ���v(��)��С
��ѹǿ����һ����ƽ�ⲻ�ƶ���v(��)��v(��)����?
������B��Ũ�ȣ�v(��)��v(��)
�ݼ��������B��ת�������
A���٢�
B����
C����
D���ܢ�
3������� ����0��10mol MnO2��ĩ��50mL H2O2��Һ�У��ڱ�״���·ų�����������ʱ��Ĺ�ϵ��ͼ��ʾ��
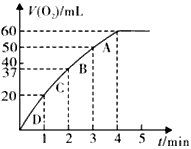
��1��д��H2O2�ڶ������������·�����Ӧ�Ļ�ѧ����ʽ____________________��
��2��ʵ��ʱ�ų�������������_____________mL��
��3���ų�1/3��������ʱ��Ϊ_____________min��
��4����Ӧ�ų�3/4��������ʱ��ԼΪ_____________min��
��5��A��B��C��D���㷴Ӧ���ʿ�����˳��Ϊ_____��____��____��____��
��6�����ͷ�Ӧ���ʱ仯��ԭ��__________________________��
��7������H2O2�ij�ʼ���ʵ���Ũ��_____________�����뱣����λ��Ч���֣�
4������� (14��)��2011��11��28����12��9�գ����Ϲ�����仯��ܹ�Լ��17�ε�Լ���������Ϸǵ°��ٿ����������������ЧӦ����Դ��ȱ����������ӣ���ν��ʹ�����CO2�ĺ�������Ч�ؿ�������CO2�������˸������ձ����ӡ�
��1��Ŀǰ��ҵ����һ�ַ�������CO2������ȼ�ϼ״���Ϊ̽���÷�Ӧԭ������������ʵ�飬�����Ϊ1L���ܱ������У�����1mol CO2��3.25 mol H2����һ�������·�����Ӧ���ⶨCO2��CH3OH(g)��H2O (g)��Ũ����ʱ��仯��ͼ��ʾ��
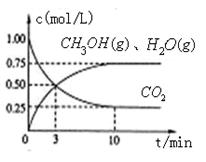
��д���ù�ҵ������ȡ�״��Ļ�ѧ��Ӧ����ʽ������������������
�ڴӷ�Ӧ��ʼ��ƽ�⣬������ƽ����Ӧ����v (H2)����?? �� ��
�۸�������CO2��ת����Ϊ��?�����¶Ƚ���ʱCO2��ת���ʱ����÷�Ӧ?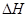 ?����������������������� ?�����������������������
�����д�ʩ����ʹn(CH3OH)/n(CO2)�����������������������
A�������¶�
B�����뵪��
C����ˮ��������ϵ�з���
D���ø���Ч�Ĵ���
|
��2��ѡ�ú��ʵĺϽ���Ϊ�缫�����������ơ��״���ˮ������Ϊԭ�ϣ������Ƴ�һ���Լ״�Ϊԭ�ϵ�ȼ�ϵ�أ���ȼ�ϵ�ظ����ĵ缫����ʽΪ
������������������������
���о�NO2 ?��SO2 ��CO�ȴ�����Ⱦ����Ĵ���������Ҫ���塣���е�Ԫ�����Ŷ���̬�������Ļ���������ڹ�ũҵ�����������з�������Ҫ�����á�����������⣺
��1����֪��2SO2(g) + O2(g)

2SO3(g)? ��H=" ��196.6" kJ��mol�D1
2NO(g) + O2(g)

2NO2(g)? ��H= ��113.0 kJ��mol�D1
��ӦNO2(g) + SO2(g)

SO3(g) + NO(g) �Ħ�H=
??��
��2��һ�������£���NO2��SO2�������1:2�����ܱ������з���������Ӧ��
��������˵����Ӧ�ﵽƽ��״̬����
?(�����) ��
a����ϵѹǿ���ֲ���? b�����������ɫ���ֲ���
c��SO3��NO������ȱ��ֲ���? d����ͬʱ���ڣ�ÿ����1 molNO2��ͬʱ����1 mol SO3
�ڵ����������Ӧƽ��ʱNO2��SO2�����Ϊ1: 6����ƽ�ⳣ��K��
?��
5��ѡ���� ����3�������ȵ��ܱ����������������з�Ӧ��CO2(g)��H2(g) ?H2O(g)��CO(g)����Ӧ�������¶���ͬ������ʼŨ�Ȳ�ͬ�����мף�CO2 = H2 =" a" mol���ң�CO2 =" a" mol ��H2 =" 2a" mol ������CO2 =H2 =H2O(g)=" a" mol ���ﵽƽ��ʱ��CO2�����ʵ����ɴ�С��˳����
?H2O(g)��CO(g)����Ӧ�������¶���ͬ������ʼŨ�Ȳ�ͬ�����мף�CO2 = H2 =" a" mol���ң�CO2 =" a" mol ��H2 =" 2a" mol ������CO2 =H2 =H2O(g)=" a" mol ���ﵽƽ��ʱ��CO2�����ʵ����ɴ�С��˳����
A����>��>��
B����>��>��
C����>��>��
D����>��>��
 2SO3(g)? ��H=" ��196.6" kJ��mol�D1
2SO3(g)? ��H=" ��196.6" kJ��mol�D1 2NO2(g)? ��H= ��113.0 kJ��mol�D1
2NO2(g)? ��H= ��113.0 kJ��mol�D1 SO3(g) + NO(g) �Ħ�H= ??��
SO3(g) + NO(g) �Ħ�H= ??�� ?H2O(g)��CO(g)����Ӧ�������¶���ͬ������ʼŨ�Ȳ�ͬ�����мף�CO2 = H2 =" a" mol���ң�CO2 =" a" mol ��H2 =" 2a" mol ������CO2 =H2 =H2O(g)=" a" mol ���ﵽƽ��ʱ��CO2�����ʵ����ɴ�С��˳����
?H2O(g)��CO(g)����Ӧ�������¶���ͬ������ʼŨ�Ȳ�ͬ�����мף�CO2 = H2 =" a" mol���ң�CO2 =" a" mol ��H2 =" 2a" mol ������CO2 =H2 =H2O(g)=" a" mol ���ﵽƽ��ʱ��CO2�����ʵ����ɴ�С��˳����