1������� ����ѧʵ����ѧ���Ŀ����ڷ�����ᴿ���ʵķ����ܶ࣬��ᾧ�����ˡ����ȷֽ⡭�����뽫������ᴿ���и�����������˵ķ������������������ڡ�
(1)��ȥ��ʯ���л��е�ʯ��ʯ�� (? ?)
(2)��ȥ�Ҵ����ܽ������ʳ�Ρ� (? )
(3)̼����л�������̼���ơ� (? ? )
(4)������л�������ʳ�Ρ� (? ? )
(5)CO���CO2�� ( ? )
�ο��𰸣�(1)���·ֽ�
(2)����
(3)����
(4)�ᾧ
(5)ϴ��
���������
�����Ѷȣ�һ��
2��ʵ���� �{����������a-Fe2O3)���ִ����ӹ�ҵ��Ҫ���ϡ�ʵ���������������� (Fe2O3��FeO��SiO2��)Ϊԭ���Ʊ��{���������IJ������¡���ش��й����⣺
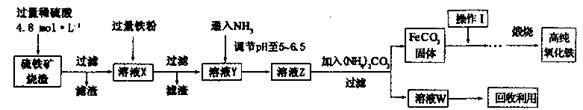
��1�����˲����еIJ�������Ϊ________��
��2��ʵ������240mL4.8mol ? L��1��������Һ������18.4 mol ? L��1��Ũ����������ƣ�����Ҫ������Ҫ����Ϊ________��
��3����ҺX������Ӧ�����ӷ���ʽΪ________��
��4��������μ�����ҺZ�е�������________��
��5������I��������________���о�W��һ����;________��
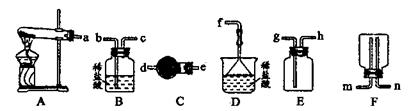
��6��?ijʵ��С����Ƶİ����Ʊ�ʵ������Ϊ:����װ�á��������ռ���β����������ӿڵ�����˳����_______________��
��7��������İ����ֱ�ͨ��ˮ�л�������,���õ�25��0.1 mol.L-1��NH3 ? H2O��Һ��NH4Cl��Һ���������ʵ�飬�Ƚ�NH3 ? H2O�ĵ���̶Ⱥ�NH4Cl��ˮ��̶ȴ�С��
�ο��𰸣���ÿ��2�֣���14�֣���1��©�����ձ�������������һ���1�֣�����2�֣�
��2��250ml����ƿ��ľ�ݻ����÷֣� ��3��2Fe3����Fe��3Fe2��
��4��ȡ������ҺZ���Թ��У�Ȼ�����ϡ���ᣬ�����������ټ���BaCl2��Һ���а�ɫ����������֤����SO42���� ��5��ϴ�ӣ�1�֣������ڻ��ʣ�1�֣� ��6��a��e��d��h��g��f
��7�������£��������ʵ���Ũ�ȣ�0.1mol/L����������İ�ˮ��NH4Cl��Һ��ϣ������ҺpH��7����������̶ȴ���ˮ��̶ȣ��������̶�С��ˮ��̶ȡ�����pH�Ʒֱ��25��ʱ0.1mol/L������NH4Cl��Һ��pH��Ȼ��Ƚ�c(OH��)��c(H��)����c(OH��)��c(H��)��������̶ȴ���ˮ��̶ȣ���c(OH��)��c(H��)��������̶�С��ˮ��̶ȡ�
�����������1�����˲����е�����������̨������Ȧ����©�����ձ��������������в���������©�����ձ�����������
��2������û��250ml����ƿ������Ҫ����240mlϡ���ᣬ����Ҫ������Ҫ����Ϊ250ml����ƿ��
��3��������ҺX�к��������ӣ���˼������۷�����Ӧ�����ӷ���ʽΪ2Fe3����Fe��3Fe2����
��4����������ͼ��֪����ҺY���Ȼ�����������Ļ��Һ��ͨ�백������������泥������ҺZ�к���SO42��������SO42���IJ�����ȡ������ҺZ���Թ��У�Ȼ�����ϡ���ᣬ�����������ټ���BaCl2��Һ���а�ɫ����������֤����SO42����
��5���������Һ�й��˳�������Ҫϴ�ӡ���˲���I��������ϴ�ӣ���ҺZ�м���̼��狀�����̼������������泥����W������泥�����Ҫ��;�����ڻ��ʡ�
��6������װ��ͼ��֪��A�Ƿ���װ�á����ڰ����ܶ�С�ڿ����Ҽ�������ˮ��������Eװ���ռ�������Dװ�ý���β�����ա��������ɵİ����к���ˮ���������Ҫ����ܸ��ﰱ����������ȷ������˳����a��e��d��h��g��f��
��7��Ҫ�Ƚ�NH3 ? H2O�ĵ���̶Ⱥ�NH4Cl��ˮ��̶ȴ�С������ͨ��������Ũ�ȡ�������Ķ����Һ��pH����ֱ�Ӳ�����Ũ����Һ��pH���������£��������ʵ���Ũ�ȣ�0.1mol/L����������İ�ˮ��NH4Cl��Һ��ϣ������ҺpH��7����������̶ȴ���ˮ��̶ȣ��������̶�С��ˮ��̶ȡ�����pH�Ʒֱ��25��ʱ0.1mol/L������NH4Cl��Һ��pH��Ȼ��Ƚ�c(OH��)��c(H��)����c(OH��)��c(H��)��������̶ȴ���ˮ��̶ȣ���c(OH��)��c(H��)��������̶�С��ˮ��̶ȡ�42���ļ��飻�����Ʊ����ռ��������Լ�β������������̶���ˮ��̶ȱȽϵ�ʵ�鷽������Ƶ�
�����Ѷȣ�����
3��ѡ���� ����ʵ�������ȷ���ǣ�������
A��ʵ������ȡ����ˮ��ʵ�飬���¶ȼ�ˮ�����������ˮ��
B����Һʱ����Һ©���²�Һ���ȴ��¿ڷų����ϲ�Һ���ٴ��¿ڷų�
C��ŨNaOH��Һ����Ƥ���ϣ������ô���ˮ��ϴ��Ȼ��Ϳ��ϡ������Һ
D������������Һʱ����������Ͳ�м���һ�������ˮ���߽��������ע��Ũ����
�ο��𰸣�C
���������
�����Ѷȣ�һ��
4��ѡ���� ����ʵ���������ȷ���ǣ�?��
A���������ʱ��Ӧ��������ƿ�м��뼸���ʯ���Է�ֹ����
B����������ʱ��Ӧʹ������е�ˮ����ȫ���ɺ���ֹͣ����
C����������ʱ���Ƚ���Һ©�����²�Һ����¿ڷų����ٽ��ϲ�Һ����¿ڷų�
D����ȡ����ʱ������ѡ��CCl4��ƾ���Ϊ��ȡ������ˮ����ȡ��
�ο��𰸣�A
���������A����ʱ�����ӷ�ʯ�����Ƭ��Һ�������ҷ������������ˮ�ͱȽ�ƽ�ȣ��ʿɷ�ֹ���С���ȷ��B����ʱ��Һʣ������Ҫֹͣ���ȣ��������Ƚ�ˮ�����ɡ�����C��������ʱ������Һ©�����²�Һ����¿ڷų����ٽ��ϲ�Һ����Ͽڵ���������D��ȡ����ʱ��ֻ��ѡ��CCl��Ϊ��ȡ������ˮ����ȡ�壬�ƾ���ˮ���ܣ���������ȡ��������
�����Ѷȣ�һ��
5��ѡ���� Ҫ���������ʵĹ�ҵ�Ҵ��ᴿ��ͨ�����õķ�����
A������
B���ؽᾧ
C������
D����ȡ
�ο��𰸣�A
�����������ȡ�ʺ��������ڲ�ͬ�ܼ��е��ܽ��Բ�ͬ�������һ�ַ������ᾧ�������ڲ�ͬ���ʵ��ܽ�����¶�Ӱ�첻ͬ�������һ�ַ��������������ݻ�����и�����ַе㲻ͬ�������һ�ַ��������ڳ�ȥ�ӷ����ѻӷ��ӷ����ʣ����������ڲ����Թ����Һ��֮���һ�ַ��뷽�����Ҵ���ˮ���ܣ����е㣨78�棩����ˮ�ģ������ϴ�����ҪҪ���������ʵĹ�ҵ�Ҵ��ᴿ��ͨ�����õķ���������ѡA��
�����Ѷȣ�һ��