1�������� ��8�֣�ij������FeC13��Һ��ʴ����ͭ�ľ�Ե������ӡˢ��·��
��1�������ӷ���ʽ��ʾ�仯ѧԭ��?��
ijʵ��С���ͬѧ�Ըó�����ӡˢ��·�����õķ�Һ�����˷�����ȡ50��00 mL����Һ�������м���0��64 g����ͭ������ͭȫ���ܽ⣻��ȡ50��00 mL��Һ�������м�������AgNO3��Һ����������43��05 g����ش��������⣺
��2���ó��������Һ������������������
��3���ó�ԭ��ʹ�õ�FeCl3��Һ�����ʵ���Ũ��Ϊ?�����跴Ӧǰ����Һ������ޱ仯����
��4������500��00 mL��Һ�м���������ϡ���ᣬ��
��״��������NO����4��48 L����ԭ��Һ�и�
���������ӵ����ʵ���Ũ��֮��Ϊ?������
�����ֵһһ��Ӧ����
�ο��𰸣�

�����������
�����Ѷȣ�һ��
2������� ��ͼ��ʾ����ͼ1��ͼ2����װ�в�ͬ���ʵ���Ͳ�õ���������������ͼ2��Ͳ�ڵ�����ѹ������Ͳ�ڣ������±����еIJ�ͬʵ�飨������ͬ��ͬѹ�²ⶨ����ҺŨ����ͬ����
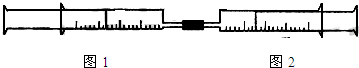
�Իش��������⣺
| ʵ����� | ͼ1��Ͳ������ | ͼ2��Ͳ������ | ͼ1��Ͳ������
1
10mLFeSO4��Һ
10mLNH3
���ɰ�ɫ���������ɫ
2
10mL1mol/LAlCl3��Һ
40mL1mol/LNaOH��Һ
______
3
10mL��ɫʯ����Һ
25mLCl2
______
4
15mLCl2
40mLNH3
______
|
��1��ʵ��1�У��������ձ�Ϊ______ɫ��д��������ɫ�Ļ�ѧ����ʽ______��
��2��ʵ��2ͼ1��Ͳ�ڵ������ǣ�______��д���йط�Ӧ�����ӷ���ʽ��______��______��
��3��ʵ��3ͼ1��Ͳ�ڵ������ǣ�______����Ӧ��ͼ2��Ͳ���������IJ������壬��ȷ�Ĵ��������ǽ���ͨ��______��Һ�У�
��4��ʵ��4�У���֪��3Cl2+2NH3=N2+6HCl��ͼ1��Ͳ���������ƶ�����Ͳ���а��̲����⣬�������ɫ�仯Ϊ______��
�ο��𰸣���1��NH3+H2O?NH3?H2O?NH4++OH-��FeSO4+2NH3?H2O�TFe��OH��2��+��NH4��2SO4��Fe��OH��2Ϊ��ɫ�������ڿ������ױ������е�����������������Ӧ��4Fe��OH��2+O2+2H2O�T4Fe��OH��3��Fe��OH��3Ϊ���ɫ��
�ʴ�Ϊ����֣�4Fe��OH��2+O2+2H2O=4Fe��OH��3��
��2��10mL1mol/L��AlCl3��Һ��40mL1mol/L��NaOH��Һ��Ӧ��0.01molAlCl3��0.04molNaOH?��Ӧ������?
? Al3++3OH-=Al��OH��3��? Al��OH��3 +OH?-=AlO2-+2H2O
?0.01mol? 0.03mol?0.01mol?0.01mol?0.01mol?0.01mol?
? ����Ϊ�����а�ɫ������������ܽ⣮
�ʴ�Ϊ�����а�ɫ������������ܽ⡢Al3++3OH-=Al��OH��3����Al��OH��3+OH-=AlO2-+2H2O��
��3��Cl2+H2O?HCl+HClO��HCl��HClO���������ԣ���ʹ��ɫʯ����Һ��죬HClO����ǿ�����ԣ���Ư��ָʾ����ɫ��ȥ��Cl2+2NaOH�TNaCl+H2O+NaClO
����������NaOH���գ�
�ʴ�Ϊ���ȱ�����ɫ��NaOH��
��4�����ݷ���ʽ��֪��3Cl2+2NH3�TN2+6HCl?
? 15mL? 10mL? 5mL? 30mL
����30mLHCl��ʣ���NH3Ϊ30mL��
��NH3+HCl�TNH4Cl?
?30mL? 30mL?
��֪�����ɵ�HCl��ʣ���NH3ǡ����ȫ��Ӧ����NH4Cl�����ŷ�Ӧ�Ľ��У�Cl2�������٣�������ȫ��Ӧ��
�������ʣ�������Ϊ5mL��ɫ��N2��
�ʴ�Ϊ������ɫ��Ϊ��ɫ��
���������
�����Ѷȣ�һ��
3��ʵ���� ����������һ�ֿ���������ȱ����ƶѪ��ҩ������������ҩƬ�������һ�����Ƶ����£��Ա��������������������е�������������������������������ƶѪ��ҩЧ���������һ��ʵ�鷽������֤ij��������ҩƬ�Ƿ��ѱ�������д����Ҫʵ�鲽�衢������йط�Ӧ���ӵķ���ʽ��
��1����Ҫ���裺________________________________________________________��
��2�����ӷ���ʽ��______________________________________________________��
�ο��𰸣���1����ȥҩƬ�����£���ҩƬ���飬�����ձ��м���������ˮ�ܽ⣬�μ���KSCN��Һ������Һ�Ժ�ɫ�������������ѱ�����
��2��Fe3++SCN-�T�TFe��SCN��2+
���������FeSO4������������Fe2��SO4��3����֤ҩƬ�Ƿ��ѱ�����ֻ������Ƿ�Fe3+���ɡ�����Fe3+�Ĵ���һ����KSCN��
�����Ѷȣ���
4��ʵ���� ��12�֣�(1)���������Ҫ�ɷ���Fe3O4�������Ҳ���Ա�ʾ��FeO��Fe2O3�����ṩ�����Լ�������ѡ����ʵ�ҩƷ��֤��������ʯ�д���+2����Ԫ�ء�
�Լ���ϡ���ᡢϡ���ᡢϡ���ᡢNaOH��Һ��KSCN��Һ��KMnO4��Һ����ˮ
���輰����
ȡ����������ʯ��Ʒ�����������_______�ܽ⣬ȡ�ܽ���Һ������������__________________���۲쵽________ __________________________________����֤��������ʯ�д���+2����Ԫ�ء�
__________________________________����֤��������ʯ�д���+2����Ԫ�ء�
��2����Fe2+��NO-3��Fe3+��NO��H+��H2O�������ӣ��ֱ�����ͬһ������ԭ��Ӧ�еķ�Ӧ��������
����д���÷�Ӧ�����ӷ���ʽ����Ҫ����ƽ��?��
�ڸ÷�Ӧ���������뻹ԭ�������ʵ���֮��Ϊ?��
�۲���2mol��ԭ����ʱת�Ƶ��ӵ�����Ϊ?��
�ο��𰸣���1��ϡ�������KMnO4��Һ������ɫ��ȥ
��2����Fe2����H����NO3����Fe3����NO����H 2O
2O
��1�s3?
��6NA
�����������
�����Ѷȣ�һ��
5��ʵ���� ����������FeC2O4�������������Լ�����Ӱ���Լ����͵�ز�����������﮵����������������ڸ�������ʱ�����ܹ��ֽ�,��ȤС��Բ��������ķֽ���������ʵ���̽��������֪��CO�����Ȼ���[PdC12]��Һ��Ӧ���ɺ�ɫ���ٷۡ���
��1�������������ֽ�������������ͨ������ʯ��ˮ���Ȼ�����Һ���۲쵽����ʯ��ˮ����ǣ��Ȼ�����Һ���к�ɫ�������ɡ�˵�������������?�����ѧʽ��
��2��̽�����������ֽ�õ��ĺ�ɫ�����������Ԫ�صĴ�����ʽ��
���������⡿
���������ֽ��õ��ĺ�ɫ������ʲô��
��������衿
����1��?������2��FeO������3��FeO��Fe�Ļ���
��ʵ�鷽����
��ѡ�Լ������ᡢ��ˮ��CuSO4��Һ��KSCN��Һ������ˮ��
ʵ�鲽��
| ʵ������
| ʵ�����
|
����1�����Թ��м��������������ټ�������?�������
| ����Һ��ɫ���Ըı䣬
���к�ɫ�������ɡ�
| ��Fe���ڡ�
|
����2��������1�еõ�����Һ���ˣ���������ˮ������ϴ����ϴ��Һ����ɫ��
| ?
| ?
|
����3��ȡ����2�õ��������������Թ��У��μӹ������ᣬ���ú�ȡ�ϲ���Һ��?
?��
| ?
?��
| ��FeO���ڡ�
|
?
����˼������
����ȤС�����۷�����Ϊ����������ֱ�ӷֽ����ù������Ӧ����FeO�������չ�������л�����Fe����Ϊ?��д��ѧ����ʽ����
��3������ʵ��̽���ͷ�˼��д�����������ڸ�������ʱ����ֱ�ӷֽ�Ļ�ѧ����ʽ?��
�ο��𰸣���1��CO��CO2����2�֣����1����1�֣�
(2)��������衿Fe����(��1��Դ:91������ 91EXAm.org��)
��ʵ�鷽����
ʵ�鲽��
ʵ������
����1��CuSO4��Һ����1�֣�
?
����3���μ�������ˮ�������μ�KSCN��Һ����2�֣��ӡ���ˮ���͡�KSCN��Һ������1�֣�˳����Եߵ���
��Һ�ʺ�ɫ����1�֣�ʵ������ߵ���ע���Ӧ����ͬ��
?
����˼������FeO+CO Fe+CO2
Fe+CO2
��3��FeC2O4 FeO+CO��+CO2�� (��2��)
FeO+CO��+CO2�� (��2��)
�����������1������ʯ��ˮ����ǣ��Ȼ�����Һ���к�ɫ�������ɣ�˵�����������ֽ����������к���CO2��CO����̼Ԫ�ؼ���+3�����ߵ�+4�ۣ�����+3�۽��͵�+2�ۣ��ɴ˿�֪FeC2O4 FeO+CO��+CO2������2������CO����ǿ��ԭ�ԣ����ܽ�FeO��ԭΪFe����FeO+CO
FeO+CO��+CO2������2������CO����ǿ��ԭ�ԣ����ܽ�FeO��ԭΪFe����FeO+CO Fe+CO2�������1Ϊ����Fe����3������ѡ����֪�Լ���ʵ���������ƣ�����1�ķ�ӦΪFe+CuSO4=FeSO4+Cu��FeO+2HCl=FeCl2+H2O��FeCl2��KSCN��Һ����죬����ˮ�ܽ�������ΪFeCl3��FeCl3��KSCN��죻��3���ԡ�
Fe+CO2�������1Ϊ����Fe����3������ѡ����֪�Լ���ʵ���������ƣ�����1�ķ�ӦΪFe+CuSO4=FeSO4+Cu��FeO+2HCl=FeCl2+H2O��FeCl2��KSCN��Һ����죬����ˮ�ܽ�������ΪFeCl3��FeCl3��KSCN��죻��3���ԡ�
�����Ѷȣ�һ��