1、填空题 (每空4分,共12分)
(1)已知:TiO2(s)+2Cl2 (g)===TiCl4(l)+O2(g) ΔH=+140 kJ・mol-1
2C(s)+O2(g)===2CO(g) Δ H=-221 kJ・mol-1
写出TiO2和焦炭、氯气反应生成TiCl4和CO气体的热化学方程式: 。
(2)在25℃,101KPa时,CO的燃烧热为280kJ/mol,写出 CO的燃烧热的热化学方程式: 。
(3)在火箭推进器中以肼(N2H4)作为燃料,可以选O2或NO2作为氧化剂,如果以氧气作为氧化剂,其化学反应与能量关系如下,
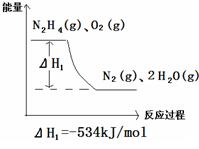
请写出该反应的热化学方程式
参考答案:(1)TiO2(s)+2Cl2(g)+2C(s)=TiCl4(l)+2CO(g) ΔH=-81 kJ・mol-1,
(2)CO(g)+1/2O2(g)=CO2(g) △H=-280kJ/mol
(3) N2H4(g)+ O2(g) =N2(g)+2H2O (g) △H=-534kJ/mol
本题解析:(1)根据盖斯定律,一式加二式可得;TiO2(s)+2Cl2(g)+2C(s)=TiCl4(l)+2CO(g) ΔH=-81 kJ・mol-1;(2)燃烧热是1mol物质完全燃烧生成稳定化合物时放出的热量,则CO的燃烧热的热化学方程式为CO(g)+1/2O2(g)=CO2(g) △H=-280kJ/mol(3)根据图像可知,该反应是放热反应,反应的热化学方程式为N2H4(g)+ O2(g) =N2(g)+2H2O (g) △H=-534kJ/mol。
考点:考查热化学方程式的书写。
本题难度:一般
2、选择题 已知N2+O2=2NO为吸热反应,△H=180kJ/mol,其中N≡N、O=O键的键能分别为946kJ/mol、498kJ/mol,则N-O键的键能为
[? ]
A.1264kJ/mol
B.632kJ/mol
C.316kJ/mol
D.1624kJ/mol
参考答案:B
本题解析:
本题难度:简单
3、填空题 现有①Ar?②金刚石?③NH4Cl?④SiO2?⑤干冰?⑥K2S六种物质,按下列要求回答:(填序号)
(1)只存在共价键的是__? ___,既存在离子键又存在共价键的是?。
(2)熔化时不需要破坏化学键的是_______,熔化时需要破坏共价键的是?。
参考答案:⑴②④,③,⑵①⑤,②④
本题解析:查化学键的判断。一般活泼的金属和活泼的非金属容易形成离子键,非金属元素的原子间容易形成共价键,所以①~⑥中含有的化学键分别是没有、非极性键、离子键和极性键、极性键、极性键、离子键。①⑤是分子晶体,熔化不需要破坏化学键。其余熔化均需要平衡化学键。
本题难度:一般
4、选择题 在指定溶液中,下列各组离子一定能大量共存的是
A.pH=1的溶液:Fe2+、Mg2+、NO3-、SO42-
B.由水电离出的c(H+)=1×10-13mol/L的溶液:HCO3-、K+、SO42-、Cl-
C.含大量Fe3+的溶液:NH4+、Na+、SCN-、Cl-
D.pH=13的溶液:Na+、K+、AlO2-、CO32-
参考答案:D
本题解析:分析:A.pH=1的溶液呈酸性,在酸性条件下反应的离子不能大量共存;
B.由水电离出的c(H+)=1×10-13mol/L的溶液可能呈酸性,也可能呈碱性;
C.含大量Fe3+的溶液,与Fe3+反应的离子不能大量共存;
D.pH=13的溶液呈碱性,如离子之间不发生任何反应,则可大量共存.
解答:A.pH=1的溶液呈酸性,酸性条件下Fe2+与NO3-发生氧化还原反应而不能大量共存,故A错误;
B.由水电离出的c(H+)=1×10-13mol/L的溶液可能呈酸性,也可能呈碱性,无论酸性还是碱性,HCO3-都不能大量共存,故B错误;
C.含大量Fe3+的溶液,与Fe3+反应的SCN-离子不能大量共存,故C错误;
D.pH=13的溶液呈碱性,离子之间不发生任何反应,可大量共存,故D正确.
故选D.
点评:本题考查离子共存问题,综合考查学生化学知识的应用能力,为高考常见题型,注意把握常见离子的性质,把握提给信息,为解答该题的关键,注意A发生氧化还原反应的特点,为易错点,题目难度中等.
本题难度:困难
5、选择题 已知:①101 kPa时,C(s)+1/2O2(g)===CO(g) ΔH1=-110.5 kJ/mol;
②稀溶液中,H+(aq)+OH-(aq)===H2O(l) ΔH2=-57.3 kJ/mol
下列结论正确的是
A.若碳的燃烧热用ΔH3来表示,则ΔH3<ΔH1
B.若碳的燃烧热用ΔH3来表示,则ΔH3>ΔH1
C.浓硫酸与稀NaOH溶液反应的中和热为-57.3 kJ/mol
D.稀醋酸与稀NaOH溶液反应生成1 mol水,放出57.3 kJ热量