|
|
|
高考化学试题《化学反应与能量》试题巩固(2017年最新版)(九)
2018-03-17 07:04:28
来源:91考试网
作者:www.91exam.org 【 大 中 小】
|
1、填空题 (12分)(1)“嫦娥一号”登月成功,实现了中国人“奔月”的梦想.“嫦娥一号”使用的推进剂是液氢和液氧,这种推进剂的优点是相同质量时,氢气放出的热量多,产物为水无污染。
已知:H2(g)+O2(g)=H2O(l) ΔH=-285.8 kJ/mol ; H2(g)=H2(l) ΔH=-0.92 kJ/mol
O2(g)=O2(l) ΔH=-6.84 kJ/mol ; H2O(l)=H2O(g) ΔH=+44.0 kJ/mol
请写出液氢和液氧生成气态水的热化学方程式:_______________________________.
(2)已知:①NH3(g)+HCl(g)===NH4Cl(s) ΔH=-176 kJ/mol
②NH3(g)+H2O(l)===NH3・H2O(aq) ΔH=-35.1 kJ/mol
③HCl(g)===HCl(aq) ΔH= -72.3 kJ/mol
④NH3・H2O(aq)+HCl(aq)===NH4Cl(aq)+H2O(l) ΔH=-52.3 kJ/mol
则NH4Cl(s)===NH4Cl(aq)的ΔH=______
(3)分别取40 mL的0.50 mol/L盐酸与0.55 mol/L氢氧化钠溶液进行中和反应.通过测定反应过程中所放出的热量可计算中和热.请回答下列问题.
① 理论上稀强酸、稀强碱反应生成1 mol水时放出57.3 kJ的热量,写出表示稀硫酸和稀氢氧化钠溶液反应的中和热的热化学方程式 __
② 假设盐酸和氢氧化钠溶液的密度都是1 g/cm3,又知中和后生成溶液的比热容
c=4.18 J/(g・℃).为了计算中和热,实验时还需测量的数据有(填序号)__________;
A.反应前盐酸溶液的温度
B.反应前盐酸溶液的质量
C.反应前氢氧化钠溶液的温度
D.反应前氢氧化钠溶液的质量
| E.反应后混合溶液的最高温度 F.反应后混合溶液的质量
③ 某学生实验记录数据如下:
实验
序号
| 起始温度t1/℃
| 终止温度t2/℃
| 盐酸
| 氢氧化钠
| 混合溶液
| 1
| 20.0
| 20.1
| 23.2
| 2
| 20.2
| 20.4
| 23.4
| 3
| 20.5
| 20.6
| 23.6
|
依据该学生的实验数据计算,该实验测得的中和热ΔH=__________ __;
④假定该学生的操作完全同上,实验中改用100 mL 0.5 mol/L盐酸跟100 mL 0.55 mol/L氢氧化钠溶液进行反应,与上述实验相比,所放出的热量________(填“相等”或“不相等”),所求中和热__________(填“相等”或“不相等”).
2、选择题 反应H2(g) +Br2(l) 2HBr(g)在25 ℃、101 kPa下进行, 已知生成2molHBr放出热量为72 kJ,蒸发1 mol Br2(l)需要吸收的能量为30 kJ,其他相关数据如下表: 2HBr(g)在25 ℃、101 kPa下进行, 已知生成2molHBr放出热量为72 kJ,蒸发1 mol Br2(l)需要吸收的能量为30 kJ,其他相关数据如下表:
1 mol分子中的化学键断时需要吸收能量/kJ
| H2(g)
| Br2(g)
| HBr(g)
| 436
| a
| 369
|
则表中a为
A.404 B.260 C.230 D.200
3、选择题 下列关于热化学反应的描述中正确的是
A.HCl和NaOH反应的中和热ΔH=-57.3 kJ/mol,则H2SO4和Ca(OH)2反应的中和热ΔH=2×(-57.3) kJ/mol
B.CO(g)的燃烧热是283.0 kJ/mol,则2CO2(g) =2CO(g)+O2(g)反应的ΔH=+566.0 kJ/mol
C.需要加热才能发生的反应一定是吸热反应
D.Ba(OH)2・8H2O与NH4Cl反应的焓变小于0,所以在常温下能自发进行
4、选择题 已知25℃、101 kPa下,拆开1 mol C―H键要吸收415 kJ的能量,拆开1 mol C―C键要吸收331 kJ的能量,拆开1 mol O2中的O==O键要吸收498 kJ的能量,形成水分子中的1 mol H―O键要放出465 kJ的能量,形成二氧化碳分子中的1 mol C==O键要放出798 kJ的能量。在丙烷燃烧过程中不考虑其他能量转化,
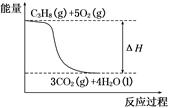
下列说法正确的是
A.丙烷完全燃烧的热化学方程式为C3H8+5O2===3CO2+4H2O ΔH=-2 036 kJ/mol
B.C3H8(g)+5O2(g)===3CO2(g)+4H2O(g);ΔH<-2 036 kJ/mol
C.丙烷完全燃烧的热化学方程式为:C3H8(g)+5O2(g)===3CO2(g)+4H2O(l) ΔH=2 036 kJ/mol
D.丙烷燃烧的能量变化可用上图表示
|
5、选择题 下列各组物质在溶液中的反应,不管反应物量的多少,都只能用同一个离子方程式来表示的是
A.FeBr2与Cl2
B.C6H5ONa与CO2
C.HCl与Na2CO3
D.Ca(HCO3)2与NaOH