1��ѡ���� �����й���Һ��������Ĺ�ϵ����һ����ȷ����
[? ]
A�����ʵ���Ũ����ȵİ�ˮ��NH4Cl��Һ�������ϣ�����Һ���ް����Ӵ��ڣ���
2c��H+���� c��NH4+����c��NH3��H2O����2c��OH-��
B��pH��2�������pH��12��Ba(OH)2��Һ��Ϻ�pH��7
C��ϡ��������μ��백ˮ��pH��7��c��NH4+���� c��Cl-���� c��OH-���� c��H+��
D��0��1mol/L�Ĵ����pH��a��0��01mol/L�Ĵ����pH��b����a��1��b
2��ѡ���� ����˵����ȷ����
[? ]
A��ϡ��Na2CO3��Һʱ��[c(HCO3-)��c(OH-)]/c(CO32-)����
B�������£���Ӧ4Fe(OH)2(s)+2H2O(l)+O2(g)=4Fe(OH)3(s)?��?��H<0,?��S<0 ?
C����0.1mol/LCH3COOH��Һ�ζ�0.1mol/L?NaOH������ʱ��c��CH3COO-��+?c��CH3COOH��=c��Na+�� ?
D����ˮ�м���������������ƶ���ʹˮ�ĵ���ƽ�������ƶ���ˮ�����ӻ���С
3��ѡ���� �����£������й���Һ���������ʵ���Ũ�ȹ�ϵ��ȷ���ǣ�������
A��1L?0��l?mol?L-1��NH4��2Fe��SO4��2����Һ��c��NH
��+c��Fe2+��+c��H+��=c��OH-��+c��SO��
B��0.1?mol?L-1?NH4HS��Һ�У�c��NH����c��HS-��+c��H2S��+c��S2-��
C��0.1?mol?L-1 pHΪ4��NaHA��Һ�У�c��HA-����c��H2A����c��A2-��
D����Ũ�ȵ�̼���ƺ�̼��������Һ��Ϻ����Һ�У�2c��OH-��+c��CO��=c��HCO��+3c��H2CO3��+2c��H+��
4������� ij��Һ�����±������еļ��֣�������ˮ�ĵ��뼰���ӵ�ˮ�⣩����Һ�����������ʵ���Ϊ0.2mol�����������ʵ���Ϊ0.3mol��������ֻ�����֣�
| ������ | Ba2+?NH4+?Fe3+?Al3+?Fe2+
������
OH-?CO32-?Cl-?SO32-?SO42-
|
������ԭ��Һ�м������ϡ���ᣬ���������ɣ��õ���ҺA��
������ҺA�м������ϡHNO3���ټ�AgNO3��Һ����Һ��������ɫ���������ˣ�����ҺB��
����B�м������NaOH��Һ�����ȣ���4.48L�̼�����ζ��������������������ܽ���ˮ����ˮ��Ӧ�����������Ϊ��״���µ��������ͬʱ�к��ɫ�������ɣ����ˣ�����ҺC���˹����г������������٣�
������ԭ��Һ�м���ϡHNO3���ټ�����BaCl2����46.6g��ɫ�������ɣ�
��������ʵ��ش��������⣮
��1��ԭ��Һ��һ�������ڵ���������______��
��2��д�����ܵ����ӷ���ʽ______��
��3����ԭ��Һ��һ�����ܽ���ˮ�Ƶã�����εĻ�ѧʽΪ______��
��4����ԭ��Һ��R��M��Ħ������R��M���������ܽ���ˮ�Ƶã����������εĻ�ѧʽΪ______�������ʵ���֮��Ϊ______��
����M��Һ�и�����Ũ���ɴ�С��˳��Ϊ______��
����ʵ�����ù�ҵ�����Ʊ���R���������ؽᾧ�������Ƹ���ʱ����Ҫ���ȹ��ˣ�ԭ����______��
5������� ������(��Ҫ�ɷ�ΪFeS2)�ǹ�ҵ��ȡ�������Ҫԭ�ϣ������ղ���ΪSO2��Fe3O4��
(1)��0.050 mol SO2(g)��0.030 mol O2(g)�����ݻ�Ϊ1 L���ܱ������У���Ӧ2SO2(g)��O2(g)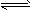 2SO3(g)��һ�������´ﵽƽ�⣬���c(SO3)��0.040 mol/L������������·�Ӧ��ƽ�ⳣ��K��SO2��ƽ��ת����(д���������)��
2SO3(g)��һ�������´ﵽƽ�⣬���c(SO3)��0.040 mol/L������������·�Ӧ��ƽ�ⳣ��K��SO2��ƽ��ת����(д���������)��
(2)��֪������Ӧ�Ƿ��ȷ�Ӧ�����÷�Ӧ����ƽ��״̬ʱ�����������������£����д�ʩ�����������
SO2ƽ��ת���ʵ���________(����ĸ)
(A)�����¶� (B)�����¶� (C)����ѹǿ (D)��Сѹǿ (E)������� (G)�Ƴ�����
(3)SO2β���ñ���Na2SO3��Һ���տɵõ���Ҫ�Ļ���ԭ�ϣ���Ӧ�Ļ�ѧ����ʽΪ_________________________________��
(4)������������ղ���Fe3O4����H2SO4�������ۣ����Ʊ�FeSO4�����ܹ������豣����Һ�㹻���ԣ���ԭ����_______________________��