1������� ij����ɫ��������A�ڿ����м���ȼ��ʱ������ɫ���棬�õ�����ɫ����B��A¶���ڿ������㹻��ʱ���ΪC��B����������D?��Ӧ������C��A��B������ˮ����E��E��DҲ������C���ش��������⣮
��1��д���������ʵĻ�ѧʽ��C______��D______��E______��
��2��д�����з�Ӧ�Ļ�ѧ����ʽ����A��ˮ����E��______��B��D����C��______��
�ο��𰸣���1������ɫ��������A�ڿ����м���ȼ��ʱ������ɫ���棬�õ�����ɫ����B����BΪNa2O2������������AΪNa��¶���ڿ������㹻��ʱ���ΪNa2CO3��
�ʴ�Ϊ��Na2CO3��CO2��NaOH��
��2����A��ˮ����E�ķ�ӦΪNa��ˮ��Ӧ������NaOH����Ӧ����ʽΪ2Na+2H2O�T2NaOH+H2����
�ʴ�Ϊ��2Na+2H2O�T2NaOH+H2����
��B��D����C�ķ�ӦΪNa2O2��CO2��Ӧ������Na2CO3����Ӧ����ʽΪ2Na2O2+2CO2�T2Na2CO3+O2��
�ʴ�Ϊ��2Na2O2+2CO2�T2Na2CO3+O2��
���������
�����Ѷȣ�һ��
2������� ��19�֣�
�й�Ԫ��X��Y��Z��W����Ϣ����
Ԫ��
| �й���Ϣ
|
X
| ��������������������������֮��Ϊ4
|
Y
| ����������Ӧ��ˮ����ܵ������������ȵ�����������
|
Z
| �����������г�������������Ʒ�ڳ�ʪ�������ױ���ʴ����
|
W
| �ؿ��к�����ߵĽ���Ԫ��
|
��ش��������⣺
��1��W�ĵ�����Y������������Ӧ��ˮ���ﷴӦ�����ӷ���ʽΪ?��
ͭƬ��̼����ZX3��Һ���ԭ��أ�д�����������ĵ缫��Ӧ����ʽ
_______________________________________________��
��2������۵⻯����Һ�еμӼ���ZX3��Ũ��Һ������Ϊ_____________________����ط�Ӧ�����ӷ���ʽΪ_______________________________��
��3������������WX3��ҺΪԭ����ȡ��ˮWX3�����Ƶ�WX3��6H2O���壬��Ҫ��������__________________________����_____________________�����¼���WX3��6H2O���壬�ܽ���4��һ����ȡ��ˮWX3����ԭ���ǣ�������ӷ���ʽ��Ҫ˵����_______________________________��
�ο��𰸣�
��1��2Al + 2OH- + 2H2O = 2AlO2- + 3H2��?��3�֣�
��2��2Fe3+ + 2e- 2Fe2+? (��Fe3+ + e-
2Fe2+? (��Fe3+ + e-  ?Fe2+)?��3�֣�
?Fe2+)?��3�֣�
��3����2�֣���Һ��Ϊ��ɫ?��2�֣�? 2Fe3+ + 2I- = 2Fe2+ + I2?��3�֣�
��4������Ũ������ȴ�ᾧ������?��3�֣�?�����HCl������2�֣�
Al3+ + 3H2O  Al(OH)3 + 3H+���ڸ����HCl�����У�����AlCl3��ˮ�⣬��
Al(OH)3 + 3H+���ڸ����HCl�����У�����AlCl3��ˮ�⣬��
����AlCl36H2O�������Ȳ�����ˮ�������ܵõ�AlCl3��?��3�֣�
�����������
�����Ѷȣ�һ��
3������� A��B��C��X��Ϊ��ѧ���������ʣ�һ�����������ǵ�ת����ϵ���£�����������ȥ����

�Իش�
��1����XΪO2����A��������?����ѡ���
a�� Si? b�� NH3? c�� Mg? d�� S
��2����A��B��C��ˮ��Һ���Լ��ԣ���ɫ��Ӧ��Ϊ��ɫ��XΪCO2�������ӷ���ʽ����B ��Һ�Լ��Ե�ԭ��?���ٳ�C��һ����;?��
��3����A��һ�ֻ���ɫ���嵥�ʣ�X��һ����ʹʪ��ĺ�ɫʯ����ֽ���������壬��Ӧ�������û���Ӧ��д����Ӧ�ٵĻ�ѧ����ʽ?��C��ˮ��Һ�и�����Ũ���ɴ�С˳��Ϊ?��
�ο��𰸣���1�� ac?��2�֣�
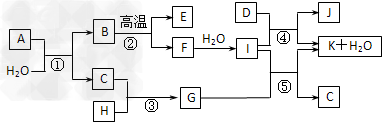
��2��CO32?+H2O  HCO3?+OH?��2�֣�?�Ʒ��ͷۻ�����θ�����Ⱥ�����?��1�֣�
HCO3?+OH?��2�֣�?�Ʒ��ͷۻ�����θ�����Ⱥ�����?��1�֣�
��3��3Cl2+2NH3=N2+6HCl?��2�֣�? c��Cl?��> c( NH4+ ) > c( H+ ) > c( OH? )?��2�֣�
�����������1��a����XΪO2��AΪSi��Si��O2��Ӧ����SiO2��SiO2��O2����Ӧ������b����AΪNH3��NH3��O2������������Ӧ����NO��NO��O2������Ӧ����NO2����ȷ��c����AΪMg��Mg��O2��Ӧ����MgO��MgO��O2����Ӧ������d����AΪS��S��O2������SO2��SO2��O2�ɼ�����Ӧ����SO3����ȷ���ʴ�Ϊac��
��2����A��B��C��ˮ��Һ���Լ��ԣ���ɫ��Ӧ��Ϊ��ɫ��XΪCO2����AΪNaOH��BΪNa2CO3��CΪNaHCO3��CO32?ˮ��ʹNa2CO3�Լ��ԣ����ӷ���ʽΪ��CO32?+H2O 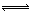 HCO3?+OH?��CΪNaHCO3�����Ʒ��ͷۻ�����θ�����ȡ�
HCO3?+OH?��CΪNaHCO3�����Ʒ��ͷۻ�����θ�����ȡ�
��3����A��һ�ֻ���ɫ���嵥�ʣ���AΪCl2��X��һ����ʹʪ��ĺ�ɫʯ����ֽ���������壬��XΪNH3����Ӧ�������û���Ӧ��Cl2��NH3��Ӧ�û���N2����ѧ����ʽΪ��3Cl2+2NH3=N2+6HCl��HCl��NH3��Ӧ���ɵ�CΪNH4Cl��NH4+ˮ�������ԣ���������Ũ���ɴ�С��˳��Ϊ��c��Cl?��> c( NH4+ ) > c( H+ ) > c( OH? )��
�����Ѷȣ�һ��
4���ƶ��� ��ͼ��ʾ����������1~20��Ԫ���в���Ԫ����ɵĵ��ʻ��仯���ͼ�в��ַ�Ӧ����δ�г�����֪C��H����ɫ�д̼�����ζ�����壬D��һ�ֻ���ɫ�����嵥�ʣ�����J������Ӿ����������Ӧ�ں͢��ǻ�����������Ҫ��Ӧ����Ӧ����ʵ�����Ʊ�����C����Ҫ������
��ش��������⣺
��1������E�ĵ���ʽ��__________��I��������ѧ������Ϊ��____________________������D����Ԫ�������ڱ��е�λ����____________________��
��2��G��ˮ��Һ��__________�ԣ������ӷ���ʽ��ʾ��ԭ��___________________________��
��3��д��E�����I��Һ��Ӧԭ���ӷ���ʽ______________________________��
��4��д��ʵ�����Ʊ�����C��Ӧ�Ļ�ѧ����ʽ______________________________����������C��ѡ��__________��������������ƣ���
��5��д����Ӧ�ܵĻ�ѧ����ʽ_________________________________��
��6����Ӧ�۵�����Ϊ______________________________��
��7����֪��7.4g?I��ϡ��Һ��200mL?1?mol/L��H��Һ��Ӧ�ų�11.56kJ��������д���÷�Ӧ���Ȼ�ѧ����ʽ________________________________________��
��8������A������Ԫ����ɣ�1?molA��ˮ��Ӧ������1?mol?B��2?mol?C��A��ѧʽΪ______________________________��
�ο��𰸣���1��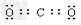 ?�����Ӽ������Լ�����������VIIA��
?�����Ӽ������Լ�����������VIIA��
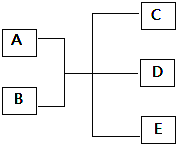
��2���NH4++H2O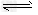 NH3��H2O+H+
NH3��H2O+H+
��3��CO2+Ca2++2OH-=CaCO3��+H2O
��4��2NH4Cl+Ca(OH)2===CaCl2+2NH3��+2H2O����ʯ��
��5��2Cl2+2Ca(OH)2===CaCl2+Ca(ClO)2+2H2O
��6����������
��7��Ca(OH)2(aq)+2HCl(aq)===CaCl2(aq)+2H2O(l) ��H=-115.6kg/mol
��8��CaCN2
���������
�����Ѷȣ�һ��
5������� ��֪A��B��C��D��E�ǻ�ѧ�г��������ʣ�����E��һ����ɫ��ζ��Һ�壬����֮�������·�Ӧ��ϵ��
��1����A��һ�ֺ�ɫ���ʣ�B��һ�ֳ������ѻӷ����ᣬC��D�������壬��д���˷�Ӧ�Ļ�ѧ����ʽ______�������Լ��п���������C��D�����������______��
�����Ը��������Һ?����ˮ?�۳���ʯ��ˮ?��Ʒ����Һ
��2����A��һ�ֺ�ɫ�����B��һ�ֳ����Ļӷ����ᣬ��Ӧʱ���ɵ�C�����壬��Ӧ�����ӷ���ʽ��______������1molCʱת�Ƶ�������______��
��3����A��һ��˫ԭ�ӷ��ӣ�B��һ����״��õ���C��D����ﻯѧʽ�ֱ���______��
��4����aA��g��+bB��g��?cC��g��+dD��s��+eE��g����Ӧ��A%���¶Ⱥ�ѹǿ�ĸı����£�
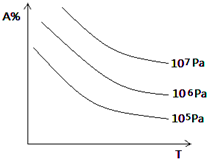
�����ж���ȷ����______��
��a+b��c+d+e?������Ӧ�����ȷ�Ӧ
�ۼ�������D��ƽ��û��Ӱ��?�������ǿʱƽ�����ƣ�ƽ�ⳣ����С��
�ο��𰸣���1����A��һ�ֺ�ɫ���ʣ�ӦΪC��B��һ�ֳ������ѻӷ����ᣬӦΪŨ���ᣬ�����ڼ��������·���������ԭ��Ӧ����CO2��SO2��H2O����Ӧ�ķ���ʽΪC+2H2SO4��Ũ��?��?.?CO2��+2SO2��+2H2O������������л�ԭ�Ժ�Ư���ԣ���ʹ���Ը��������Һ����ˮ�Լ�Ʒ����ɫ��
�ʴ�Ϊ��C+2H2SO4��Ũ��?��?.?CO2��+2SO2��+2H2O��?�٢ڢܣ�
��2����A��һ�ֺ�ɫ�����ӦΪMnO2��B��һ�ֳ����Ļӷ����ᣬӦΪ���ᣬ�����¼��������·�Ӧ����Cl2����Ӧ�����ӷ���ʽΪMnO2+4H++2Cl-?��?.?Mn2++Cl2��+2H2O��������1molCl2ʱת�Ƶ�������2NA��
�ʴ�Ϊ��MnO2+4H++2Cl-?��?.?Mn2++Cl2��+2H2O��?2NA��
��3����A��һ��˫ԭ�ӷ��ӣ�B��һ����״�ӦΪCl2��ʯ����ķ�Ӧ������CaCl2��Ca��ClO��2���ʴ�Ϊ��CaCl2��Ca��ClO��2��
��4����ͼ���жϣ������¶ȣ�A%��С��˵�������¶�ƽ��������Ӧ�����ƶ���������ӦΪ���ȷ�Ӧ������ѹǿ��A%��С��˵������ѹǿƽ��������Ӧ�����ƶ���Ӧ��a+b��c=e����ٴ�����ȷ��DΪ���壬��ƽ����Ӱ�죬����ȷ������ѹǿ�������¶Ȳ��䣬��ƽ�ⳣ�����䣬�ܴ���
�ʴ�Ϊ���ڢۣ�
���������
�����Ѷȣ�һ��