1��ѡ���� ͭƬ��пƬ�õ������Ӻ����ϡ�����У�пƬ��
[? ]
A������ ��
B������
C������ ��
D������
2��ѡ���� ijǦ�����صĹ���ԭ����ͼ��ʾ�����ܷ�ӦʽΪPb��PbO2��2H2SO4=2PbSO4��2H2O�������жϲ���ȷ����(����)
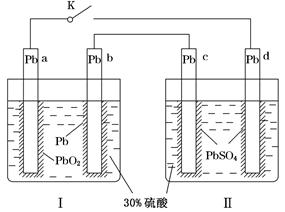
A���պ�Kʱ��d�缫�ķ�ӦʽΪPbSO4��2H2O��2e��=PbO2��4H����SO42��
B������·��ת��0.2 mol����ʱ���������ĵ�H2SO4Ϊ0.2 mol
C���պ�Kʱ������SO42����c�缫Ǩ��
D���պ�Kһ��ʱ���ɵ�����Ϊԭ��أ�d�缫Ϊ����
3������� ��10�֣�
����β���к���CO�͵����������β���ķ��������������ϰ�һ����ת�������ɷ������·�Ӧ��2NO+2CO N2+2CO2��
N2+2CO2��
��1��2NO��g��+2CO��g�� N2��g��+2CO2��g����Ӧ��ƽ�ⳣ���ı���ʽΪ��
N2��g��+2CO2��g����Ӧ��ƽ�ⳣ���ı���ʽΪ��
K=?��
��2����֪��CO��g��+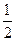 O2��g��=2CO2��g��?��H=һ283 kJ��mol
O2��g��=2CO2��g��?��H=һ283 kJ��mol
N2��g��+O2��g��="2" NO��g��?��H="+180" kJ/mol
��Ӧ2NO��g��+2CO��g�� N2��g��+2CO2��g����H=?kJ��mol��
N2��g��+2CO2��g����H=?kJ��mol��
��3�����ڿ��淴Ӧ2NO��g��+2CO��g�� N2��g��+2CO2��g������ϣ�2������Ϣ������˵����ȷ����?��
N2��g��+2CO2��g������ϣ�2������Ϣ������˵����ȷ����?��
�������¶ȣ�ƽ�ⳣ������
�������¶ȣ��淴Ӧ���ʽ���
���ڵ�λʱ��������CO��CO2�����ʵ������ʱ����Ӧ�ﵽƽ��
�ܷ�Ӧ�ﵽƽ��������������䣬��С�����ݻ���ƽ��������N2��CO2�ķ����ƶ�
��4������˵����ȷ����?
��NO��CO��CO2������������
��CO2�Ĵ����ŷŻᵼ������ЧӦ������Ӧ����ѡ�ù�����ͨ���ᳫ��̼ ����
����
������β���еĵ���������Ҫ�ǿ����еĵ����������ڸ������������ɵ�
��5��ʵ���ҿ�����NaOH��Һ����CO2����״����2.24LCO2���屻1.5 L 0.1 mol/L NaOH��Һȫ�����գ�������CO2����ˮ��������NaCO3�����ʵ���Ϊ?mol��
4������� ����ѧ--��ѧ�뼼����
��ѧ�ڲ��ϵķ�չ���������ź���Ҫ�����ã�2012��ȹ�����߿�ѧ����������֣����Ժʿ����С��Ժʿ�����˾��ڲ��Ϸ��������˾��ף�Ϊ���Ҵ�����ϴ�ľ���Ч�森
��1��ʯ��ʯ����ʯ�Һ���ʯ�Ҿ�����Ҫ�Ļ���ԭ�ϣ����й�ҵ�����У��������õ�����ԭ�ϵ���______������ţ�
��������?�����֡�?�۴Ӻ�ˮ����ȡþ��?������ұ��
����ˮ�ࡡ?���Ʋ�����?����Ư�ۡ�?�������մ�
��2�����ݰ˺����칬һ�ŵijɹ��Խ�����룬��־���ҹ����칤ҵ��չ�������½Σ�����ѡ���е������뻯ѧ�о������ص���
A��ȼ��ȼ��Ϊ���ݰ˺������ṩ����?B�������ָ��������ϵ�����ߵ�ͨѶ
C�����ʹ�õĺϳ���ά���²���?D��̫�ղ�������NiFeO4���������ķ���
��3���������ǽ�������ά�߷��Ӳ��ϸ��϶��ɵĸ��ϲ��ϣ�������ǿ�ȸߡ������ᡢ��ʴ�����������Ե���ܺõ��������ܣ����л�����______����ǿ����______��
��4�����ʯ��LiFePO4��-������ӵ���������ϣ�����FeԪ����+2�ۣ�����LiFePO4�м�����������̿�ڣ������ó��˿��Ը���LiFePO4�ĵ��������⣬����______��
5��ѡ���� Ǧ����Ч�ʵͣ���Ⱦ��Ŀǰ����п���ȡ��.п��ص�ԭ��Ϊп�������͵������Һ����ط�ӦΪ2Zn+O2=2ZnO�����й���п��ص������У���ȷ����
A��пΪ�������������븺��������Ӧ
B����������������Ӧ������������ԭ��Ӧ
C�������缫��Ӧ�ǣ�Zn �C 2e- +2OH-=ZnO+H2O
D����ع���ʱ����Һ��pH��С