1、选择题 下列溶液中粒子的物质的量浓度关系正确的是
[? ]
A.0.1 mol/L NaHCO3溶液中:c(Na+)>c(HCO3-)> c(H+)>c(OH-)
B.25℃时,pH =2的盐酸与pH= 12的氨水等体积混合后,混合液中:c(H+) =c(OH-)
C.0.1 mol/1 Na2S溶液中:c(OH-)=c(H+)+c(HS-)+c(H2S)
D.醋酸溶液与氢氧化钠溶液混合后溶液呈酸性,混合液中:c(CH3COO-)>c(Na+)
参考答案:D
本题解析:
本题难度:一般
2、选择题 常温下,将NaHY晶体加入水中溶解,得到0.1mol/L?NaHY溶液,下列叙述正确的是( )
A.若NaHY溶液的pH=4,该溶液中粒子浓度关系为:c(Na+)>c(HY-)>c(H+)>c(Y2-)>c(H2Y)
B.若NaHY的水溶液显碱性,该溶液中粒子浓度关系为:c(Na+)>c(OH-)>c(H+)>c(HY-)
C.若溶液中粒子浓度关系为c(H+)+c(H2Y)=c(OH-)+c(Y2-),则NaHY的水溶液一定显碱性
D.将NaHY晶体加入水中一定能促进水的电离
参考答案:A
本题解析:
本题难度:一般
3、简答题 (1)AgNO3的水溶液常温时的pH______7(填“>”、“=”、“<”),原因是:______(用离子方程式表示);实验室在配制AgNO3的溶液时,常将AgNO3固体先溶于较浓的硝酸中,然后再用蒸馏水稀释到所需的浓度.以______(填“促进”、“抑制”)其水解.
(2)氯化铝水溶液呈______性,原因是(用离子方程式表示):______,把AlCl3溶液蒸干,灼烧,最后得到的主要固体产物是______.
(3)在配制硫化钠溶液时,为了防止发生水解,可以加入少量的______.
参考答案:(1)AgNO3中的银离子在水中易水解,而显酸性,水解方程为:Ag++H2O?AgOH+H+,所以为了抑制其水解,配制AgNO3的溶液时,常将AgNO3固体先溶于较浓的硝酸中,然后再用蒸馏水稀释到所需的浓度,故答案为:<;Ag++H2O?AgOH+H+;抑制;
(2)氯化铝水溶液中铝离子水解显酸性,其水解方程式为:Al3++3H2O?Al(OH)3+3H+;其溶液加热促进水解,生成的HCl挥发,最后蒸干,灼烧得到Al2O3,
故答案为:酸;Al3++3H2O?Al(OH)3+3H+;Al2O3;
(3)硫化钠在溶液中水解生成NaOH,所以为了防止发生水解,可以加入少量的NaOH,故答案为:NaOH.
本题解析:
本题难度:一般
4、选择题 常温常压下,将a mol CO2气体通入1L b mol/L的NaOH 溶液中,下列对所得溶液的描述不正确的是
[? ]
A.当a=时,所得溶液中存在:c(Na+)>c(CO32-)> c(OH-)>c(HCO3-)>c(H+)
B.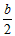 <a<b时,所得溶液中存在:c(Na+)>c(CO32-)+ c(HCO3-) +c(H2CO3)
<a<b时,所得溶液中存在:c(Na+)>c(CO32-)+ c(HCO3-) +c(H2CO3)
C.当a=b时,所得溶液中存在:c(OH-)+c(CO32-)= c(H+) +c(H2CO3)
D.当a=b时,所得溶液中存在:c(Na+)>c(CO32-)> c(HCO3-)>c(OH-)>c(H+)
参考答案:D
本题解析:
本题难度:一般
5、简答题 25℃时,如果取0.1mol?L-1HA溶液与0.1mol?L-1NaOH溶液等体积混合(混合后溶液体积的变化不计),测得混合溶液的pH=8,试回答以下问题:
(1)混合溶液的pH=8的原因(用离子方程式表示):______;
(2)混合溶液中由水电离出的c(H+)______(填“<”“>”“=”)0.1mol?L-1?NaOH溶液中由水电离出的c(H+);
(3)求出混合液中下列算式的精确计算结果:c(Na+)-c(A-)=______mol?L-1;
(4)已知NH4A溶液为中性,又知将HA溶液加到Na2CO3溶液中有气体放出,试推断(NH4)2CO3溶液的pH______7?(填“<”“>”“=”);
(5)将相同温度下相同浓度的五种溶液:①(NH4)2CO3;②NH3?H2O;③(NH4)2SO4;④NH4Cl;⑤CH3COONH4 按c(NH4+)由大到小的顺序排列______填序号).
参考答案:(1)等物质的量的一元酸和一元碱恰好反应生成盐和水,生成的盐溶液呈碱性说明该酸是弱酸,生成的盐能水解导致溶液中氢氧根离子浓度大于氢离子浓度,溶液的pH值大于7,水解方程式为:A-+H2O=HA+OH-,
故答案为:A-+H2O?HA+OH-;
(2)该盐含有弱根离子能促进水电离,氢氧化钠是强碱能抑制水电离,所以混合溶液中由水电离出的c(H+)>0.1mol?L-1NaOH溶液中由水电离出的c(H+),
故答案为:>;
(3)溶液中存在电荷守恒,即:c?(Na+)+c(H+)=c(A-)+c(OH-),
则c?(Na+)-c(A-)=c(OH-)-c(H+)=10-6mol/L-10-8mol/L=9.9×10-7mol/L,
故答案为:9.9×10-7;
(4)将HA溶液加到Na2CO3溶液中有气体放出,说明HA的酸性比碳酸的强,NH4A溶液为中性,说明相同条件下,氨水和HA的电离程度相同,所以(NH4)2CO3中铵根离子的水解程度小于碳酸根离子的水解程度,所以溶液的pH>7,
故答案为:>;
(5)①③④⑤相比,由于①⑤中NH4+水解得到促进,水解程度大于③④,且①>⑤中c(NH4+);
③中(NH4)2SO4物质的量浓度与④相比,当二者浓度相等时,③中c(NH4+)接近④的2倍,
NH3?H2O,溶液中c(NH4+)小于铵盐的c(NH4+),应最小,由于水解程度一般较小,则①>④,
按c(NH4+)由大到小的顺序排列为③①④⑤②.
故答案为:③①④⑤②.
本题解析:
本题难度:一般