1、实验题 (12分)NO很容易与许多分子迅速发生反应,科学家发现在生物体中不断地产生NO,用于在细胞和细胞间传递信息;NO还参与心血管系统、免疫系统以及中枢和外围神经系统的调控。
(1)实验室用金属铜和稀硝酸制取NO的离子方程式为
________________________________________________________________。
(2)NO是有毒气体,某学生为防止污染,用分液漏斗和烧杯装配了一套简易的、能随开随用、随关随停的NO气体发生装置,如图甲所示。
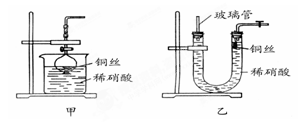
打开分液漏斗的活塞使反应进行,在分液漏斗中实际看到的气体是红棕色的,原因是_________________________________(写化学方程式)。
(3)为证明铜丝与稀硝酸反应生成的确实是NO,某学生另设计了一套如图乙所示的装置制取NO。反应开始时,可以在U形管右端观察到无色的NO气体。长玻璃管的作用是_______________________________________。
(4)假设实验中12.8 g Cu全部溶解,需要通入标准状况下________L O2才能使NO全部溶于水。
(5)用金属铜制取硝酸铜,从节约原料和防止环境污染的角度考虑,下列4种方法中最好的是________(填“甲”“乙”“丙”或“丁”),理由是__________________________________。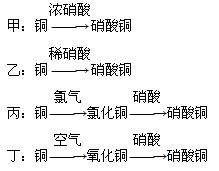
参考答案:(1)3Cu+8H++2NO3-=3Cu2++4H2O+2NO↑?(2)2NO+O2=2NO2
(3)接收被气体压出U形管的液体,防止稀硝酸溢出?(4)2.24L
(5)?丁?制取相同质量的Cu(NO3)2,丁所消耗的HNO3的量最少(原料的利用率最高)且不产生污染环境的气体? (每空2分,共12分)
本题解析:(1)硝酸是氧化性酸,和铜反应的方程式为3Cu+8H++2NO3-=3Cu2++4H2O+2NO↑。
(2)NO极易被氧气氧化生成红棕色的NO2,方程式为2NO+O2=2NO2。
(3)由于反应中生成的NO难溶于水,导致压强增大,所以长玻璃导管的作用是接收被气体压出U形管的液体,防止稀硝酸溢出。
(4)12.8g铜是0.2mol,失去电子是0.4mol;由于最终NO又生成硝酸,说明铜失去的电子被氧气得到,根据电子的得失守恒可知,氧气的物质的量是0.1mol,标准状况下的体积是2.24L。
(5)甲乙中均产生大气污染物,丙中原子利用率不高,且氯气有毒,所以正确的答案选丁。
本题难度:一般
2、填空题 (9分)氮及其化合物与人们的生活息息相关。
(1)氮元素在周期表中的位置是?。
(2)实验室可用铜与稀硝酸反应制取NO,其离子方程式是?。为防止环境污染,可用碱液吸收氮的氧化物。NO与NO2按物质的量之比1:1被NaOH溶液完全吸收后得到一种钠盐,该化学方程式是?。
(3)已知:① CH4(g) + 4 NO2(g) =" 4" NO(g) + CO2(g) +2 H2O(g)?△H= -574 kJ・mol-1
② CH4(g) + 4 NO(g) =" 2" N2(g) + CO2(g) + 2 H2O(g)?△H= -1160 kJ・mol-1
根据①和②,标准状况下,4.48 L CH4恰好将NO2转化为N2时,△H=?。
由反应①可推知:CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(l)?△H?-574 kJ・mol-1
(4)同温同压下,3.5 L NH3恰好将3.0 L NO和NO2的混合气完全转化为N2,则原混合
气中 NO和NO2的体积比是 。
(5)含有1mol HNO3的稀硝酸分别与不同质量的铁粉,所得氧化产物a、b与铁粉物质的量关系如下图所示。? b是?n3 =?p=?
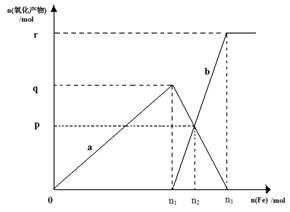
参考答案:(9分,每空1分)
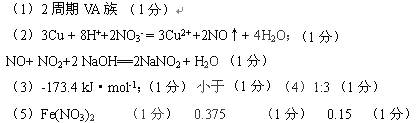
本题解析:略
本题难度:一般
3、选择题
Au+HNO3+3HCl===AuCl3+NO↑+2H2O
玻尔走后,纳粹分子窜进他的实验室,那瓶溶有金质奖章的溶液就在纳粹眼皮底下,纳粹分子却一无所知,多么高明的隐藏奖章的方法啊!德军战败后,玻尔回到自己的实验室,他从溶液中提取出金,重新铸成了诺贝尔奖章,新奖章显得更加光彩夺目。则下面所列方法中,你认为不能从溶有黄金的王水中提取出金的是________。
A.用铁置换
B.电解其水溶液
C.先蒸发水分后灼烧固体
D.渗析或过滤
参考答案:D
本题解析:题给反应是一很重要的信息,它告诉我们黄金溶于过量的王水中,得到了HNO3、HCl和AuCl3的混合溶液。
A.用铁置换是可以的:3Fe+2AuCl3====3FeCl2+2Au
B.电解其水溶液也是可以的:阳极:2Cl--2e-====Cl2↑阴极:Au3++3e-====Au
C.先蒸发水分再灼烧固体也是可以的。水分蒸发后得AuCl3固体(酸性条件下蒸发,可不考虑AuCl3的水解),由2AgCl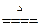 2Ag+Cl2↑,而Au不如银活泼推知,2AuCl3
2Ag+Cl2↑,而Au不如银活泼推知,2AuCl3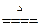 2Au+3Cl2↑。AuCl3(aq)蒸发水解加剧,可得Au(OH)3、Au2O3固体、灼烧Au(OH)3变为Au2O3,Au2O3变为Au和O2,前面我们可由AlCl3溶液蒸干而推知,后者我们可由HgO受热分解而推知。
2Au+3Cl2↑。AuCl3(aq)蒸发水解加剧,可得Au(OH)3、Au2O3固体、灼烧Au(OH)3变为Au2O3,Au2O3变为Au和O2,前面我们可由AlCl3溶液蒸干而推知,后者我们可由HgO受热分解而推知。
D.渗析和过滤都无法将其分开
本题难度:一般
4、计算题 (8分)铜能与稀硝酸反应,反应方程式为:
3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O,当有9.6克Cu参加反应时,
求:
(1)产生气体在标准状况下的体积
(2)被还原的硝酸的质量
参考答案:(1)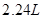 (2)6.3g
(2)6.3g
本题解析:考查根据方程式进行的有关计算。稀硝酸具有氢氧化性,能氧化铜生成硝酸铜、NO和水,这说明硝酸没有被完全还原,据此可以进行有关计算。
9.6g铜是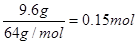 ,铜和稀硝酸反应的发生为
,铜和稀硝酸反应的发生为
3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O
3mol? 8mol? 2×22.4L
0.15ml n(HNO3)? V(NO)
(1)所以产生气体在标准状况下的体积为V(NO)=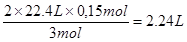
(2)参加反应的硝酸是n(HNO3)=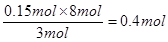
根据方程式可知被还原的硝酸是参加反应的硝酸的1/4
所以被还原的硝酸的物质的量是1/4×0.4mol=0.1mol
其质量是0.1mol×63g/mol=6.3g
本题难度:一般
5、计算题 取5.64gCu(NO3)2无水晶体,强热使其分解,得到NO2、O2和2.32固体氧化物。将气体用水充分吸收后,还有气体剩余,同时得到100mL溶液。请通过计算确定:(写出计算过程)
(1)所得溶液的物质的量浓度;
(2)残留固体的成分和质量分别是多少克?
参考答案:(1)0.6mol/L
(2)Cu2O为0.72g(2分),CuO为1.60g
本题解析:假设固体氧化物全部为CuO,则:2Cu(NO3)2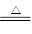 2CuO+4NO2↑+O2↑
2CuO+4NO2↑+O2↑
另外气体被水吸收的方程式为:4NO2+O2+2H2O=4HNO3
可看出,气体将被水全部吸收,且5.64gCu(NO3)2无水晶体( )生成的CuO为0.03×80=2.4g,故固体氧化物中除CuO外,还有Cu2O:4CuO
)生成的CuO为0.03×80=2.4g,故固体氧化物中除CuO外,还有Cu2O:4CuO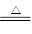 2Cu2O+O2↑
2Cu2O+O2↑
(1)从以上分析可看出,剩余气体为氧气,故N元素全部转化为硝酸,所得溶液的浓度为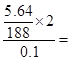 0.6mol/L
0.6mol/L
(2)设固体氧化物中CuO、Cu2O的物质的量分别为x、y
则80x+144y=2.32
再由铜的守恒可知:x+2y=0.03
得:x=0.02mol? y=0.005mol
故CuO、Cu2O的质量分别为1.60g、0.72g
本题难度:简单