1、简答题 设在某温度时,在容积为1L的密闭容器内,把氮气和氢气两种气体混合,反应后生成氨气.实验测得,当达到平衡时,测得氮气和氢气的浓度各为2mol/L,该温度下的平衡常数为0.5625则
(1)平衡时氨气的浓度为______
(2)求起始加入氮气的浓度
(3)反应前混合气体的平均分子量.
参考答案:达到平衡时,测得氮气和氢气的浓度各为2mol/L,该温度下的平衡常数为0.5625,
(1)根据平衡常数表达式k=c2(NH3)c(N2)?c3(H2)可知,c2(NH3)2×2=0.5625,解得c(NH3)=1.5mol/L,
故答案为:1.5mol/L;
(2)根据N2+3H2?2NH3,可知氮气的浓度变化量为1.5mol/L×12=0.75mol/L,故氮气的起始浓度为2mol/L+0.75mol/L=2.75mol/L,
答:氮气的起始浓度为2.75mol/L.
(3)根据N2+3H2?2NH3,可知氢气的浓度变化量为1.5mol/L×32=2.25mol/L,故氮气的起始浓度为2mol/L+2.25mol/L=4.25mol/L,
故反应前混合气体中氮气与氢气的物质的量之比为2.75mol/L:4.25mol/L=11:17,故反应前混合气体的平均相对分子质量为11×14+17×211+17=6.7,
答:反应前混合气体的平均相对分子质量为6.7.
本题解析:
本题难度:一般
2、选择题 下列有关化学方应方向的说法中正确的是
A.凡是焓变小于零的反应都能自发进行
B.凡是熵变小于零的化学反应都能自发进行
C.凡是焓变小于零,熵变大于零的化学变化都能自发进行
D.CaCO3在高温下的分解反应不属于自发过程
参考答案:C
本题解析:考查反应的自发性和化学反应进行的方向。一般情况下放热反应容易自发,熵值增加的反应容易自发,但不是绝对的。根据△G=△H-T・△S可知,当△H<0、△S>0时反应一定是自发的。答案是C。
本题难度:简单
3、选择题 氯化铜在水溶液中存在有如下平衡:
〔Cu(H2O)4〕2+(蓝色)+4Clˉ 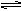 ?〔CuCl4〕2ˉ(绿色)+4H2O 下列操作可以使溶液变蓝色的是:
?〔CuCl4〕2ˉ(绿色)+4H2O 下列操作可以使溶液变蓝色的是:
A.向溶液中加入少量NaCl晶体
B.向溶液中滴加少量浓盐酸
C.向溶液中滴加少量AgNO3溶液
D.加水将溶液稀释
参考答案:CD
本题解析:略
本题难度:一般
4、填空题 (10分)甲醇(CH3OH)的用途广泛,摩托罗拉公司也开发出一种由甲醇、氧气以及强碱做电解质溶液的新型手机电池,容量达氢镍电池或锂电池的10倍,可连续使用一个月才充一次电.请完成下列与甲醇有关的问题.
(1)工业上用3克氢气与二氧化碳反应生成气态甲醇和水蒸气,放出24.5千焦的热量。
①请写出该反应的热化学反应方程式:?利用该反应,在温度和容积相同的A、B两个容器中,按不同方式投入反应物,保持恒温恒容,经10秒钟后达到平衡,达到平衡时的有关数据如下表:?
②从反应开始到达到平衡时,A中用CO2来表示的平均反应速率为?。
③A中达到平衡时CO2的转化率为?, B中a=?。
(2)某同学设计了一个甲醇燃料电池,其装置如图:
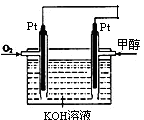
①写出图中通入甲醇这一极的电极反应式?。
②反应一段时间后,正极附近的碱性?(增强。减弱?不变)
参考答案:(1)①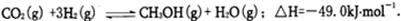 ? (2分)
? (2分)
② 0.1c1 mol/(L・s) 或0.1c2 mol/(L・S)(任答对一个得分)(1分)
③ 60%? (2分)?19.6(2分)
(2)① CH3OH - 6e-+ 8OH- = CO32-+ 6H2O? (2分)?② 增强(1分)
本题解析:(1)①考查热化学方程式的书写②甲醇的浓度变化未c1,则根据方程式可知,CO2的浓度变化也是c1,所以反应速率为0.1c1 mol/(L・s)。放出的热量是29.4kJ,所以消耗的CO2是 ,所以转化率是60%。根据反应物投入量可知A和B是等效的,所以B中吸收的热量是49kJ-29.4kJ=19.6kJ。
,所以转化率是60%。根据反应物投入量可知A和B是等效的,所以B中吸收的热量是49kJ-29.4kJ=19.6kJ。
(3)甲醇失去电子,发生氧化反应,在负极通入。氧气在正极通入,得到电子发生还原反应,生成OH-,所以正极周围碱性增强。
本题难度:一般
5、选择题 在密闭容器里,A与B反应生成C,其反应速率分别用 表示,已知
表示,已知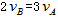 、
、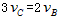 ,则此反应可表示为
,则此反应可表示为
[? ]
A.2A+3B = 2C
B.A+3B = 2C
C.3A+B = 2C
D.A+ B = C
参考答案:A
本题解析:
本题难度:简单