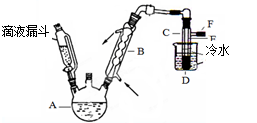
1、实验题 下图是实验室用乙醇与浓硫酸和溴化钠反应来制备溴乙烷的装置,反应需要加热,图中省去了加热装置。有关数据见表3:
?
| 乙醇
| 溴乙烷
| 溴
|
状态
| 无色
液体
| 无色
液体
| 深红棕色
液体
|
密度/g・cm-3
| 0.79
| 1.44
| 3.1
|
沸点/℃
| 78.5
| 38.4
| 59
|
?
表3.乙醇、溴乙烷、溴有关参数
(1)制备操作中,加入的浓硫酸必需进行稀释,其目的是?(选填序号)。
a.减少副产物烯和醚的生成? b.减少Br2的生成
c.减少HBr的挥发?d.水是反应的催化剂
(2)写出溴化氢与浓硫酸加热时发生反应的化学方程式?。
(3)图中试管C中的导管E的末端须在水面以下,其原因是?。
(4)加热的目的是?。
(5)为除去产品中的一种主要杂质,最好选择下列?(选填序号)溶液来洗涤产品。
A.氢氧化钠? B.碘化亚铁? C.亚硫酸钠? D.碳酸氢钠
(6)第(5)步的实验所需要的玻璃仪器有?。
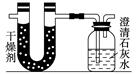
2、实验题 已知某醇燃料含有碳、氢、氧三种元素。为了测定这种燃料中碳和氢两种元素的质量比,可将气态燃料放入足量的氧气中燃烧,并使产生的气体全部通入如图所示的装置,得到如下表所列的实验结果(假设产生的气体完全被吸收):
?
| 实验前
| 实验后
|
(干燥剂+U形管)的质量
| 101.1 g
| 102.9 g
|
(石灰水+广口瓶)的质量
| 312.0 g
| 314.2 g
|
?
根据实验数据求:
(1)实验完毕后,生成物中水的质量为________ g,
假设广口瓶里生成一种正盐,其质量为________ g;
(2)生成的水中氢元素的质量为________ g;
(3)生成的二氧化碳中碳元素的质量为________ g;
(4)该燃料中碳元素与氢元素的质量比为________;
(5)已知这种醇的每个分子中含有一个氧原子,则该醇的分子式为__________,结构简式为_______________________________。
3、推断题 由碳、氢、氧三种元素组成的某有机物,分子中共含有10个原子,其原子
核外共有32个电子,lmol该有机物在氧气中完全燃烧时需要4molO2,回答:
(1)求该有机物的分子式。
(2)若该有机物可使溴水褪色,但不发生银镜反应,取2mol该有机物与足量钠反应,
能产生22.4L H2(标准状况),则该有机物的结构简式可能是什么?
(3)若该有机物能发生银镜反应,则其结构简式是什么? 并写出该有机物发生银镜反应的化学方程式。
4、选择题 在20℃时,某气态烃与O2的混合气在密闭的容器中点燃爆炸后又恢复到20℃,此时容器内气体的压强变为反应前的一半,再经NaOH溶液吸收后,容器内几乎成真空,此烃的分子式可能是
A.C3H6
B.C2H2
C.C2H6
D.C3H8
5、计算题 在某一温度下,将20 g乙炔溶于40 g苯(C6H6)中,所得混合溶液中氢元素的质量分数是(? )
A.7.7%
B.7.9%
C.15.4%
D.15.8%