|
高考化学知识点总结《物质组成与性质实验方案的设计》在线测试(2017年最新版)(十)
2018-03-17 07:56:39
来源:91考试网
作者:www.91exam.org 【 大 中 小】
|
1、实验题 (15分)某化学兴趣小组拟采用下图装置甲电解饱和氯化钠溶液,并用电解产生的H2还原CuO粉末来测定Cu的相对原子质量Ar(Cu),同时检验氯气的氧化性,图中夹持和加热仪器已略去。
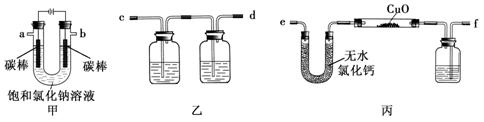
(1)写出装置甲中反应的离子方程式:?。
(2)为完成上述实验,正确的连接顺序为a连?,b连?(填写连接的字母)。
(3)装置乙中第一个广口瓶内的溶液不能是(?)
A.淀粉碘化钾溶液
B.NaOH溶液
C.FeCl2与KSCN混合溶液
D.Na2SO3溶液
| (4)在 对硬质玻璃管里的氧化铜粉末加热前,需进行的操作为?。 对硬质玻璃管里的氧化铜粉末加热前,需进行的操作为?。
(5)装置丙中广口瓶内盛放的试剂为?,作用是??。
(6)为了测定Cu的相对原子质量,某同学通过实验测得丙装置反应前后如下数据:样品质量为m1g、反应后硬质玻璃管中剩余固体质量为m2g、反应前后U型管及其中固体质量差为m3g、反应前后洗气瓶及其中液体质量差为m4g。
①请选择理论上误差最小的一组数据计算Ar(Cu),Ar(Cu)=?。
②如果选用其他组数据进行计算,会导致Ar(Cu)?(填“偏大”、“偏小”或“不受影响”),理由是?。
参考答案:(15分)
(1)2Clˉ+2H2O 2OHˉ +H2↑+Cl2↑(2分) 2OHˉ +H2↑+Cl2↑(2分)
(2)f? c(各1分,共2分)
(3)BD(2分)
(4)检验氢气的纯度,防止发生爆炸(2分)
(5)浓硫酸?干燥H2,防止硬质玻璃管炸裂(各1分, 共2分) 共2分)
(6)①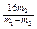 (2分) (2分)
②偏小(1分)
空气中的H2O通过e导管口进入U型管造成m3偏大(2分)
本题解析:略
本题难度:简单
2、选择题 下列实验不能作为判断依据的是(?)
A.钠和镁分别与冷水反应,判断钠和镁金属性强弱
B.在MgCl2与AlCl3溶液中分别加入过量的氨水,判断镁与铝的金属性强弱
C.硅酸钠溶液中通入CO2产生白色沉淀,判断碳酸与硅酸的酸性强弱
D.Br2与I2分别与足量的H2反应,判断溴与碘的非金属性强弱
参考答案:B
本题解析:略
本题难度:简单
3、实验题 某化学课外小组用下图装置制取溴苯并探究该反应的类型。先向分液漏斗中加入苯和液溴,再将混合液滴入反应器A(A下端活塞关闭)中。
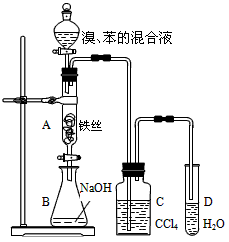
(1)写出A中反应的化学方程式:______________________________________。
(2)实验结束时,打开A下端的活塞,让反应液流入B中,充分振荡,目的是______________________。 (3)C中盛放CCl4的作用是______________________________。
(4)若要证明苯和液溴发生的是取代反应,而不是加成反应,通常有两种方法,请按要求填写下表。

参考答案:(1)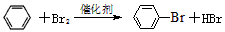
(2)除去溶于溴苯中的溴
(3)除去溴化氢气体中的溴蒸气
(4)方法一:AgNO3溶液;产生(淡黄色)沉淀
方法二:石蕊试液;溶液变红色(或其他合理答案)
本题解析:
本题难度:一般
4、实验题 某化学小组拟采用如下装置(夹持和加热仪器已略去)来电解饱和食盐水,并用电解产生的H2还原CuO粉末来测定Cu的相对原子质量,同时检验氯气的氧化性。
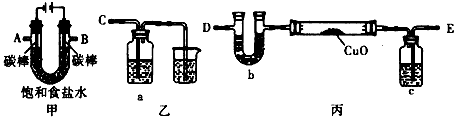
(1)为完成上述实验,正确的连接顺序为A连____;B 连____(填写连接的字母)。
(2)对硬质玻璃管里的氧化铜粉末加热前,需要进行的操作为___________________。
(3)若检验氯气的氧化性,则乙装置的a瓶中溶液可以是____________,对应的现象为_____________。
(4)丙装置的c瓶中盛放的试剂为____________,作用是_______________。
(5)精确测量硬质玻璃管的质量为ag,放入CuO后,精确测量硬质玻璃管和CuO的总质量为bg,实验完毕后,为测定Cu的相对原子质量,设计了如下甲、乙两个实验方案。
甲方案:通过精确测量硬质玻璃管和Cu粉的总质量(cg),进而确定Cu的相对原子质量。
乙方案:通过精确测定生成水的质量(dg),进而确定Cu的相对原子质量。
①请你分析并回答:_____方案测得的结果更准确。你认为不合理的方案的不足之处是____________。
②按测得结果更准确的方案进行计算,Cu的相对原子质量为__________。
参考答案:(1)E;C
(2)检验氢气的纯度
(3)淀粉KI溶液;溶液变为蓝色
(4)浓硫酸;吸收H2中的H2O
(5)①甲;空气中的CO2和H2O会通过D进入U形管而造成较大的实验误差
②16(c-a)/(b-c)
本题解析:
本题难度:一般
5、实验题 某同学利用下图所示的实验装置进行铁跟水蒸气反应的实验,并继续研究铁及其化合物的部分性质。
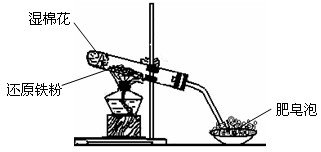
请回答下列问题。
(1)硬质试管中发生反应的化学方程式为___________________________________。
(2)该同学欲确定反应后硬质试管中固体物质的成分,设计了如下实验方案:
①待硬质试管冷却后,取少许其中的固体物质溶于稀硫酸得溶液B;
②取少量溶液B滴加KSCN溶液,若溶液变红色则说明硬质试管中固体物质的成分是_____________,若溶液未变红色则说明硬质试管中固体物质的成分是_____________。
(3)该同学按上述实验方案进行了实验,结果溶液未变红色,原因是________________________(用离子方程式表示)。
(4)该同学马上另取少量溶液B,使其跟NaOH溶液反应。若按下图所示的操作,可观察到生成白色沉淀,迅速变成灰绿色,最后变成红褐色的现象,请写出与上述现象相关的反应的化学方程式__________________________。
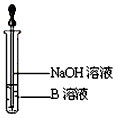
(5)一段时间后,该同学发现(3)中未变红的溶液变成红色,说明Fe2+具有________性。由此可知,实验室中含Fe2+的盐溶液现用现配制的原因是_____________,并且配制含Fe2+的盐溶液时应加入少量
________________________。
参考答案:(1)3Fe+4H2O(g) Fe3O4+4H2 Fe3O4+4H2
(2)一定有Fe3O4,可能有Fe;Fe3O4和Fe
(3)Fe+2Fe3+=3Fe2+
(4)FeSO4+2NaOH=Fe(OH)2↓+ Na2SO4、4Fe(OH)2+O2+2H2O=4Fe(OH)3
(5)还原;Fe2+易被空气中的氧气氧化而变质;铁粉
本题解析:
本题难度:一般
|  对硬质玻璃管里的氧化铜粉末加热前,需进行的操作为?。
对硬质玻璃管里的氧化铜粉末加热前,需进行的操作为?。