1��ʵ���� ����ʵ�����ṩ�������Լ����������ԭ����ͬ�ļ�ʵ�飨ֻҪд������ʵ�鷽�����ɣ���֤��þԪ�صĽ����Ա���ǿ���Լ���Mg����Al˿��AlCl3��Һ��MgCl2��Һ��ϡHCl��NaOH��Һ
ʵ�鷽������__________________��
ʵ�鷽������__________________��
2������� �{����������a-Fe2O3�����ִ����ӹ�ҵ��Ҫ���ϣ�ʵ������������������Fe2O3��FeO��SiO2�ȣ�Ϊԭ���Ʊ��{���������IJ�����ͼ��ʾ����ش��й����⣺
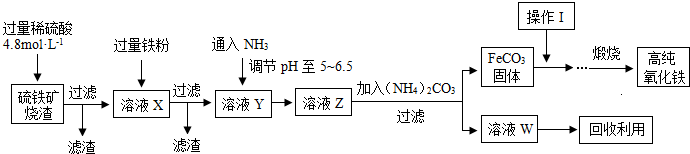
��1�����˲����еIJ�������Ϊ______��
��2��ʵ������240mL4.8mol?L-1��������Һ������18.4mol?L-1��Ũ����������ƣ�����Ҫ������Ҫ����Ϊ______��
��3����ҺX������Ӧ�����ӷ���ʽΪ______��
��4��������μ�����ҺZ�е�������______��
��5������I��������______���о�W��һ����;______��
��6��ijʵ��С����Ƶİ����Ʊ�ʵ������Ϊ������װ�á��������ռ���β��������ѡ����ʵ�������������������������ͼ��ʾ��д��ĸ��ʾ��______��
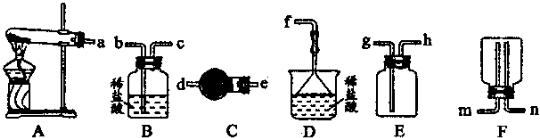
��7��������İ���ͨ��ˮ�У����õ�25��0.2mol?L-1��NH3?H2O��Һ�����ṩ0.1 mol?L-1������Һ���������ʵ�飬֤��NH3?H2O�ĵ���̶ȴ���NH4Cl��ˮ��̶ȣ�����ʵ�鷽��������______��
3��ʵ���� ij��ѧ��ȤС���ͬѧΪ̽����������Ļ�ѧ���ʣ����������ͼ��ʾ��װ�á�

��ش��������⡣
��1��ͭ��Ũ���ᷴӦ�Ļ�ѧ����ʽΪ____________________��
��2��Bƿ��ʢ��Ʒ����Һ���۲쵽Ʒ����Һ��ɫ��������ΪSO2����___________����ѡ�����ĸ����ͬ����Cƿ��ʢ�����Ƶ���ˮ���۲쵽��ˮ��ɫ��������ΪSO2����___________��
A�������� B����ԭ�� C��Ư����
��3��Dƿ��ʢ��NaOH��Һ��������___________���÷�Ӧ�����ӷ���ʽΪ______________________��
��4����ַ�Ӧ��С��ͬѧ����ͭ�����ᶼ��ʣ�ࡣ����ʹʣ���ͭƬ�ܽ⣬���ټ���__________����ѡ�����ĸ����
A��HNO3 B��NaNO3 C��NaHCO3 D��Na2CO3
4��ʵ���� �ڳ����£�Fe��ˮ������Ӧ�����ڸ����£����ȵ�������ˮ������Ӧ�����������ɣ�������ͼ��ʾװ�ý������ڸ�������ˮ������Ӧ��ʵ�飬���üķ����ռ����������ɵ���������ش���������
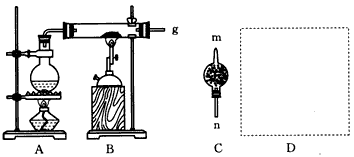
(1)д�����ڸ�������ˮ������Ӧ�Ļ�ѧ����ʽ��________________________��
(2)�����C��ʢ�ŵ�ҩƷ��____��____������ܵ�____���m����n��������g���������ӡ�
(3)��D�������ü��������Թܣ����ռ�������װ��ͼ���������������Լ�ѡ��
(4)Բ����ƿ��ʢװ����ˮ����װ�����Ⱥ����Ҫ������_________________��
(5)�����üķ��������ռ���������������������ʵ��������������________________��
5������� ij����С����MnO2��Ũ�����Ʊ�Cl2ʱ�����ø����չ�����SO2��NaOH��Һ����β���������մ�����
��1�������SO2��������NaOH��Һ��Ӧ�Ļ�ѧ����ʽ��?��2�֣�
��2����ӦCl2+Na2SO3+2NaOH===2NaCl+Na2SO4+H2O��ÿת��2.5mol�ĵ�����μӷ�Ӧ�Ļ�ԭ�������ʵ���Ϊ?mol����2�֣�
��3������β��һ��ʱ�������Һ��ǿ���ԣ��п϶�����Cl ��OH
��OH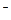 ��SO
��SO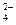 �������ʵ�飬̽��������Һ�п��ܴ��ڵ����������ӣ������ǿ�����CO2��Ӱ�죩��
�������ʵ�飬̽��������Һ�п��ܴ��ڵ����������ӣ������ǿ�����CO2��Ӱ�죩��
������������� ��
����1��ֻ����SO32-��?����2��ֻ����ClO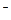
����3���Ȳ�����SO32-Ҳ������ClO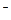 ��
��
����4��?����2�֣�
�����ʵ�鷽������ʵ�顣���ڴ����д��ʵ�鲽���Լ�Ԥ������ͽ���
��ѡʵ���Լ���3moL L-1H2SO4��0.01mol
L-1H2SO4��0.01mol L-1KMnO4����ɫʯ����Һ����ÿ��2�֣�
L-1KMnO4����ɫʯ����Һ����ÿ��2�֣�
ʵ�鲽��
| Ԥ������ͽ���
|
����1��ȡ��������Һ���Թ��У��μ�3 moL L-1 H2SO4����Һ�����ԣ�Ȼ��������Һ������A��B�Թ��У� L-1 H2SO4����Һ�����ԣ�Ȼ��������Һ������A��B�Թ��У�
| ?
|
����2��
| ?
|
����3��
| ?
|
?