1��ʵ���� ��֪�����������ȵ�����ͭ��Ӧ�õ������ͽ���ͭ����ʾ��ͼ�е�װ�ÿ���ʵ�ָ÷�Ӧ��
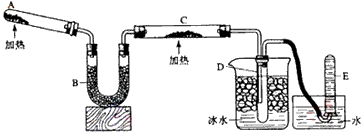
�ش��������⣺
��1��A�м����������_________��������Ӧ�Ļ�ѧ����ʽ��__________________��
��2��B����������_________����������__________________��
��3��ʵ��ʱ��C�й۲쵽��������_________________��������Ӧ�Ļ�ѧ����ʽ��_______________��
��4��ʵ��ʱ��D�й۲쵽��������__________________��D���ռ�����������_________����������ʵķ�����������__________________��
�ο��𰸣���1������NH4Cl��Ca(OH)2��2NH4Cl��Ca(OH)2 CaCl2��2NH3����2H2O
CaCl2��2NH3����2H2O
��2����ʯ�ң���CaO������ȥNH3�����е�ˮ��
��3����ɫ��ĩ������Ϊ��ɫ��2NH3��3CuO N2��3H2O��3Cu
N2��3H2O��3Cu
��4��������ɫҺ�壻��ˮ���ú�ɫʯ����ֽ���顢��ֽ����������ˮ����ͭ���顢��ˮ����ͭ����
���������
�����Ѷȣ�һ��
2������� ��12�֣�ij��ѧ�о���ѧϰС��Ϊ̽��ijƷ�ƻ������в�����֬����ĺ���������������ʵ�飺

�����ȡ0.4g��������Ʒ��������������ĵ�ƿ����ͼ���ڣ�����10mL���Ȼ�̼������ҡ��ʹ��ȫ���ܽ⡣���ƿ�м���25.00mL��0.01mol IBr����ˮ������Һ���Ǻ�ƿ�����ڲ�������ƿ��֮��μ�����10%�⻯����Һ��շ�϶������IBr�Ļӷ���ʧ��
������ڰ�������30min������ʱ����ҡ����30min��С�ĵش��������������Ƶ�10%�⻯��10mL������ˮ50mL�Ѳ�������ƿ���ϵ�Һ���ϴ��ƿ�ڡ�
�������ָʾ������0.1mol��L��1�����������Һ�ζ���������ƿ��ֱ���յ㡣
�ⶨ�����з�������ط�Ӧ���£�
��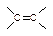 ��IBr ��
��IBr ��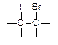
��IBr��KI��I2��KBr
��I2��2S2O32����2I����S4O62��
��ش��������⣺
����֪±�ػ�����IBr��������±�ص������ƣ�ʵ����ȷ��ȡIBr��ҺӦ��?��?���÷���ʽ��ʾ��ƿ��������ԭ��?��?��
�Ʋ�����е�ƿ�ڰ�������30min������ʱ����ҡ����ԭ����?��?��
�Dz����������ָʾ��Ϊ?��?���ζ��յ������?��?��
�ȷ�Ӧ�������Һ�������л������Ȼ�̼�������������?��?��
�ο��𰸣�����ʽ�ζ��ܣ�����Һ�ܣ�? IBr��H2O��HIO��HBr
�Ƶ�ƿ���ڰ������Լ���IBr�Ļӷ�������ҡ�����������ʼ��ַ�Ӧ��
�ǵ�����Һ?��Һ����ɫǡ�ñ�Ϊ��ɫ
�ȷ�Һ������
�����������
�����Ѷȣ�һ��
3��ʵ���� ij����С���ͬѧ��ʵ������п��Ũ���ᷴӦ��ʵ��ʱ����ͬѧ��Ϊ�����������Ƕ���������ͬѧ��Ϊ���������������⣬�����ܲ���������Ϊ����֤�ס�����ͬѧ���ж��Ƿ���ȷ����ͬѧ�������ͼ��ʾ��ʵ��װ��(п��Ũ���Ṳ��ʱ����������ΪX���Ҹ÷�Ӧװ������ȥ)��
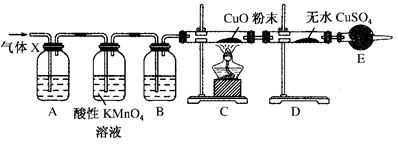
�Իش�
(1)����ʵ�������ɶ�����������Ļ�ѧ��Ӧ����ʽΪ
_________________________________________________________��
(2)��ͬѧ��Ϊ�����ܲ���������������____________________ _____________________________________��
(3)��ͬѧ�ڰ�װ��װ�úز����ٵ�һ������___________________________________________��
(4)B�м�����Լ���________����������___________________ _____________________________________��
(5)����֤������X�к���������ʵ�������ǣ�C��________��D��________�������ȥװ��B���Ƿ��ܸ���D�е������ж�����X�к���������
�� ___________________________________________________��
�ο��𰸣�(1)Zn��2H2SO4(Ũ)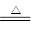 ZnSO4��SO2����2H2O
ZnSO4��SO2����2H2O
(2)��п��Ũ����ķ�Ӧ�����У�H2SO4�����ģ�����ˮ���ɣ�c(H2SO4)��С����Ũ������ϡ���ᣬп��ϡ���ᷴӦ��������
(3)����װ��������
(4)Ũ����,?����ˮ����
(5)��ɫ����ͭ��ĩ��ɺ�ɫ, ��ˮ����ͭ��ĩ�ɰ�ɫ�����ɫ�����ܣ��������ͨ��KMnO4��Һʱ�����ˮ���������ź���ʵ����H2�ļ���
���������(1)Ũ�������ǿ�����ԣ���п��Ӧ�Ļ�ѧ����ʽ�ǣ�Zn��2H2SO4(Ũ)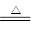 ZnSO4��SO2����2H2O��
ZnSO4��SO2����2H2O��
��2������п����Ũ����ķ�Ӧ�����У�H2SO4�����ģ�����ˮ���ɣ�����c(H2SO4)��С����Ũ������ϡ�����п����ϡ���ᷴӦ����������
��3���κ�ʵ��װ�����Ӻ��Ժ���Ҫ����װ�õ������ԡ�
��4������Ҫͨ����ˮ����ͭ�Ƿ������֤�������Ƿ��������������ں�����ͭ��Ӧ֮ǰ������Ҫ�������壬���B�м�����Լ���Ũ���ᣬԭ������ˮ������
��5�����ʵ���к�ɫ����ͭ��ĩ��ɺ�ɫ����ˮ����ͭ��ĩ�ɰ�ɫ�����ɫ��������˵���������������ڻ������ͨ��KMnO4��Һʱ�����ˮ���������ź���ʵ����H2�ļ��飬���������ȥװ��B���Ͳ��ܸ���D�е������ж�����X�к���������
��������ѧ��һ����ʵ��Ϊ������ѧ�ƣ������л�ѧʵ�鼴��ѧ̽��֮˵����̽����ʵ���һ��˼·�ǣ�1.ȷ�ذ���ʵ��Ŀ�ģ�2.������ѧ֪ʶ���������ʵ�����Ŀ�ĨD�Dʵ��ԭ����3.���ʵ����ϣ�����ȷ����ƶԲߣ���ʵ�鷽����
�����Ѷȣ�һ��
4��ѡ���� ����ʵ���ܹ��ﵽԤ��Ŀ�ĵ��ǣ�
A����һ֧ʢ��2mL 2�� CuSO4��Һ���Թ��У����뼸��10����NaOH��Һ���ټ���1mL��ȩ��Һ�����Ⱥ���Կ�����ɫ������ͭ��������
B��������������NaOH��Һ��ϲ���ˮԡ���ȣ����ɵõ�ˮ������Ҵ�������
C����������Ѿ�ˮ�⣬������������ϡ�������һ��ʱ�����NaOH��Һ�к����ᣬ�ټ���������Һ����
D����һ֧�Թ��е���10�������飬�ټ���1mL 5����NaOH��Һ�����Ⱥ�μ���������Һ���ɹ۲쵽��dz��ɫ�廯����������
�ο��𰸣�C
���������A������������ͭ��NaOH���������
B������������ˮ�⣬���ɵ��������Σ�
D��ˮ�������ữ�������������������ӽ�ϣ��������顣
�����Ѷȣ���
5��ʵ���� ijѧ��Ϊ��֤���ӡ����ᡢ̼�������ǿ�����������ؿ��ǣ��������ʵ��װ�ã���ش���������
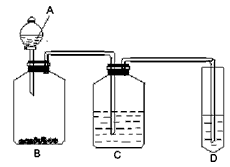
(1)����������ʢ�ŵ�ҩƷ��A______C______D______������������������ �ٱ��� �ڴ��� ��̼��
��Na2CO3 ��NaHCO3 �ޱ����ƣ�
(2) װ��C������____________��
(3) ��������֤�������������ǿ��������____________��
(4)д��װ��D�з�����Ӧ�Ļ�ѧ����ʽ__________________��
�ο��𰸣�(1)�ڣ��ݣ���
(2)��ȥCO2�е��Ȼ���
(3)Bװ���������ݣ�Dװ����Һ�����
(4)C6H5ONa?+CO2+H2O==C6H5OH+NaHCO3
���������
�����Ѷȣ�һ��