1、选择题 下列物质不属于有机物的是
A.CH4
B.C2H4
C.KSCN
D.C2H5OH
参考答案:C
本题解析:分析:根据含有碳元素的化合物叫有机化合物,简称有机物;碳的氧化物、碳酸盐、碳酸虽含碳,但其性质与无机物类似,因此把它们看作无机物;据此进行分析判断.
解答:A.CH4是一种含碳的化合物,属于有机物,故A错误;
B.乙烯是一种含碳的化合物,属于有机物,故B错误;
C.KSCN常归为无机物,故C正确;
D.乙醇是一种含碳的化合物,属于有机物,故D错误.
故选C.
点评:本题考查有机物的概念,难度不大,掌握有机物与无机物的概念、特征等是正确解答此类题的关键.
本题难度:一般
2、选择题 下列各分子中,所有原子都满足最外层为8电子结构的是
A.H2O
B.BF3
C.PCl5
D.CCl4
参考答案:D
本题解析:只要分子中元素化合价的绝对值与最外层电子数之和等于8,即可以满足满足最外层为8电子结构,据此可以判断。A、水中的H和O的化合价分别是+1价和-2价,因此氢元素不能满足最外层为8电子结构,氧元素满足,A不正确;B、BF3中B和F的化合价分别是+3价和-1价,则B元素不能满足最外层为8电子结构,F元素满足,B不正确;C、PCl5中P和Cl的化合价分别是+5价和-1价,则P元素不能满足最外层为8电子结构,Cl元素满足,C不正确;D、四氯化碳中C和Cl的化合价分别是+4价和-1价,均满足最外层为8电子结构,D正确,答案选D。
本题难度:一般
3、选择题 短周期元素X、Y、Z、W的原子序数依次增大,且原子最外层电予数之和为l3。X的原子半径比Y的小,X与W同主族,Z是地壳中含量最高的元素。下列说法正确的是
A.原子半径的大小顺序:r(Y)>r(Z)>r(W)
B.元素Z、W的简单离子的电子层结构不同
C.元素Y的简单气态氢化物的热稳定性比Z的强
D.只含X、Y、Z三种元素的化合物,可能是离子化合物,也可能是共价化合物
参考答案:D
本题解析:A、Z是地壳中含量最高的元素,则Z是O元素;X比Y的原子序数小,且X的原子半径比Y的小,所以X与Y不是同周期元素,X是第一周期元素H;X与W同主族,且W的原子序数大于O,所以W是Na;根据原子最外层电予数之和为l3,则Y是N元素。所以原子半径的大小顺序:r(W)>r(Y)>r(Z),错误;B、元素Z、W的简单离子的电子层结构都与Ne的原子结构相同,错误;C、N的非金属性比O的非金属性弱,所以Y的简单气态氢化物的热稳定性比Z的弱,错误;D、只含X、Y、Z三种元素的化合物,可能是离子化合物,如硝酸铵,也可能是共价化合物,如硝酸,正确,答案选D。
本题难度:一般
4、填空题 (10分)五种元素A、B、C、D、E位于元素周期表的前四周期,已知它们的核电荷数依次增加,A是宇宙中含量最多的元素;B原子的L层p轨道中有2个电子;C与B原子的价层电子数相同;D原子M层的d轨道有一个成对电子;E原子的L层电子数与最外层电子数之比为4:1,其d轨道中的电子数与最外层电子数之比为5:1。
(1)B与A形成只含一个中心原子的共价化合物,其分子的电子式为?,中心原子的杂化轨道类型是 ?,其分子的的立体构型是?
(2)A的氧化物与B的氧化物中,分子极性较小的是(填分子式)__________
(3)B与C比较,电负性较大的(填元素名称)____________
(4)写出D的价层电子排布式?
(5)E与Al的化学性质相似,请写出E与NaOH溶液反应的化学方程式?
(6)写出D的最高价氧化物与盐酸反应的离子方程式?
参考答案:(10分)(1)电子式?类型是?sp3杂化??,立体构型是?正四面体?
(2)分子极性较小的是(填分子式)_CO2__ (3)电负性较大的(填元素名称)___碳__
(4)价层电子排布式?3d64s2?
 (5化学方程式? Zn + 2NaOH = Na2ZnO2 + H2?
(5化学方程式? Zn + 2NaOH = Na2ZnO2 + H2?
(6)离子方程式? Fe2O3 + 6H+ = 2Fe3+ + 3H2O?
本题解析:略
本题难度:简单
5、计算题 铜有两种天然同位素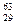 Cu和
Cu和 Cu,参考铜的原子量(63.5)估算
Cu,参考铜的原子量(63.5)估算 Cu的百分含量约是
Cu的百分含量约是
A.20%
B.25%
C.50%
D.66.7% E. 75%
参考答案:B
本题解析:用十字交叉法可求得两种同位素的原子个数比
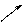
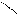 ? 65? 0.5 (65Cu)
? 65? 0.5 (65Cu)
 ? 63.5
? 63.5
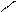 ? 63? 1.5 (63Cu)
? 63? 1.5 (63Cu)
即65Cu与63Cu的原子个数比为1:3,所以 Cu%=
Cu%=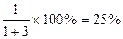 ,故应选B。
,故应选B。
本题难度:简单