1、选择题 下列物质中,既能与盐酸反应,又能与氢氧化钠溶液反应的是
A.Fe
B.Ca(OH)2
C.Na2CO3
D.NaHCO3
参考答案:D
本题解析:分析:根据物质间的反应进行判断,中学常见的既能与酸反应又能与碱反应的物质主要有:
①两性物质:Al2O3、ZnO、Al(OH)3、Zn(OH)2、氨基酸、蛋白质等;
②多元弱酸的酸式盐:NaHCO3、KHS、KHSO3、NaH2PO4等;
③弱酸的铵盐及其酸式盐:(NH4)2S、NH4HS、(NH4)2CO3、NH4HCO3、CH3COONH4等;
④某些具有两性的金属:Zn、Al等;
⑤某些非金属:Si、S等;
⑥其它一些物质.如:a、某些盐类物质既与酸反应,又与碱反应;
b、个别酸性氧化物SiO2;
c、具有还原性的无氧酸:H2S、HI等与氧化性酸反应、与碱反应;
d、具有氧化性酸:浓H2SO4、HNO3等与还原性酸反应、与碱反应,以此解答本题.
解答:A.Fe只能与盐酸反应,不能与氢氧化钠溶液反应,故A错误;
B.Ca(OH)2只能与盐酸反应,不能与氢氧化钠溶液反应,故B错误;
C.Na2CO3只能与盐酸反应,不能与氢氧化钠溶液反应,故C错误;
D.NaHCO3是弱酸的酸式盐,既能与盐酸反应,又能与氢氧化钠溶液反应,故D正确;
故选:D;
点评:本题考查了物质的性质,难度不大,旨在考查学生对知识的理解识记与知识归纳,明确物质的性质是解本题的关键,注意基础知识的积累.
本题难度:简单
2、选择题 向600mL?0.5?mol・L-1的硫酸溶液一定量的中加入Fe2O3、Cu的混合物,恰好使混合物完全溶解,所得溶液中不含Fe3+,若用过量的CO在高温下还原相同质量的原混合物,固体减少的质量为
A.6.4g
B.4.8g
C.2.4g
D.1.6g
参考答案:B
本题解析:设Fe2O3、Cu的物质的量分别是x和y,则根据反应式3H2SO4+Fe2O3=3H2O+Fe2(SO4)3、Fe2(SO4)3+Cu=2FeSO4+CuSO4可知,x=y,消耗硫酸是3x,所以x=0.1mol,则混合物中氧元素的质量是3x×16g/mol=4.8g,则固体减少的质量就是4.8g,答案选B。
本题难度:一般
3、选择题 a?g铁粉与含有H2SO4的CuSO4溶液完全反应后,得到a?g铜,则参与反应的CuSO4与H2SO4的物质的量之比为
A.7:1
B.1:7
C.7:8
D.8:7
参考答案:A
本题解析:分析:Fe先与CuSO4反应,再与H2SO4反应,根据反应的顺序和相关的量进行计算.
解答:ag铁粉为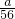 mol,agCu为
mol,agCu为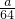 mol,根据氧化还原顺序Fe先与CuSO4反应,再与H2SO4反应,因为
mol,根据氧化还原顺序Fe先与CuSO4反应,再与H2SO4反应,因为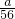 mol>
mol>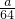 mol,
mol,
所以CuSO4反应完全,剩余Fe与H2SO4反应,
所以参加反应的CuSO4的物质的量为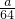 mol,
mol,
参加反应的H2SO4的物质的量为(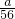 -
-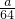 )mol,
)mol,
参加反应的CuSO4和H2SO4的物质的量之比为: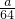 :(
:(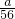 -
-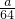 )=7:1,
)=7:1,
故选A.
点评:本题考查学生对金属铁的性质的掌握,可以根据所学知识进行回答,难度较大.
本题难度:困难
4、选择题 下列各项操作中,不发生“先产生沉淀,然后沉淀又溶解”现象的是
A.向饱和碳酸钠溶液中通入过量的CO2
B.向Fe(OH)3胶体中逐滴加入过量的稀硫酸
C.向NaAlO2溶液中逐滴加入过量的盐酸
D.向硅酸钠溶液中逐滴加入过量的盐酸
参考答案:AD
本题解析:分析:根据复分解反应发生的条件及物质的溶解性来分析能够反应且“先产生沉淀,然后沉淀又溶解”,注意反应与量有关.
解答:A、向饱和碳酸钠溶液中通入过量的CO2,二氧化碳和碳酸钠反应生成碳酸氢钠,碳酸氢钠的溶解性小于碳酸钠的溶解性,所以向饱和碳酸钠溶液中通入过量二氧化碳后溶液中会产生碳酸氢钠沉淀,但沉淀不溶解,所以符合条件,故A选.
B、向Fe(OH)3胶体中逐滴加入过量的稀硫酸,先胶体和电解质溶液产生聚沉现象,有沉淀生成;后氢氧化铁又和硫酸反应生成可溶性的硫酸铁,所以沉淀又溶解,所以不符合条件,故B不选.
C、向NaAlO2溶液中逐滴加入过量的盐酸,偏铝酸钠和盐酸反应先生成氢氧化铝沉淀,后氢氧化铝和盐酸反应生成可溶性的氯化铝,所以看到的现象是“先产生沉淀,然后沉淀又溶解”,所以不符合条件,故C不选.
D、向硅酸钠溶液中逐滴加入过量的盐酸,硅酸钠和盐酸反应生成难溶性的硅酸,所以看到的现象是“有沉淀生成”,所以符合条件,故D选.
故选AD.
点评:本题考查物质之间的化学反应,熟悉复分解反应发生的条件及常见物质的溶解性是解答本题的关键,注意有些反应与反应物的量有关,量不同反应现象不同,如B、C选项.
本题难度:简单
5、选择题 下列各组内物质的转化,只通过一步反应不能完成的是
A.Fe→H2
B.Na2O→Na2SO4
C.SO2→CaSO3
D.Cu→Cu(OH)2
参考答案:D
本题解析:分析:A、铁和稀硫酸反应生成氢气;
B、氧化钠和硫酸反应生成硫酸钠;
C、二氧化硫和氧化钙反应生成亚硫酸钙;
D、铜不能一步反应生成氢氧化铜;
解答:A、铁和稀硫酸反应生成氢气,Fe+H2SO4=FeSO4+H2↑,故A不符合;
B、氧化钠和硫酸反应生成硫酸钠和水,Na2O+H2SO4=Na2SO4+H2O,故B不符合;
C、二氧化硫和氧化钙反应生成亚硫酸钙,CaO+SO2=CaSO3 ,故C不符合;
D、铜不能一步生成氢氧化铜,故D符合;
故选D.
点评:本题考查了物质性质的分析判断,一步反应的转化是解题的关键,熟练掌握物质性质,注意积累知识,题目较简单.
本题难度:简单