1、选择题 硫-钠原电池具有输出功率较高,循环寿命长等优点。其工作原理可表示为:2Na+xS Na2Sx。但工作温度过高是这种高性能电池的缺陷,科学家研究发现,采用多硫化合物(
Na2Sx。但工作温度过高是这种高性能电池的缺陷,科学家研究发现,采用多硫化合物(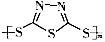 )作为电极反应材料,可有效地降低电池的工作温度,且原材料价廉、低毒,具有生物降解性。下列有关叙述正确的是
)作为电极反应材料,可有效地降低电池的工作温度,且原材料价廉、低毒,具有生物降解性。下列有关叙述正确的是
A.多硫化合物(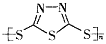 )是一种新型无机非金属材料
)是一种新型无机非金属材料
B.多硫化合物( )化合物不能发生加成反应
)化合物不能发生加成反应
C.原电池的负极反应是将单体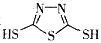 转化为
转化为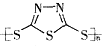 的过程
的过程
D.当电路中有0.02mol电子通过时,原电池的负极将消耗原料0.46g
2、选择题 根据下列实验现象,所得结论正确的是
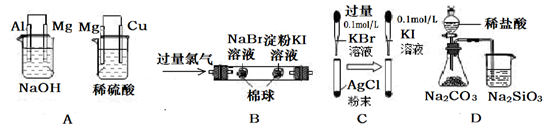
实验
| 实验现象
| 结论
|
A
| 左边烧杯中镁表面有气泡,右边烧杯中铜表面有气泡
| 还原性: Al>Mg>Cu
|
B
| 左边棉花变为橙色,右边棉花变为蓝色
| 氧化性:Cl2>Br2>I2
|
C
| 试管中白色固体先变淡黄色,后变为黄色
| 沉淀转化的实质就是沉淀溶解平衡的移动
|
D
| 锥形瓶中有气体产生,烧杯中溶液变浑浊
| 非金属性:Cl>C>Si
|
3、选择题 有关下列图像说法正确的是(?)
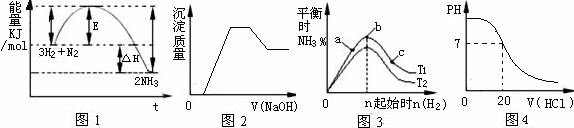
A.由图1可知合成氨反应为自发反应,加入适当的催化剂,E和△H都减小
B.图2表示向含有H+、Mg2+、Al3+、NH4+中加入NaOH溶液与产生沉淀质量的变化关系
C.图3表示合成氨反应在其他条件不变的情况下,改变起始物n(H2)对此反应平衡的影响。可知反应物N2的转化率最高的是b点;T1>T2,K2> K1(T1和T2表示温度,K1、K2表示对应温度下平衡常数)
D.图4表示25℃时,用0.1 mol・L-1盐酸滴定20 mL 0.1 mol・L-1氨水的pH随加入盐酸体积的变化
4、选择题 有一种燃料电池,所用燃料为H2和空气,电解质为熔融的K2CO3。电池的总反应式为:2H2+O2===2H2O,负极反应为H2+CO-2e-===H2O+CO2。该电池放电时,下列说法中正确的是( )
A.正极反应为2H2O+O2+4e-===4OH-
B.常温常压下每消耗22.4LH2向外电路提供的电子小于2mol
C.电子由正极经外电路流向负极
D.电池中CO的物质的量将逐渐减少
5、选择题 如图,一种微型钮扣电池,其电极材料分别为Ag2O和Zn,电解质溶液是KOH溶液。该电池负极的反应式:Zn -2e-+ 2OH-=ZnO+ H2O,总反应式为:Zn+ Ag2O=ZnO+ 2Ag。根据以上提供的资料,判断下列说法正确的是

[? ]
A.正极的反应式:Ag2O+ 2e-+H2O=2Ag+ 2OH-
B.放电时负极附近溶液的 pH不变
C.放电时每消耗6.5 g Zn,转移电子0.1 mol
D.放电时溶液中阴离子向正极方向移动,阳离子向负极方向移动