|
|
|
高中化学知识点大全《化学反应速率》考点预测(2017年强化版)(七)
2018-03-17 08:22:49
来源:91考试网
作者:www.91exam.org 【 大 中 小】
|
1、填空题 一定温度下在体积为5 L的密闭容器中发生可逆反应。(Ⅰ)若某可逆反应的化学平衡常数表达式为:K=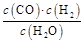
(1)写出该反应的化学方程式:?
(2)能判断该反应一定达到化学平衡状态的依据是 (填选项编号)。?
A.容器中气体的平均相对分子质量不随时间而变化
B.v正(H2O)=v逆(H2)
C.容器中气体的密度不随时间而变化
D.容器中总质量不随时间而变化
| E.消耗n mol H2的同时消耗n mol CO
(Ⅱ)若该密闭容器中加入的是2 mol Fe(s)与1 mol H2O(g),t1秒时,H2的物质的量为0.20 mol,到第t2秒时恰好达到平衡,此时H2的物质的量为0.35 mol。
(1)t1~t2这段时间内的化学反应速率v(H2)= 。?
(2)若继续加入2 mol Fe(s),则平衡 移动(填“向正反应方向”、“向逆反应方向”或“不”),继续通入1 mol H2O(g),再次达到平衡后,H2物质的量为 mol。?
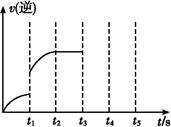
(3)该反应的逆反应速率随时间变化的关系如图。t1时改变了某种条件,改变的条件可能是 、 (填写2项)。?
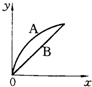
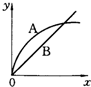
2、选择题 进行如下实验,在A锥形瓶中放入10g绿豆大小的碳酸钙,在B锥形瓶中放入5g粉末状的碳酸钙,分别加入50mL?1mol/L盐酸,下图中能正确表示实验结果的是(注:x一时间、y-锥形瓶中碳酸钙减少的质量)( )
A.
B.
C.
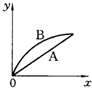
D.

3、选择题 某探究小组利用丙酮的溴代反应(CH3COCH3+Br2 CH3COCH2Br+HBr)来研究反应物浓度与反应速率的关系.反应速率v(Br2)通过测定溴的颜色消失所需的时间来确定.在一定温度下,获得如下实验数据:
| 实验序号 | 初始浓度c/mol-L-1 | 溴颜色消失所需的时间t/s
CH3COCH3
HCl
Br2
①
0.80
0.20
0.0010
290
②
1.60
0.20
0.0010
145
③
0.80
0.40
0.0010
145
④
0.80
0.20
0.0020
580
|
分析实验数据所得出的结论不正确的是( )
A.增大c(CH3COCH3),v(Br2)增大
B.实验②和③的v(Br2)相等
C.增大c(HCl),v(Br2)增大
D.增大c(Br2),v(Br2)增大
4、填空题 (14分)捕碳技术(主要指捕获CO2)在降低温室气体排放中具有重要的作用。目前NH3和(NH4)2CO3已经被用作工业捕碳剂,它们与CO2可发生如下可逆反应:
反应Ⅰ:2NH3(l)+H2O(l)+CO2(g)  ?(NH4)2CO3(aq)? ΔH1 ?(NH4)2CO3(aq)? ΔH1
反应Ⅱ:NH3(l)+H2O(l)+CO2(g)  NH4HCO3(aq)? ΔH2 NH4HCO3(aq)? ΔH2
反应Ⅲ:(NH4)2CO3(aq)+H2O(l)+CO2(g)  2NH4HCO3(aq)? ΔH3 2NH4HCO3(aq)? ΔH3
请回答下列问题:
(1)ΔH3与ΔH1、ΔH2之间的关系是:ΔH3=?。
(2) 反应Ⅲ的化学平衡常数表达式为 ?。
(3)为研究温度对(NH4)2CO3捕获CO2效率的影响,在某温度T1下,将一定量的(NH4)2CO3溶液置于密闭容器中,并充入一定量的CO2气体(用氮气作为稀释剂),在t时刻,测得容器中CO2气体的浓度。然后分别在温度为T2、T3、T4、T5下,保持其他初始实验条件不变,重复上述实验,经过相同时间测得CO2气体浓度,得到趋势图(见图1)。则:
①ΔH3?0(填“>”、“=”或“<”)。
②在T1~T2及T4~T5两个温度区间,容器内CO2气体浓度呈现如图1所示的变化趋势,其原因是?
?。
③反应Ⅲ在温度为T1时,溶液pH随时间变化的趋势曲线如图2所示。当时间到达t1时,将该反应体系温度迅速上升到T2,并维持该温度。请在该图中画出t1时刻后溶液的pH变化总趋势曲线。
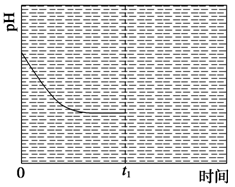 ? ?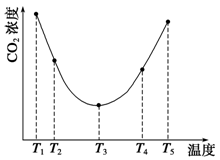
图1?图2
(4)利用反应Ⅲ捕获CO2,在(NH4)2CO3初始浓度和体积确定的情况下,提高CO2吸收量的措施有?
?。
(5)下列物质中也可以作为CO2捕获剂的是?。
A.NH4Cl
B.Na2CO3
C.HOCH2CH2OH
D.HOCH2CH2NH2
5、选择题 已知某反应的各物质浓度数据如下:
aA(g)+bB(g)  2C(g) 2C(g)
起始浓度(mol・L-1)? 3.0? 1.0? 0
2 s末浓度(mol・L-1)? 1.8? 0.6? 0.8
据此可推算出上述反应化学方程式中,各物质的化学计量数之比是
( )。
A.9∶3∶4
B.3∶1∶2
C.2∶1∶3
D.3∶2∶1
|
