1、选择题 某无色溶液,由Na+、Ca2+、Al3+、Cu2+、AlO2-、CO32-、SO32-、SO42-中的若干种组成.取适量该溶液进行如下实验:①加入过量盐酸,有无色、无味气体X生成;②在①所得的溶液中再加入过量碳酸氢铵溶液,有气体生成,同时析出白色沉淀甲;③在②所得溶液中加入过量Ba(OH)2溶液并加热,有刺激性气味的气体Y生成,并析出白色沉淀乙.则下列判断正确的是( )
A.原溶液中一定存在的离子是Na+、AlO2-、CO32-
B.原溶液中一定存在的离子是Al3+、SO42-、CO32-
C.白色沉淀甲为Al(OH)3、乙为BaSO4
D.气体X为CO2、气体Y为SO2
2、选择题 今有一混合物的水溶液,只可能含有以下离子中的若干种:NH4+、Cl-、Mg2+、Ba2+、K+、CO32-、SO42-,现取三份100mL溶液进行如下实验:
①第一份加入AgNO3溶液有沉淀产生;
②第二份加足量NaOH溶液加热后,收集到气体0.04mol
③第三份加足量BaCl2溶液后,得干燥沉淀6.27g,经足量盐酸洗涤.干燥后,沉淀质量为2.33g.
根据上述实验,以下推测正确的是( )
A.K+一定存在
B.该溶液中含CO32-离子的浓度为0.1mol/L
C.Cl-可能存在
D.Ba2+一定不存在,Mg2+可能存在
3、选择题 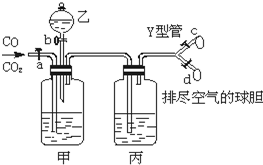 下图的实验装置用来分离CO2和CO气体并干燥.图中a为止水夹,b为分液漏斗的活塞,通过Y型管和止水夹分别接c、d两球胆,现装置内的空气已排尽.为使实验成功,甲、乙、丙分别盛放的溶液是
下图的实验装置用来分离CO2和CO气体并干燥.图中a为止水夹,b为分液漏斗的活塞,通过Y型管和止水夹分别接c、d两球胆,现装置内的空气已排尽.为使实验成功,甲、乙、丙分别盛放的溶液是
A.NaHCO3饱和溶液? 12 mol?L-1盐酸? ?18.4 mol?L-1H2SO4
B.Na2CO3饱和溶液? 2 mol?L-1H2SO4 18.4 mol?L-1H2SO4
C.NaOH饱和溶液?2 mol?L-1H2SO4?18.4 mol?L-1H2SO4
D.18.4 mol?L-1H2SO4 NaOH饱和溶液? 18.4 mol?L-1H2SO4
4、选择题 下列鉴别方法可行的是
[? ]
A.用氨水鉴别Al3+、Mg2+和Ag+
B.用Ba(NO3)2溶液鉴别Cl-、SO42-和CO32-
C.用核磁共振氢谱鉴别1-溴丙烷和2-溴丙烷
D.用KMnO4酸性溶液鉴别CH3CH=CHCH2OH和CH3CH2CH2CHO
5、填空题 由Fe2O3、Fe、CuO、C、Al中的几种物质组成的混合粉末,取样进行下列实验(部分产物略去)

(1)取少量溶液X,加入过量的NaOH溶液,有沉淀生成。取上层清液,通入CO2,无明显变化,说明样品中不含有的物质是________________。(填化学式)
(2)如何检验Y中的金属阳离子______________________________。
(3)Z为一种或两种气体:
①若Z只为一种气体,试剂a为饱和NaHCO3溶液,则反应Ⅰ中能同时生成两种气体的化学方程式是
______________________________。
②若Z为两种气体的混合物,试剂a为适量的水,则Z中两种气体的化学式是________________。
(4)向Y中通入过量的Cl2,并不断搅拌,充分反应后,溶液中的阳离子是________。(填写离子符号)
(5)取Y中的溶液,调节pH约为7,加入淀粉KI和H2O2,溶液呈蓝色并有红褐色沉淀生成。当消耗2molI-时,共转移3mol电子,该反应的离子方程式是__________________________。