1��ѡ���� �����豸����ʱ������ѧ��ת��Ϊ���ܵ���(? )

�ο��𰸣�B
���������A����̫���ܵ���ǽ�̫����ֱ��ת��Ϊ���� ������B������ӵ�ؽ���ѧ��ֱ��ת��Ϊ���ܣ�����C��̫���ܼ������ǽ�̫����ת��Ϊ���ܣ�����D��ȼ��ȼ�ս���ѧ��ֱ��ת��Ϊ���ܣ���ȷ��
�����Ѷȣ���
2��ѡ���� CO(g)+H2O(g)  ?H2(g)+CO2(g)?��H��0���������������������£�����˵����ȷ����
?H2(g)+CO2(g)?��H��0���������������������£�����˵����ȷ����
A������������ı��˷�Ӧ��;������Ӧ�ų�������Ҳ��֮�ı�
B���ı�ѹǿ��ƽ�ⲻ�����ƶ�����Ӧ�ų�����������
C�������¶ȣ���Ӧ���ʼӿ죬��Ӧ�ų�����������
D������ԭ����н��У���Ӧ�ų�����������
�ο��𰸣�B
���������A������������ı��˷�Ӧ��;���������ı䷴Ӧ��Ͳ�����������ʷ�Ӧ�ų����������ı䣬��ԭ˵������B���ı�ѹǿ��ƽ�ⲻ�����ƶ�����Ӧ�ų����������䣬��ȷ��C�������¶ȣ���Ӧ���ʼӿ죬ʹ����ƽ�������ȷ����ƶ����������ƶ�����Ӧ�ų���������С��ԭ˵������D������ԭ����н��У�����ѧ��ת��Ϊ�����ˣ���Ӧ�ų������������٣���ԭ˵������ȷ��
�����Ѷȣ�һ��
3��ѡ���� �����뻯ѧ��Ӧ�����仯��ص���������ȷ����(? )
A����Ӧ�Ⱦ��Ƿ�Ӧ�ų�������
B�����ȷ�Ӧ�ķ�Ӧ�������Ǵ������ȷ�Ӧ�ķ�Ӧ����
C����ѧ��Ӧ�е��ʱ������ѧ�����Ѻ��γɵ������仯
D��ͬ��ͬѹ�£�H2(g)��Cl2(g)��2HCl(g) ��H���ڹ��պ͵�ȼ�����·�Ӧ����H��ͬ
�ο��𰸣�D
�����������Ӧ����ָ��Ӧǰ��������仯���з��Ⱥ��������֣�A����Ӧ��������Ⱥ������أ�B����ѧ��Ӧ�е��ʱ䲻���뻯ѧ�����γɡ������йأ��������ʵ�״̬�йأ�C�����ݸ�˹���ɣ���Ӧ��ֻ�뷴Ӧʼĩ״̬�йأ��뷴Ӧ�������أ�����D��ȷ����ѡD��
�����Ѷȣ���
4��ѡ���� ����˵����������
A��SO2ͨ��Ba��NO3��2��Һ�еõ�BaSO3����
B���к͵ζ�ʵ���У���ƿ������ˮϴ����δ�����Ӱ��ⶨ���
C�������ȷ�Ӧ�����Է����У������ȷ�Ӧ�����Է�����
D����C��ʯī����C�����ʯ������H����1��90 kJ��mol��֪���ʯ��ʯī�ȶ�
�ο��𰸣�B
������������⿼��Ԫ�ػ�����֪ʶ���к͵ζ�����ѧ��Ӧ�ķ�����жϼ���ѧ��Ӧ�������ı仯������NO3-�������������ܽ�SO2����ΪH2SO4����SO2ͨ��Ba��NO3��2��Һ��Ӧ�õ�BaSO4������A���������к͵ζ�ʵ���У���ƿ������ˮϴ����δ�����Ӱ�����Һ�����ʵ����ʵ������ʲ�Ӱ��ⶨ�����B�������е����ȷ�ӦҲ���Է����еģ����Ȼ����Ba��OH��2��8H2O�ķ�ӦΪ�Է����еķ�Ӧ��C���������ӷ�Ӧ����ʽ��֪����Ӧ��������������������������������ʯī�Ƚ��ʯ�ȶ���D��������
�����Ѷȣ�һ��
5������� ���ô�������Ӧ��SO2ת��ΪSO3�ǹ�ҵ����������Ĺؼ����裮T��ʱ��Ӧ2SO2��g��+O2��g��

2SO3��g�������е������仯��ͼ��ʾ���ش��������⣮
��1��д���÷�Ӧ���Ȼ�ѧ����ʽ����E1��E2��E3��ʾ����ͬ��______��
��2��T��ʱ��3molSO2��1molO2ͨ�����Ϊ2L�ĺ��º����ܱ������У�������Ӧ��2minʱ��Ӧ�ﵽƽ�⣬��ʱ��÷�Ӧ��O2��ʣ��0.1mol����ﵽƽ��ʱSO2��ת����Ϊ______����Ӧ______����ų��������ա���______����������E1��E2��E3��ʾ��
��3������������֤���÷�Ӧ�Ѵﻯѧƽ��״̬����______������ţ�
��SO2������������ٷ����仯?��������ѹǿ���ٷ����仯?������������ԭ���������ٷ����仯?����ͬʱ��������2n?molSO2��ͬʱ����n?molO2?����ͬʱ��������2n?molSO2��ͬʱ����2n?molSO3
��4���ڷ�Ӧ��ϵ�м����������Ӧ��������E1��E2��E3�ı仯�ǣ�E1______��E2______��E3______���������С�����䡱����
��5��������ͼ��ʾװ�ã��õ绯ѧԭ���������ᣬ��SO2��O2��һ��ѹǿ�絽���Ե缫�Ϸ�Ӧ��д�����缫�ĵ缫��Ӧʽ��______��Ϊ�ȶ�����������������Һ��Ũ��Ӧά�ֲ��䣬��ͨ��SO2��ˮ��������Ϊ______��
��6��SOCl2��һ����ɫҺ�壬����̼��ͬ����﮵�ص��������ϣ�����ŵ�ʱҲ��SO2���������д��SOCl2�ڵ���зŵ�ʱ�ĵ缫��Ӧʽ______��

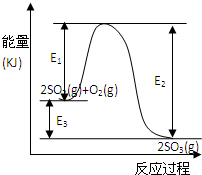
�ο��𰸣���1����H=��Ӧ�����յ�����-������ų��������T-E3kJ/mol=-��E2-E1��kJ/mol��
�ʴ�Ϊ��2SO2��g��+O2��g��?2SO3��g����H=-E3kJ/mol ���H=-��E2-E1��kJ/mol
��2����ͼ��֪����Ӧ���������������������������Ը÷�Ӧ�Ƿ��ȷ�Ӧ��
? 2SO2��g��+O2��g��?2SO3��g��?���� E3?
? ��Ӧ��ʼ?3 mol? 1mol? 0? E3
? ת��?1.8 mol? 0.9mol? 1.8 mol? 0.9E 3
? ƽ��?1.2mol? 0.1mol? 1.8 mol?
? ����SO2��ת����=1.8mol?3mol��100%=60%
�ų����� 0.9E 3
�ʴ�Ϊ��60%���ų��� 0.9 E3��
��3���÷�Ӧǰ�����������С����ѧƽ��״̬�ı�־�����淴Ӧ������ȡ���ϵ�����ʵĺ������䣮
�٢ڢܷ�������������ԭ���غ㣬��Ԫ�ص�ԭ������ʼ�ղ��䣬�ʢ۴�������ָ����һ�£��ʢݴ���
��ѡ���٢ڢܣ�
��4������������ı��˷�Ӧ���̣��ı䷴Ӧ���ʣ���ƽ�ⲻ�ƶ�������E2��E1 ��С��E3���䣬
�ʴ�Ϊ��E2��E1 ��С��E3���䣻
��5������ԭ��ط�Ӧԭ������ԭ���ڸ����Ϸ���������Ӧ�缫��ӦʽΪSO2-2e-+2H2O�TSO42-+4H+�����������������Ϸ�����ԭ��Ӧ�缫��ӦʽΪO2+4e-+4H+�T2H2O����ԭ��صı�����2SO2+O2+2H2O=2H2SO4��Ϊά��Ũ�Ȳ��䣬SO2��O2��Ӧ�������������������50%�������ˮΪ��Ӧ��Ӧ��ˮ�����ܼ���ˮ������������Ϊ=2��64����2��18+2��98��=16��29
�ʴ�Ϊ��+��O2+4e-+4H+�T2H2O��-��SO2-2e-+2H2O�TSO42-+4H+�� 16��29��
��6��SOCl2��S�Ļ��ϼ���+4�ۣ����м��̬���ܷ���������ԭ��Ӧ����Ӧ���ж����������ɣ�Ҳ��S�������ɣ���ط�ӦʽΪ2SOCl2+4e-�TS+SO2��+4Cl-��
�ʴ�Ϊ��2SOCl2+4e-�TS+SO2��+4Cl-��
���������
�����Ѷȣ�һ��