|
|
|
高考化学知识点总结《能量的相互转化》高频试题特训(2019年最新版)(十)
2019-03-14 22:53:01
【 大 中 小】
|
1、简答题 如图是198K时N2与H2反应过程中能量变化的曲线图.下列叙述正确的是( )
A.该反应的热化学方程式为:N2+3H2?2NH3,△H=-92kJ?mol-1
B.a曲线是加入正催化剂时的能量变化曲线
C.加入催化剂,该化学反应的反应热改变
D.在温度体积一定的条件下,通入1molN2和3molH2反应后放出的热量为Q1kJ,若通入2?molN2和6?molH2反应后放出的热量为Q2kJ,则184>Q2>2Q1
| 
参考答案:A、热化学方程式必须标注物质的聚集状态反应的焓变,该反应的热化学方程式为:N2(g)+3H2(g)?2NH3(g),△H=-92kJ?mol-1,故A错误;
B、催化剂能改变反应的路径,使发生反应所需的活化能降低,但不改变化学平衡,反应的热效应不变,故图象中的b曲线是加入正催化剂时的能量变化曲线,故B错误;
C、催化剂能改变反应的路径,使发生反应所需的活化能降低,但不改变化学平衡,反应的热效应不变,故C错误;
D、向密闭容器中通入1mol?N2和3mol?H2,不可能完全转化,所以达到平衡时放出热量Q1kJ<92.4kJ;另一容积相同的密闭容器中通入2mol N2和6mol H2,达到平衡时放出热量理论上讲应该是2×92.2kJ=184KJ,但反应物不可能充分进行彻底,所以Q2<184KJ,同时通入2mol N2和6mol H2的压强比通入1mol?N2和3mol?H2的大了,平衡还会向正向移动,放出的热量还会增大,即Q2>2Q1,故D正确.
故选D.
本题解析:
本题难度:一般
2、选择题 已知某反应的△H=-150kJ?mol-1,下列有关该反应的叙述正确的是( )
A.该反应的反应物总能量低于生成物总能量
B.逆反应活化能一定小于150?kJ?mol-1
C.正反应活化能小于150?kJ?mol-1
D.逆反应活化能比正反应活化能大150?kJ?mol-1
参考答案:A、该反应为放热反应,所以反应物总能量大于生成物总能量,故A错误;
B、某反应的△H=-150kJ?mol-1,则正反应的活化能-逆反应的活化能=-150kJ?mol-1,无法确定逆反应活化能的大小,故B错误;
C、某反应的△H=-150kJ?mol-1,则正反应的活化能-逆反应的活化能=-150kJ?mol-1,无法确定正反应活化能的大小,故C错误;
D、某反应的△H=-150kJ?mol-1,则正反应的活化能-逆反应的活化能=-150kJ?mol-1,即逆反应活化能比正反应活化能大150?kJ?mol-1,故D正确;
故选:D.
本题解析:
本题难度:简单
3、填空题 (15分)二甲醚(CH3OCH3)被称为21世界的新型燃料,在未来可能替代汽油、液化气、煤气等并具有优良的环保性能。工业制备二甲醚在催化反应室中(压力2.0~10.0Mpa,温度230~280℃)进行下列反应:
①CO(g)+2H2(g) CH3OH(g)?△H1=-90.7kJ・mol-1 CH3OH(g)?△H1=-90.7kJ・mol-1
②2CH3OH(g) CH3OCH3(g) +H2O(g)?△H2=-23.5kJ・mol-1 CH3OCH3(g) +H2O(g)?△H2=-23.5kJ・mol-1
③CO(g)+H2O(g) CO2(g)+H2(g)?△H3=-41.2kJ・mol-1 CO2(g)+H2(g)?△H3=-41.2kJ・mol-1
(1)若要增大反应①中H2的转化率,在其它条件不变的情况下可以采取的措施为?。
A.加入某物质作催化剂
B.加入一定量CO
C.反应温度降低
D.增大容器体积
|
(2)在某温度下,若反应①的起始浓度分别为:
c(CO)=1 mol/L,
c(H2)=2.4 mol/L,5 min后达到平衡,CO的转化率为50%,则5 min内CO的平均反应速率为
?;若反应物的起始浓度分别为:
c(CO)=4 mol/L,
c(H2)=
a mol/L;达到平衡后,
c(CH3OH)=2 mol/L,
a=
?mol/L。
(3)催化反应室中总反应3CO(g)+3H2(g)

CH3OCH3(g)+CO2(g)的△
H=
?;830℃时反应③的K=1.0,则在催化反应室中反应③的K
?1.0(填“>”、“<”或“=”)。
(4)二甲醚的燃烧热为1455 kJ・mol-1,则二甲醚燃烧的热化学方程式为
?。

(5)“二甲醚燃料电池”是一种绿色电源,其工作原理如图所示。b电极是
?极,写出a电极上发生的电极反应式
?。
参考答案:(15分)(1)B C(2分)?(2)0.1mol/(L・min) (2分);5.4 (2分)
(3)ΔH=-246.1 kJ・mol-1(2分);>(2分)
(4)CH3OCH3(g)+3O2(g)=2CO2(g)+3H2O(l)?ΔH=-1455 kJ・mol-1(2分)
(5)正极(1分);CH3OCH3+3H2O-12e-=2CO2+12H+(2分)
本题解析:略
本题难度:一般
4、选择题 某反应的反应过程和能量变化如图所示,下列有关该反应的叙述正确的是
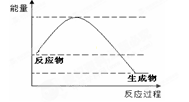
A.该反应的反应热△H < 0
B.反应物的总能量低于生成物的总能量
C.该反应是吸热反应
D.加入催化剂后反应放出的热会减少
参考答案:A
本题解析:根据图像可知,反应物的总能量高于生成物的总能量,反应是放热反应,所以选项A正确,其余都是错误的,答案选A。
本题难度:简单
5、选择题 下列说法不正确的是
A.焦炭在高温下与水蒸气的反应是吸热反应
B.氢氧化钾与硝酸的反应是放热反应
C.燃料有足够的空气就能充分燃烧
D.化学反应的过程,都可以看成是“贮存”在物质内部的能量转化为热能等而被释放出来的过程
参考答案:CD
本题解析:略
本题难度:简单

 CH3OCH3(g)+CO2(g)的△H=?;830℃时反应③的K=1.0,则在催化反应室中反应③的K?1.0(填“>”、“<”或“=”)。
CH3OCH3(g)+CO2(g)的△H=?;830℃时反应③的K=1.0,则在催化反应室中反应③的K?1.0(填“>”、“<”或“=”)。
