| �߿�ʡ������ | |
|
|
| �߿�ʡ������ | |
|
|
|
�߿���ѧ֪ʶ������������ˮ���ԭ����������ѵ��2019���̰棩(��)
�ο��𰸣�BD ���������CH3COONa ��Һ�д��ڣ�CH3COO����H2O �����Ѷȣ�һ�� 3��ѡ���� 50��ʱ�����и���Һ�У����ӵ����ʵ���Ũ�ȹ�ϵ��ȷ���� |
�ο��𰸣�C
���������A��pH=4�Ĵ����У�c��H+��=10��4mol��L��1������B�����������غ�֪������С�մ���Һ�У�c��Na+��= c��HCO3����+ c��CO32����+ c��H2CO3��������C�����ݵ���غ�֪������ʳ��ˮ�У�c��Na+��+ c��H+��= c��Cl����+c��OH��������ȷ��D��50��ʱKw��1��10��14��pH=12�Ĵ�����Һ�У�c��OH������1��0��10��2mol?L��1������
���㣺����pH���㡢��Һ������Ũ�ȴ�С��ϵ��
�����Ѷȣ�һ��
4������� ��ҵ���õ�ⱥ��NaCl��Һ�ķ�������ȡNaOH��Cl2��H2����������Ϊԭ������һϵ�л�����Ʒ����Ϊ�ȼҵ��
��1����������Ĥ��������ʳ��ˮʱ��Cl2����NaOH��ֽӴ������²������NaClO��H2����Ĥ��������ʳ��ˮ��Ӧ�����ӷ���ʽΪ ��
��2���ȼҵ���ܸߣ�һ�ֽ�������ȼ�ϵ������ϵ��¹��տ��Խڣ��磩��30�����ϡ������ֹ�������У�������ϵĴ�����ת����ϵ����ͼ��ʾ�����еĵ缫δ��������õ�����Ĥ��ֻ����������ͨ����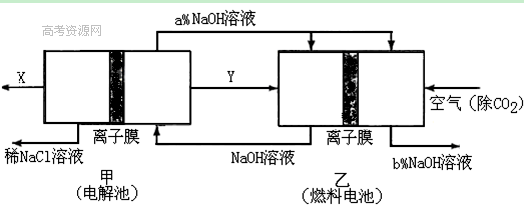
�پ����Ƶı���NaCl��ҺӦ��ͼ�е��ص� ����д���� ���ҡ�����ע�롣
��ͼ��X��____ __���ѧʽ�����������ҵĵ缫��ӦʽΪ�� _ ��ͼʾ������������Һ��������a����b���Ĺ�ϵ�� ������ĸ����
A. a%=b% B. a%
�ο��𰸣�
���������
�����Ѷȣ�����
5��ѡ���� 200mL0.1 mol��L-1CH3COOH��200mL0.1 mol��L-1NaOH��Һ��Ϻ�����Ũ�ȹ�ϵ��ȷ����
A.c(Na��)=c(CH3COO��)+c(CH3COOH)
B.c(Na��)��c(OH��)��c(CH3COO��)��c(H+)
C.c(Na��)+c(OH��)= c(CH3COO��)+c(H+)
D.c(Na��)��c(CH3COO��)��c(H+)��c(OH��)
�ο��𰸣�A
������������������200mL0.1 mol��L-1CH3COOH��200mL0.1 mol��L-1NaOH��Һ��Ϻ��൱��400mL0.1 mol��L-1CH3COONa��Һ��A����ȷ�������غ㣬��Ԫ�ص����������ĸ��ִ�����̬�൱��B��D����ȷ��CH3COO�D����ˮ�⣬��Һ�ʼ��ԣ�c(CH3COO��)��c(OH��)��ӦΪc(Na��)��c(CH3COO��)��c(OH��)��c(H+)��C������ȷ���ɵ���غ��֪��c(Na��)+c(H+)= c(CH3COO��)+c(OH��)��ѡA��
����?���������Һ������Ũ�ȼ��ϵ����С�Ƚ�
�����Ѷȣ�����
| ���� �� С������ӡ�� �������� ���ر��� �����ض����� | |
| ��һƪ���߿���ѧ֪ʶ���ܽᡶԭ���ԭ��.. | |
| �����Ŀ |