1、选择题 一定条件下,在体积为10L的密闭容器中,1mol X和1mol Y进行反应:2X(g)+Y(g)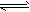 Z(g),经60s达到平衡,生成0.3mol Z,下列说法正确的是
Z(g),经60s达到平衡,生成0.3mol Z,下列说法正确的是
[? ]
A.以X浓度变化表示的反应速率为0.001 mol/(L・s)
B.将容器体积变为20 L,Z的平衡浓度变为原来的1/2
C.若增大压强,则物质Y的转化率减小
D.若升高温度,X的体积分数增大,则该反应的△H>0
2、选择题 对于可逆反应:C(s)+CO2(g) 2CO(g),在一定温度下其平衡常数为K。下列条件的变化中,能使K值发生变化的是(? )
2CO(g),在一定温度下其平衡常数为K。下列条件的变化中,能使K值发生变化的是(? )
A.将C(s)的表面积增大
B.增大体系的压强
C.升高体系的温度
D.使用合适的催化剂
3、选择题 同在室温下,同种规格的铝片分别与下列物质混合能放出H2,反应刚开始时化学反应速率最大的是( )
A.0.1?mol?L-1的盐酸15?mL
B.0.2?mol?L-1的盐酸5?mL
C.0.15?mol?L-1的硫酸溶液8?mL
D.18?mol?L-1的浓硫酸15?mL
4、选择题 把3 mol M和2.5 mol N混合于2 L的密闭容器中,发生反应的化学方程式为:
3M(g) + N(g) 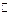 xP(g) + 2Q(g),5min后反应达到平衡,若反应前后温度不变,容器内压强变小,已知
xP(g) + 2Q(g),5min后反应达到平衡,若反应前后温度不变,容器内压强变小,已知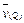 = 0.1mol・L-1・min-1,则下列说法错误的是(?)
= 0.1mol・L-1・min-1,则下列说法错误的是(?)
A.M的平均反应速率为0.15 mol・L-1・min-1
B.平衡时N的转化率为25%
C.平衡时P的浓度为0.25 mol・L-1
D.平衡时容器内的压强为原来的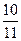 倍
倍
5、计算题 恒温下,将a?mol?N2与b?mol?H2的混合气体通入一个固定容积的密闭容器中,发生如下反应: N2(g)+3H2(g) 2NH3(g)
2NH3(g)
(1)若反应进行到某时刻t时,n(N2)=13?mol,n(NH3)= 6?mol,计算a的值。
(2)反应达到平衡时,混合气体的体积为716.8?L(标准状况下),其中NH3的含量(体积分数)为25%。计算平衡时NH3的物质的量。
(3)原混合气体与平衡混合气体的总物质的量之比(写出最简整数比,下同)n始:n平=
_________________。
(4)原混合气体中,a:b=_________。
(5)达到平衡时,N2和H2的转化率之比α(N2):α(H2)=________________。