1、填空题 (每空2分共10分)
I.在1L容器中通入CO2、H2各2mol,在一定条件下发生反应:CO2 + H2 CO + H2O,
CO + H2O,
回答下列问题:
(1)在830℃条件下,反应达到平衡时CO2的转化率为50%。若把体系温度降至800℃求得平衡常数K1=0.81,可以推知该反应的正反应为__________反应(填“吸热”、“放热”)。
(2)800℃时,某时刻测得体系中各物质的量如下:n(CO2)=1.2mol,n(H2)=1.5mol,n(CO)=0.9mol,n(H2O)=0.9mol,则此时该反应?进行.(填“向正反应方向”“向逆反应方向”或“处于平衡状态”)。
II.向一容积为1L的密闭容器中加入一定量的X、Y,发生化学反应X(g)+2Y(s)  2Z(g);△H<0。右图是容器中X、Z的物质的量浓度随时间变化的曲线。
2Z(g);△H<0。右图是容器中X、Z的物质的量浓度随时间变化的曲线。
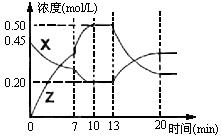
(1)0~10min 容器内气体的压强逐渐? ___________。(填“变大”、“变小”或“无法确定”)
(2)推测在第7min时曲线变化的原因可能是? ___第13min时曲线变化的原因可能是? __(填序号)
①增加Z的量? ②增加X的量? ③升温? ④降温? ⑤使用催化剂
参考答案:I.(1)?①?吸热?②?向正反应方向
II.(1)变大?(2)③⑤?(3)③
本题解析:I.(1)在830℃条件下,反应达到平衡时CO2的转化率为50%,则平衡时容器内物质的物质的量都是1mol,所以此时平衡常数是1。降低温度平衡常数减小,说明降低温度平衡向逆反应方向移动,所以正反应是吸热反应。
(2)因为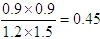 <0.81,所以向正反应方向进行。
<0.81,所以向正反应方向进行。
II.(1)根据图像可知,在0~10min时生成物的浓度增大,反应物的浓度减小,反应向正反应方向进行,即向体积增大的方向进行,所以压强增大。
(2)第7min时,物质的浓度变化程度变大,说明正逆反应速率都变大,所以答案只能是③⑤。
(3)第13min时,X的浓度增加,Z的浓度减小说明反应向逆反应方向减小。由于正反应是放热反应,所以是通过升高温度实现的。答案选③。
本题难度:一般
2、选择题 一定温度下,某反应达到平衡,平衡常数K= 。恒容时,温度升高,H2浓度增大。下列说法正确的是(?)
。恒容时,温度升高,H2浓度增大。下列说法正确的是(?)
A.该反应的化学方程式为CH3OH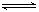 CO+2H2
CO+2H2
B.使用催化剂,H2浓度一定减小
C.升高温度,逆反应速率减小
D.该反应的焓变(ΔH)为负值
参考答案:D
本题解析:化学常数是在一定条件下的可逆反应中,当可逆反应反应达到平衡状态时,生成物浓度的幂之积和反应物浓度的幂之积的比值,所以根据平衡常数的表达式可知,该反应的方程式是CO+2H2 CH3OH,A不正确;催化剂不能影响平衡状态,B不正确;升高温度正逆反应速率都是增大的,C不正确;恒容时,温度升高,H2浓度增大,这说明升高温度平衡向逆反应方向移动,因此正反应是放热反应,答案选D。
CH3OH,A不正确;催化剂不能影响平衡状态,B不正确;升高温度正逆反应速率都是增大的,C不正确;恒容时,温度升高,H2浓度增大,这说明升高温度平衡向逆反应方向移动,因此正反应是放热反应,答案选D。
点评:本题容易错选C。平衡向逆反应方向移动,并不是因为逆反应速率减小,而是由于逆反应速率小于正反应速率引起的。
本题难度:一般
3、填空题 硫碘循环分解水制氢主要涉及下列反应:
I SO2+2H2O+I2=H2SO4+2HI
II 2HI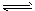 H2+I2
H2+I2
Ⅲ 2H2SO4=2SO2+O2+2H2O
(1)分析上述反应,下列判断正确的是____。
a.反应Ⅲ易在常温下进行
b.反应I中SO2氧化性比HI强
c.循环过程中需补充H2O
d.循环过程产生1molO2的同时产生1mol H2
(2)一定温度下,向1L密闭容器中加入1molHI(g),发生 反应II,H2物质的量随时间的变化如右图所示。0~2 min内的平均反应速率v(HI)=____。该温度下的平衡常数K=____ 相同温度下,若开始加入HI(g)的物质的量是原来的2倍,则___是原来的2倍。
a.平衡常数
b.HI的平衡浓度
c.达到平衡的时间
d.平衡时H2的体积分数

(3)实验室用Zn和稀硫酸制取H2,反应时溶液中水的电离平衡___移动(填 “向左”“向右”或“不”);若加入少量下列试剂中的____,产生H2的速率将增大。
a.NaNO3
b.CuSO4
c.Na2SO4
d.NaHSO3
(4)以H2为燃料可制作氢氧燃料电池。已知2H2(g)+O2(g) = 2H2O(1) △H=-572kJ・mol-1 某氢氧燃料电池释放228.8 kJ电能时,生成1mol液态水,该电池的能量转化率为________。
参考答案:(1)c
(2)0.1 mol.L-1・min-1 ;64;b
(3)向右;b 、f
(4)80%
本题解析:
本题难度:一般
4、填空题 反应A(g)+3B(g) 2C(g)+2D(g)在四种不同情况下的反应速率如下所示:
2C(g)+2D(g)在四种不同情况下的反应速率如下所示:
①v(A)= 0.15?mol/(L s);②v(B)=0.6mol/(L
s);②v(B)=0.6mol/(L s);③v(C)= 0.4?mol(L
s);③v(C)= 0.4?mol(L s);④v(D)=0.45?mol/(L
s);④v(D)=0.45?mol/(L s)。该反应进行的快慢顺序为_________。
s)。该反应进行的快慢顺序为_________。
参考答案:④>③=②>①
本题解析:
本题难度:一般
5、选择题 可逆反应2A+B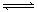 2C(g)(放热反应),随温度变化气体平均相对分子质量如图所示,则下列叙述正确的是
2C(g)(放热反应),随温度变化气体平均相对分子质量如图所示,则下列叙述正确的是
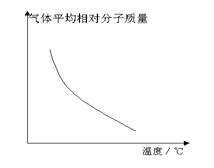
A.A和B可能都是固体
B.A和B一定都是气体
C.若B为固体,则A一定是气体
D.A和B可能都是气体
参考答案:CD
本题解析:略
本题难度:简单