1������� ��1����֪���ױȰ����ȶ�����֪��4P(���ף�s��+5O2��g����2P2O5��s�� ��H1��
4P�����ף�s��+5O2��g����2P2O5��s�� ��H2����H1�ͦ�H2�Ĺ�ϵ�ǡ�H1 ��H2���������������
��������
��2����֪H2��g����CH3OH��l����ȼ���ȡ�H�ֱ�Ϊ-285.8kJ��mol-1��-726.5kJ��mol-1��д����CO2
��H2����Һ̬�״���Һ̬ˮ���Ȼ�ѧ����ʽ ��
��3����֪һ���¶��£����з�Ӧ��ƽ�ⳣ����SO2(g)+1/2O2(g)  SO3(g) K1,CO(g)+1/2O2(g)
SO3(g) K1,CO(g)+1/2O2(g)
 CO2(g) K2������ͬ�¶��·�ӦSO2(g)+CO2(g)
CO2(g) K2������ͬ�¶��·�ӦSO2(g)+CO2(g)  SO3(g)+CO(g)��ƽ�ⳣ��Ϊ ��
SO3(g)+CO(g)��ƽ�ⳣ��Ϊ ��
����K1��K2��ʾ��
�ο��𰸣�����6�֣��� ��2��3H2(g)��CO2(g)��CH3OH��l��H2O(l) ��H����130.9 kJ/mol ��3��
�����������1�����ױȰ����ȶ�����˵���������������ڰ�����������������ת��Ϊ���������ȷ�Ӧ����H��0�����ݷ�Ӧ��4P(���ף�s��+5O2��g����2P2O5��s�� ��H1�͢�4P�����ף�s��+5O2��g����2P2O5��s�� ��H2�����ݸ�˹���ɿ�֪���ڣ��ټ��õ���Ӧ4P�����ף�s����4P(���ף�s������÷�Ӧ�ġ�H����H2����H1��0�����ԡ�H1����H2��
��2��H2��g����CH3OH��l����ȼ���ȡ�H�ֱ�Ϊ-285.8kJ��mol-1��-726.5kJ��mol-1�����з�Ӧ��H2(g)��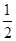 O2(g)��H2O(l) ��H����285.8kJ/mol����CH3OH��l����
O2(g)��H2O(l) ��H����285.8kJ/mol����CH3OH��l����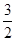 O2(g)��2H2O(l)��CO2(g) ��H����726.5kJ/mol������ݸ�˹���ɿ�֪���١�3���ڼ��õ���Ӧ3H2(g)��CO2(g)��CH3OH��l��H2O(l)����˸÷�Ӧ�ķ�Ӧ�ȡ�H����285.8kJ/mol��3��726.5kJ/mol����130.9 kJ/mol��
O2(g)��2H2O(l)��CO2(g) ��H����726.5kJ/mol������ݸ�˹���ɿ�֪���١�3���ڼ��õ���Ӧ3H2(g)��CO2(g)��CH3OH��l��H2O(l)����˸÷�Ӧ�ķ�Ӧ�ȡ�H����285.8kJ/mol��3��726.5kJ/mol����130.9 kJ/mol��
��3�����ݷ�Ӧ��SO2(g)+1/2O2(g)  SO3(g)����CO(g)+1/2O2(g)
SO3(g)����CO(g)+1/2O2(g) CO2(g)��֪���٣��ڼ��õ���ӦSO2(g)+CO2(g)
CO2(g)��֪���٣��ڼ��õ���ӦSO2(g)+CO2(g)  SO3(g)+CO(g)����������ͬ�¶��·�ӦSO2(g)+CO2(g)
SO3(g)+CO(g)����������ͬ�¶��·�ӦSO2(g)+CO2(g)  SO3(g)+CO(g)ƽ�ⳣ��K��
SO3(g)+CO(g)ƽ�ⳣ��K�� ��
��
���㣺���鷴Ӧ�ȵļ��㡢�Ȼ�ѧ����ʽ����д�Լ�ƽ�ⳣ���ļ����
�����Ѷȣ�һ��
2������� ��������������Ӧ����1 molˮ��������241.8kJ��д���÷�Ӧ���Ȼ�ѧ����ʽ��
��
��֪H2O(l) �� H2O (g) ��H �� ��44 kJ��mol��1�����״����33.6 L H2����Һ̬ˮʱ�ų��������� kJ ��
�ο��𰸣���1��H2(g)��1/2O2(g)===H2O(g)����H��-241.8 kJ/mol ��2��428.25kJ
���������������������Ӧ����1 molˮ��������241.8kJ�����Ը÷�Ӧ���Ȼ�ѧ����ʽ��H2(g)��1/2O2(g)��H2O(g) ��H����241.8 kJ/mol����֪H2O(l) �� H2O (g) ��H �� ��44 kJ/mol������ݸ�˹���ɿ�֪��H2(g)��1/2O2(g)��H2O(l) ��H����285.8 kJ/mol����״����33.6 L H2�����ʵ�����1.5mol����������Һ̬ˮʱ�ų���������285.8 kJ/mol��1.5mol��428.25kJ��
���㣺���鷴Ӧ�ȵļ�����Ȼ�ѧ����ʽ����д
�����������ǻ���������Ŀ��飬���ض�ѧ��������û���֪ʶ���ʵ�����������������������ѧ������˼ά�����淶�Ĵ����������ѶȲ���
�����Ѷȣ�һ��
3��ѡ���� �����кͷ�Ӧ�Ȼ�ѧ����ʽ���ã�H+��aq��+OH-��aq��=H2O��l����H=-57.3kJ?mol-1����ʾ���ǣ� ? ��
A��CH3COOH��aq��+NaOH��aq��=CH3COONa��aq��+H2O��l������H=-Q1?kJ?mol-1
B��
 H2SO4��Ũ��+NaOH��aq��=1/2Na2SO4��aq��+H2O��l������H=-Q2?kJ?mol-1
H2SO4��Ũ��+NaOH��aq��=1/2Na2SO4��aq��+H2O��l������H=-Q2?kJ?mol-1
C��HNO3��aq��+NaOH��aq��=NaNO3��aq��+H2O��l������H=-Q3?kJ?mol-1
D��
 H2SO4?��aq��+
H2SO4?��aq��+ Ba��OH��2��aq��=
Ba��OH��2��aq��= BaSO4?��s��+H2O��l������H=-Q4?kJ?mol-1
BaSO4?��s��+H2O��l������H=-Q4?kJ?mol-1
�ο��𰸣�C
���������
�����Ѷȣ�һ��
4��ѡ���� ��֪��������ˮʱ����Һ�¶Ƚ��͡��������½�1mol��ˮ����ͭ�Ƴ���Һʱ���ų�����ΪQ1kJ���������ֽ���Ȼ�ѧ����ʽ��CuSO4��5H2O(s)��CuSO4(s)��5H2O(l)����H����Q2kJ/mol����Q1��Q2�Ĺ�ϵ��
[? ]
A��Q1��Q2
B��Q1��Q2
C��Q1��Q2
D����ȷ��
�ο��𰸣�C
���������
�����Ѷȣ�һ��
5������� ���Ȼ��ѣ�TiCl4������ȡ���캽�չ�ҵ����--�ѺϽ����Ҫԭ�ϣ�����������Ҫ�ɷ���FeTiO3���Ʊ�TiCl4�Ȳ�Ʒ��һ�ֹ�������ʾ�����£�

�ش��������⣺
��1�������м�����м������Һ����ɫ����ʱ��Һ�Գ�ǿ���ԣ��ù����������·�Ӧ������
2Fe3++Fe�T3Fe2+
2TiO2+����ɫ��+Fe+4H+�T2Ti3+����ɫ��+Fe2++2H2O
Ti3+����ɫ��+Fe3++H2O�TTiO2+����ɫ��+Fe2++2H+
�������������______��
��2���ڢڡ��۹�������Ҫ�����������γ�TiO2?nH2O�ܽ����÷�ɢ�ʿ���ֱ����С��______��Χ��
��3�����Ѣ����ƵõĹ���TiO2?nH2O������ϴ��ȥ���е�Fe��OH��3���ʣ������Ƶ��Ѱۣ���֪25��ʱ��Ksp[Fe��OH��3]=2.79��10-39�����¶��·�ӦFe��OH��3+3H+?Fe3++H2O��ƽ�ⳣ��K=______��
��4����֪��TiO2��s��+2Cl2��g���TTiCl4��l��+O2��g����H=+140kJ?mol-1��2C��s��+O2��g���T2CO��g����H=-221kJ?mol-1
д������TiO2�ͽ�̿��������Ӧ����Һ̬TiCl4��CO������Ȼ�ѧ����ʽ��______��
��5���������վ��гɱ��͡����õ�Ʒλ����Ϊԭ�ϵ��ŵ㣮������ɫ��ѧ����ù��������д��ڵIJ���֮����______��ֻҪ��д��һ���
��6�����������Ϣ��Ҫ���ƺ�����SiCl4���ʵ�TiCl4���ɲ���______������
| TiCl4 | SiCl4
�۵�/��
-25.0
-68.8
�е�/��
136.4
57.6
�ο��𰸣���1�������м�����м������Һ����ɫ��˵������Һ�к���Ti3+���ɷ���ʽ��֪��Fe3+����ΪTi3+��������м����ԭ������Fe3+��ԭΪFe2+����ֹTi3+��Fe3+������TiO2+��
�ʴ�Ϊ����ֹTi3+��Fe3+������TiO2+��
��2�������������γ�TiO2?n H2O�ܽ���˵���õ����壬���ɢ�ʿ���ֱ����СΪ10-9��10-7m����1nm-100nm����
�ʴ�Ϊ��10-9��10-7m����1nm-100nm����
��3��Ksp[Fe��OH��3]=c��Fe3+����c3��OH-��=2.79��10-39����ӦFe ��OH��3+3H+?Fe3++H2O��ƽ�ⳣ��K=c(Fe3+)c3(H+)=c(Fe3+)(10-14c(OH-))3=c��Fe3+����c3��OH-����1042=2.79��10-39��1042=2.79��103��
�ʴ�Ϊ��2.79��103��
��4����TiO2 ��s��+2Cl2 ��g���TTiCl4��l��+O2��g����H=+140KJ?mol-1
��2C��s��+O2��g���T2CO��g����H=-221KJ?mol-1
���ݸ�˹���ɢ�+�ڵõ���TiO2��s��+2C��s��+2Cl2 ��g��=TiCl4��l��+2CO��g����H=-81KJ?mol-1��
�ʴ�Ϊ��TiO2��s��+2C��s��+2Cl2 ��g��=TiCl4��l��+2CO��g����H=-81KJ?mol-1
��5���ɹ������̿�֪�������в�����������Һ�������ȣ���������ɫ��ѧ���
�ʴ�Ϊ�������˷�������Һ�������ȣ�
��6���ɱ������ݿ�֪��SiCl4��TiCl4ΪҺ�壬���߷е����ϴ�Ҫ���ƺ�����SiCl4���ʵ�TiCl4���ɲ��������������
�ʴ�Ϊ���������
���������
�����Ѷȣ�һ��
|