1ЎўСЎФсМв ПВБРУР№ШИИ»ҜС§·ҪіМКҪөДұнКҫј°Лө·ЁХэИ·өДКЗЈЁЎЎЎЎЈ©
AЈ®ТСЦӘcЈЁКҜД«Ј¬sЈ©=cЈЁҪрёХКҜЈ¬sЈ©ЎчHЈҫ0Ј¬ФтҪрёХКҜұИКҜД«ОИ¶Ё
BЈ®ТСЦӘH2ЈЁgЈ©+F2ЈЁgЈ©ЁT2HFЈЁgЈ©ЎчH=-270kJ/molЈ¬Фт2L·ъ»ҜЗвЖшМе·ЦҪвіЙ1LЗвЖшәН1L·ъЖшОьКХ270kJИИБҝ
CЈ®HClәНNaOH·ҙУҰөДЦРәНИИОӘ-57.3kJ/molЈ¬ФтH2SO4әНBaЈЁoHЈ©2·ҙУҰөДЦРәНИИЎчH=2ЎБЈЁ-57.3Ј©kJ/mol
DЈ®ТСЦӘI2ЈЁgЈ©+H2ЈЁgЈ©ЁT2HIЈЁgЈ©ЎчH1Ј»I2ЈЁsЈ©+H2ЈЁgЈ©ЁT2HIЈЁgЈ©ЎчH2Ј»ФтЎчH1ЈјЎчH2
2ЎўМоҝХМв (15·Ц)ДЬФҙөДҝӘ·ўЎўАыУГУлИЛАаЙз»бөДҝЙіЦРш·ўХ№ПўПўПа№ШЈ¬ФхСщід·ЦАыУГәГДЬФҙКЗ°ЪФЪИЛАаГжЗ°өДЦШҙуҝОМвЎЈ
IЈ®ТСЦӘЈәFe2O3(s)+3C(КҜД«) =2Fe(s)+3CO(g) ЎчH=akJЎӨmol-1
CO(g)+1ЈҜ2O2(g)= CO2(g) ЎчH=bkJЎӨmol-1
C(КҜД«)+O2(g)=CO2(g) ЎчH=ckJЎӨmol-1
Фт·ҙУҰЈә4Fe(s)+3O2(g)= 2Fe2O3(s)өДмКұдЎчH= kJЎӨmol-1ЎЈ
ўтЈ®ЈЁ1Ј©ТАҫЭФӯөзіШөД№№іЙФӯАнЈ¬ПВБР»ҜС§·ҙУҰФЪАнВЫЙПҝЙТФЙијЖіЙФӯөзіШөДКЗ (МоРтәЕ)ЎЈ
AЈ®C(s)+CO2(g)=2CO(g)
BЈ®NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l)
CЈ®2H2O(l)= 2H2(g)+O2(g)
DЈ®CH4(g)+2O2(g)=CO2(g)+2H2O(l)
ИфТФKOHИЬТәОӘөзҪвЦКИЬТәЈ¬ТАҫЭЛщСЎ·ҙУҰҝЙТФЙијЖіЙТ»ёцФӯөзіШЈ¬ЗлРҙіцёГФӯөзіШөДөзј«·ҙУҰЎЈ
ёәј«Јә Ј¬
Хэј«Јә ЎЈ
ЈЁ2Ј©¶юСх»ҜВИ(ClO2)КЗТ»ЦЦёЯР§°ІИ«өДЧФАҙЛ®Пы¶ҫјБЎЈClO2КЗТ»ЦЦ»ЖВМЙ«ЖшМеЈ¬ТЧИЬУЪЛ®ЎЈКөСйКТТФNH4ClЎўСОЛбЎўNaClO2ОӘФӯБПЦЖұёClO2БчіМИзПВЈә
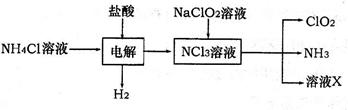
ТСЦӘЈәөзҪв№эіМЦР·ўЙъөД·ҙУҰОӘЈә
NH4Cl+2HCl NCl3+3H2ЎьЈ»јЩЙиNCl3ЦРөӘФӘЛШОӘ+3јЫЎЈ
NCl3+3H2ЎьЈ»јЩЙиNCl3ЦРөӘФӘЛШОӘ+3јЫЎЈ
ўЩРҙіцөзҪвКұТхј«өДөзј«·ҙУҰКҪ ЎЈ
ўЪФЪСфј«ЙП·ЕөзөДОпЦК(»тАлЧУ)КЗ ЎЈ
ўЫіэИҘClO2ЦРөДNH3ҝЙСЎУГөДКФјБКЗ (МоРтәЕ)
AЈ®ЙъКҜ»Т BЈ®јоКҜ»Т CЈ®ЕЁH2SO4 DЈ®Л®
ўЬФЪЙъІъ№эіМЦРЈ¬ГҝЙъіЙ1mol ClO2Ј¬РиПыәД mol NCl3ЎЈ
3ЎўМоҝХМв (8·Ц)
IТСЦӘ2H2(g)+O2(g)=2H2O(g) ЎчH=-483Ј®6 kJЈҜmol
2H2(g)+O2(g)=2H2O(l) ЎчH=-571Ј®6 kJЈҜmol
(1)ЗвЖшөДИјЙХИИЎчH= kJЈҜmol
(2)ИјЙХ2gH2ЙъіЙЛ®ХфЖшЈ¬·ЕіцөДИИБҝОӘ kJЎЈ
ўт°СГәЧчОӘИјБПҝЙНЁ№эПВБРБҪЦЦНҫҫ¶»сөГИИБҝЈә
Нҫҫ¶1ЈәЦұҪУИјЙХ
C(s)+O2(g)=CO2(g) ЎчH=E1 ўЩ
Нҫҫ¶2ЈәПИЦЖіЙЛ®ГәЖшЈ¬ФЩИјЙХЛ®ГәЖш
C(s)+H2O(g)=CO(g)+H2(g) ЎчH=E2 ўЪ
H2(g)+1ЈҜ2 O2(g)=H2O(g) ЎчH=E3 ўЫ
CO(g)+1ЈҜ2 O2(g)=CO2(g) ЎчH=E4 ўЬ
Зл»ШҙрЈә
(1)ЙПКцЛДёцИИ»ҜС§·ҪіМКҪЦРДДёц·ҙУҰЎчH >0? (МоРтәЕ)
(2)өИЦКБҝөДГә·ЦұрНЁ№эТФЙПБҪМхІ»Н¬өДНҫҫ¶ІъЙъөДҝЙАыУГөДЧЬДЬБҝ№ШПөХэИ·өДКЗ
(МоСЎПоЧЦДё)ЎЈ
AЈ®Нҫҫ¶1ұИНҫҫ¶2¶а BЈ®Нҫҫ¶1ұИНҫҫ¶2ЙЩ CЈ®Нҫҫ¶1УлНҫҫ¶2ФЪАнВЫЙППаН¬
(3)ёщҫЭДЬБҝКШәг¶ЁВЙЈ¬E1ЎўE2ЎўE3ЎўE4Ц®јдөД№ШПөОӘ Ј®
4ЎўСЎФсМв ПВұнЦРЈ¬¶ФУР№ШАлЧУ·ҪіМКҪ»тИИ»ҜС§·ҪіМКҪөДЖАјЫәПАнөДКЗ
[? ]