1、填空题 某化学小组进行Na2SO3的性质实验探究。
在白色点滴板的a、b、c三个凹槽中滴有Na2SO3溶液,再分别滴加下图所示的试剂:
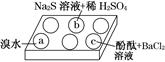
实验现象如下表:
编号
| 实验现象
|
a
| 溴水褪色
|
b
| 产生淡黄色沉淀
|
c
| 滴入酚酞溶液变红,再加入BaCl2溶液后产生沉淀且红色褪去
|
?
根据实验现象进行分析:
(1)a中实验现象证明Na2SO3具有________性。
(2)b中发生反应的离子方程式是_____________________________________________
(3)应用化学平衡原理解释c中现象(用化学用语及简单文字表述)__________________________________________________________。
参考答案:(1)还原性 (2)SO32-+2S2-+6H+=3S↓+3H2O
(3)在Na2SO3溶液中,SO32-水解显碱性:SO32-+H2O HSO3-+OH-,所以滴入酚酞后溶液变红;在该溶液中加入 BaCl2后,Ba2++SO32-=BaSO3↓(白色),由于c(SO32-)减小,SO32-水解平衡左移,c(OH-)减小,红色褪去。
HSO3-+OH-,所以滴入酚酞后溶液变红;在该溶液中加入 BaCl2后,Ba2++SO32-=BaSO3↓(白色),由于c(SO32-)减小,SO32-水解平衡左移,c(OH-)减小,红色褪去。
本题解析:(1)a中发生反应的化学方程式为:Na2SO3+Br2+H2O=Na2SO4+2HBr,证明Na2SO3具有还原性。
(2)b中产生淡黄色沉淀,发生反应的离子方程式是SO32-+2S2-+6H+=3S↓+3H2O。
(3)滴入酚酞溶液变红是因为SO32-发生了水解反应而使溶液显碱性:SO32-+H2O?HSO3-+OH-,再加入BaCl2溶液后,Ba2+与SO32-反应产生BaSO3沉淀,反应消耗了SO32-使其浓度减小,水解平衡向左移动,OH-浓度减小,红色褪去。
本题难度:一般
2、选择题 在通常状况下,A是固体单质。根据如图所示的转化关系,回答:

(1)写出A、E的化学式:A__________;E__________。
(2)写出指定反应的化学方程式:
E→C:____________________________________________________________。
C→D:____________________________________________________________。
(3)若A为气态单质,则A、E的化学式:A__________;E__________。
参考答案:(1)S? H2SO4
(2)Cu+2H2SO4(浓)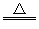 CuSO4+SO2↑+2H2O
CuSO4+SO2↑+2H2O
2SO2+O2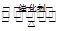 2SO3
2SO3
(3)N2?HNO3
本题解析:A是固体单质,由图知A能与H2反应,所以它应是一种非金属单质;A及其氢化物B能连续与O2反应,最终生成的氧化物D能够与水反应生成含氧酸E,而E能够与Cu反应生成C,所以E应是一种强氧化性酸,故可知A是硫。若A为气态单质,由转化关系可知,A~E分别为N2、NH3、NO、NO2、HNO3。
本题难度:一般
3、选择题 下列能说明R元素一定为氧族元素的是(? )
A.R为非金属元素,其氧化物的化学式为XO2
B.R的氢化物中,R原子与氢原子的个数之比为1∶1
C.R的单质与金属铝能化合生成Al2R3
D.R的氢化物的水溶液呈酸性
参考答案:C
本题解析:氧化物的化学式为XO2的元素除了氧族元素外,还有CO2、SiO2等,A项错误;B项H2O2符合条件,HCl等也符合条件;C项Al2R3中R元素的最低化合价为-2,只有氧族元素才具有;D项如卤化氢的水溶液也显酸性,但它们都不是氧族元素。
本题难度:简单
4、选择题 下列关于浓硫酸和稀硫酸的叙述中,正确的是
A.常温时都能与铁发生反应,放出气体
B.加热时都能与铜发生反应
C.硫元素的化合价都是+6价
D.都能作为气体的干燥剂
参考答案:C
本题解析:常温下铁在浓硫酸中发生钝化,A不正确;稀硫酸和铜不反应,B不正确;稀硫酸不能作为干燥剂,D不正确,答案选C。
点评:该题是基础性试题的考查,也是高考中的常见考点。试题基础性强,难度不大,侧重对学生基础知识的巩固和训练,有利于调动学生的学习兴趣和学习积极性。
本题难度:简单
5、选择题 下列物质①NaOH、②氯水、③空气、④氢硫酸、⑤Na2SO3、⑥Na2CO3,其中能与SO2在一定条件下发生反应的是(? )
A.①②④⑤
B.②④⑤⑥
C.②③④⑤
D.全部
参考答案:D
本题解析:①SO2+2NaOH Na2SO3+H2O或NaOH+SO2
Na2SO3+H2O或NaOH+SO2 NaHSO3?②Cl2+SO2+2H2O
NaHSO3?②Cl2+SO2+2H2O H2SO4+2HCl?③2SO2+O2
H2SO4+2HCl?③2SO2+O2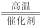 2SO3?④2H2S+SO2
2SO3?④2H2S+SO2 3S↓+2H2O?⑤Na2SO3+SO2+H2O
3S↓+2H2O?⑤Na2SO3+SO2+H2O 2NaHSO3?⑥Na2CO3+SO2
2NaHSO3?⑥Na2CO3+SO2 Na2SO3+CO2。
Na2SO3+CO2。
本题难度:简单