1、选择题 飘尘是物质燃烧时产生的颗粒状漂浮物,颗粒很小,不易沉降。它与空气中的SO2、O2接触时会部分转化为SO3,,使空气的酸度增加。飘尘所起的作用是 (?)
A?氧化剂? B 还原剂? C 催化剂? D吸附剂?
2、填空题 有一纯净的亚硫酸钠晶体因部分被氧化而变质,为了测定样品中杂质的质量分数进行以下实验过程,按要求填写空格:
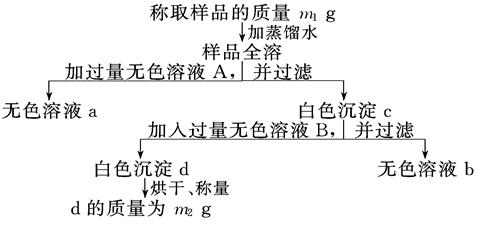
(1)向混合溶液中加入的无色溶液A是____________(填化学式),A必须过量的原因是
________________________________________________________________________.
(2)白色沉淀c中含有____________________(填化学式).
(3)无色溶液B通常是_____________(填试剂名称),加入后与c反应的离子方程式为
________________________________________________________________________.
(4)通过以上测定可得到样品中杂质的质量分数的计算式为_______________________.
3、实验题 碳跟浓硫酸共热产生的气体X和铜跟浓硝酸反应产生的气体Y同时通入盛有足量氯化钡溶液的洗气瓶中(如图装置)
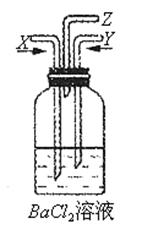
请回答下列问题。
(1)气体X的主要成分有______ ______。(写化学式)
______。(写化学式)
(2)洗 气瓶中的反应现象为_____________。用文字简要解释产生上述实验现象的原因:_______________________。
气瓶中的反应现象为_____________。用文字简要解释产生上述实验现象的原因:_______________________。
(3)管口Z处的现象是_________________,产生此现象的原因是_______________。(用化学方程式表示)
4、计算题 煤是重要的化工原料,用煤作燃料,不仅存在浪费,而且因烟煤中含有硫的化合物(如FeS2),燃烧时会生成SO2气体造成环境污染。
设某具有30万户人口的中等城市,每户每天燃煤5 kg,这种煤中含FeS2 5%,燃烧时,设有90%的硫转化成二氧化硫,被排放到大气中。FeS2燃烧时化学方程式如下:
4FeS2+11O2 2Fe2O3+8SO2
2Fe2O3+8SO2
问:(1)燃烧1 t煤,可产生多少千克的SO2?
(2)该中等城市如果全部以上述的煤作燃料,每年(按365天计算)将有多少吨SO2排放到大气中?
5、填空题 浓硫酸和碳在加热的情况下反应的化学方程式为C+2H2SO4=CO2↑+2SO2↑+2H2O为了验证反应的各种生成物,用如图Ⅰ装置进行实验。
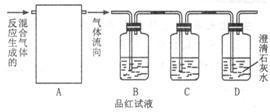
图Ⅰ
(1)图Ⅰ中A处是完成实验中的必要装置,它是下列图Ⅱ所示中的(填编号)_________;
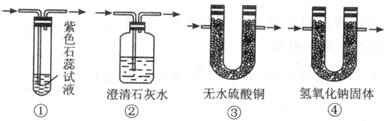
图 Ⅱ
(2)C装置中应盛的试剂为足够_______________,其作用__________;
(3)能够确定存在二氧化碳气体的实验现象_______________________。