1������� (13��)��1��A��B��DΪ������Ԫ�أ��������Ϣ�ش����⣺
Ԫ��
| A
| B
| D
|
���ʻ�ṹ��Ϣ
| ��ҵ��ͨ������Һ̬��������䵥�ʣ���������ȼ
| ��̬�⻯���ˮ��Һ�Լ���
| ԭ�����������Ӳ㣬�������ڱ������а뾶��С
|
�ٵ�һ�����ܣ�A?B���>��������������<��������̬Dԭ�ӵĵ����Ų�ʽΪ?��
��B��D�ɹ��ۼ��γɵ�ij������BD��2200�濪ʼ�ֽ⣬BD�ľ�������Ϊ?��
��2����չú��Һ�����������롰ʮ����滮�����п�Ժɽ��ú��������úҺ�������ĸ�Ч�����з���Ŀȡ�û�����չ����֪��ú������ת��Ϊһ����̼�����������ڴ��������ºϳɼ״���CH3OH��,�Ӷ�ʵ��Һ����
��ij��ͭ���ӵ����ӽṹ����ͼ��ʾ��
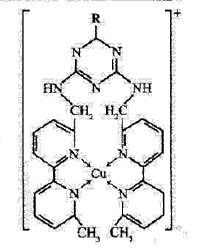
�ڸ������ڲ������������������У�?������ĸ����
A�����Ӽ�? B.���Լ� C.�Ǽ��Լ�? D.��λ��? E.���»���? F.���
��úҺ����ü״�,�پ����õ���Ҫ��ҵԭ�ϼ�ȩ(HCHO)���״��ķе�Ϊ65�棬��ȩ�ķе�Ϊ��21�棬���߾�������ˮ���״��ķе�ȼ�ȩ������Ϊ�״����Ӽ���������������ȩ���Ӽ�û��������״��ͼ�ȩ������ˮ������Ϊ���Ǿ����Ժ�ˮ�γɷ��Ӽ����������˵����ȩ���Ӽ�û�������ԭ����?��
�ۼ״������У�����sp3�ӻ���ԭ����?����ȩ��H2�����ӳɷ�Ӧ��������1mol�״�ʱ�����ѵġǼ�����ĿΪ?
�ο��𰸣���1���� < (1��) ��1s22s22p63s23p1 (2��) ��ԭ�Ӿ��� (2��)
��2���� B��C��D ��F(2��)
�ڼ�ȩ��������ԭ����̼ԭ���γɹ��ۼ���̼�ĵ縺�Խ�С���������γ���������������ȩ�����е��ⲻ�����á������Ե����Եȣ���(2��)
��C��O (2��) NA (2��)
�����������1������������ȼ�������������A��O���⻯��ˮ��Һ�Լ��Ե��ǰ�������B��N��D��3�����Ӳ㣬���ڵ������ڣ����Ӱ뾶��С������D��Al����ԭ�ӵ�2p����ǰ�����ģ��ȶ���ǿ�����Ե�һ�����ܴ�����ԭ�ӵġ�����ԭ��������13�����ݹ���ԭ����֪��̬���ӵ��Ų�ʽΪ1s22s22p63s23p1��AlN���۵�ܸߣ������ɹ��ۼ����ɵģ��������ԭ�Ӿ��塣
��2�����ݽṹʾ��ͼ���жϣ����͵�֮�䡢̼��̼֮���γɷǼ��Լ�������̼֮���γɼ��Լ�������Ϊ��ԭ�Ӻ��йµ��Ӷԣ����Ժ�ͭ�γ���λ����ͬʱ��ԭ��Ҳ���Ժ���ԭ���γ���������Դ���BCDF���ڼ�ȩ����ԭ�Ӻ�̼ԭ���γɼ��Լ�C��H����������̼�ķǽ����ԱȽ��������縺��С�������γɵļ��Լ��ļ��Բ���ǿ����˲����γ�����������ĵ縺�Դ�O��H�ļ��Դ������γ�������״��Ľṹ��ʽΪCH3OH���ṹʽΪ ������̼ԭ�Ӻ���ԭ�Ӳ�ȡ����sp3�ӻ�����ȩ�������ӳɵı�����̼��˫���ϼ���Ȼ��̼�����ֱ�������ԭ�ӣ����Զ��ѵĦм���1mol��
������̼ԭ�Ӻ���ԭ�Ӳ�ȡ����sp3�ӻ�����ȩ�������ӳɵı�����̼��˫���ϼ���Ȼ��̼�����ֱ�������ԭ�ӣ����Զ��ѵĦм���1mol��
�����Ѷȣ�һ��
2��ѡ���� ��aAm����bBn���ĺ�������Ų���ͬ�������й�ϵ����ȷ����(����)
A��b��a��n��m
B�����Ӱ뾶Am��<Bn��
C��ԭ�Ӱ뾶A<B
D��A��ԭ��������B��(m��n)
�ο��𰸣�C
���������aAm����bBn���ĺ�������Ų���ͬ��˵��������������ȣ�����a��m��b��n��A��ȷ����������Ų���ͬ�����������뾶��˵�������������С��B��ȷ��B���ڷǽ�����A���ڽ�����Aλ��B����һ���ڣ���ԭ�Ӱ뾶����B�ģ�C����ȷ����a��m��b��n�ɵ�a��b��m��n��D��ȷ��
�����Ѷȣ�һ��
3��ѡ���� ��48?mL?0.1?mol/L��FeSO4��Һ��ǡ�û�ԭ2.4��10-3?mol[RO(OH)2]+���ӣ���RԪ�ص����ռ�̬Ϊ?
[? ]
A��+2��?
B��+3��
C��+4��?
D��+5��
�ο��𰸣�B
���������
�����Ѷȣ���
4��ѡ���� 374�桢22.1Mpa���ϵij��ٽ�ˮ���к�ǿ���ܽ��л���������������н϶��H+��OH�C���ɴ˿�֪���ٽ�ˮ
A�������ԣ�pH����7
B�����ֳ��Ǽ����ܼ�������
C�������ԣ�pHС��7
D�����ֳ������ܼ�������
�ο��𰸣�B
������������ٽ������϶��H+��OH�C����Ũ�ȴ��ڳ�����ˮ�е�H+��OH�C��pH��7������ʱˮ��c(H+)��c(OH�C)��ȣ��ʸ�ˮ�����ԣ����á���������ԭ������������С����ٽ�ˮ���к�ǿ���ܽ��л������������֪���ٽ�ˮ���ֳ��Ǽ����ܼ������ԡ�
�����Ѷȣ�һ��
5��ѡ���� ���и��������б�ֵ��Ϊ1��2����
A��������C��C�ļ�������ϩ��C��C�ļ���֮��
B�����ʯ������̼ԭ�Ӹ�����C��C���ۼ�����֮��
C��Al��̬ԭ�Ӻ��������P�����S���������֮��
D��̼��̬ԭ�Ӻ���δ�ɶԵ������ͳɶԵ�����֮��
�ο��𰸣�A
���������
�𰸣�A
A����ȷ��˫������һ���ģ�һ���Ǽ������ܲ��ǵ����ܵĶ�����
�����Ѷȣ�һ��