1、选择题 下列有关实验可行的是()
①可用倒扣在NaOH溶液上面的漏斗装置吸收残余的Cl2②混入KI溶液中的KHCO3可滴加盐酸除去③碘升华形成的污迹可用热的浓盐酸洗去④制Cl2后的黑褐色污迹可用热的浓盐酸洗去
A.①②
B.②③
C.③④
D.①④
2、选择题 在室温时,下列各组中的物质分别与过量NaOH溶液反应,能生成3种盐的一组是
[?]
A.SO2、CO2
B.C12、A12O3
C.CO2、SO3
D.SiO2、CO2
3、实验题 某研究性学习小组欲利用已经学过的化学知识和下列装置制取少量次氯酸钠,并进一步探究次氯酸钠的化学性质。
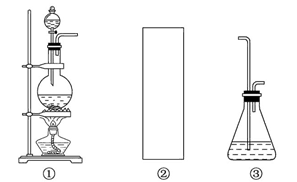
相关资料:反应Cl2+2NaOH=NaClO+NaCl+H2O属于放热反应,温度稍高时便发生副反应:3Cl2+6NaOH=NaClO3+5NaCl+3H2O。
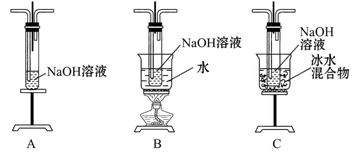
(1)制取氯气时,在烧瓶中加入一定量的二氧化锰,通过________(填写仪器名称)向烧瓶中加入适量的浓盐酸。请在装置A、B、C中选择一个合适的装置放在②处________。
(2)部分学生认为上述装置存在缺点,他们指出在前两个仪器之间应增加如D图所示的装置:你认为D中所盛液体是________,其作用是____________。

(3)该化学兴趣小组对产品的性质进行了如下探究。
第一步,测其pH=10。结合相关离子方程式解释原因________。
第二步,该化学兴趣小组的同学备选了紫色石蕊试液对次氯酸钠的性质进行实验检验。请你帮助他们完成实验报告:
?
4、填空题 硫酸、硝酸和盐酸既是重要的化工原料也是化学实验室里必备的试剂。
(1)常温下,可用铝槽车装运浓硫酸,这是因为浓硫酸具有?性;硝酸应保存在棕色试剂瓶中,这是因为硝酸具有?性;敞口放置的浓盐酸浓度会减小,这是因为盐酸具有?性。
(2)①在100 mL 18 mol・L-1的浓硫酸中加入过量的铜片,加热使之充分反应,产生的气体在标准状况下的体积为13.44 L,则参加反应的铜片的质量为?(选填序号);
a.115.2 g? b.76.8 g? c.57.6 g? d.38.4 g
②若使上述①中反应剩余的铜片继续溶解,可向其中加入硝酸钠,写出反应的离子方程式:?。
(3)工业制盐酸是以电解饱和氯化钠溶液为基础进行的,该电解过程中阳极的电极反应式为:?。
5、选择题 下列说法中正确的是
A.硅主要以单质、氧化物、硅酸盐的形式存在于自然界中
B.青铜是我国使用最早的合金,钢是用量最大、用途最广泛的合金
C.铁容器可以盛放浓盐酸、浓硝酸、浓硫酸
D.漂白粉、漂粉精可用来漂白棉、麻、纸张,不能用作游泳池及环境的消毒剂