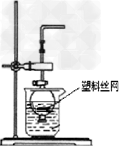
1��ѡ���� �÷�Һ©�����ձ�����װ���һ���ģ����濪���á������ͣ�����巢��װ�ã���ͼ��ʾ�����ô�װ���Ʊ���������
[? ]
A.?�ÿ�״����ʯ��ϡ���ᷴӦ��ȡCO2?
B.?��п����ϡ���ᷴӦ��ȡH2
C.?�ù���������ˮ��Ӧ��ȡO2
D.?�ö���������Ũ���ᷴӦ��ȡCl2
�ο��𰸣�B
���������
�����Ѷȣ�һ��
2��ʵ���� ����ͼ��ʾװ�ã��г�����ʡ�ԣ�����ʵ�飬��Һ��A�������B�С��ش��������⣺
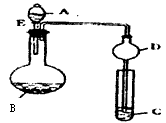
��1��ͼ��Dװ����ʵ���е�����____________________________ ��
��2����AΪŨ���ᣬBΪ������أ�C��ʢ��KI������Һ������E��C�е���������Һ����ɫ����д��A��B��Ӧ�Ļ�ѧ����ʽ��____________________________________ ��
��3����AΪŨ��ˮ��BΪ��ʯ�ң�C��ʢ�� ��Һ������E�㹻����ʱ���C�е�������_________________ ��C�з�����Ӧ�Ļ�ѧ����ʽΪ��________________________��
��Һ������E�㹻����ʱ���C�е�������_________________ ��C�з�����Ӧ�Ļ�ѧ����ʽΪ��________________________��
��4������ͼʾװ���ж�����;�����һ����������֮�⣩��գ�AΪ_______ ��BΪ___________ ��C��ʢ��______________ ����Ŀ��Ϊ____________________________________ ��
�ο��𰸣���1����ֹ����
��2��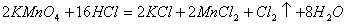
��3��������ɫ������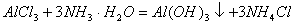
��4��ϡ���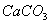 ������ʯ��ˮ����֤
������ʯ��ˮ����֤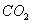 ���壨�����
���壨�����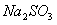 ��Ʒ����Һ����֤
��Ʒ����Һ����֤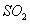 ��Ư���ԣ����𰸺������ɣ�
��Ư���ԣ����𰸺������ɣ�
���������
�����Ѷȣ�һ��
3��ѡ���� ijͬѧ������װ���Ʊ�������Cl2�����ʡ�����˵��������ǣ� ? ��
A��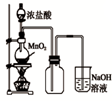
��ͼ�У���ʹMnO2����������Ҳ����ȫ������
B��
��ͼ�У�ʪ�����ɫ��������ɫ����������Һ�����ձ��У�����Һ�����ԣ������Cl2����
C��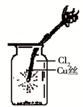
��ͼ�У�������ɫ����
D��
��ͼ�У�ˮ���Գ����Թ�
�ο��𰸣�D
���������
�����Ѷȣ�һ��
4������� ijУ��ѧ��ȤС���ڼ������������ö���������Ũ���ᷴӦ����ȡ���ռ�������
��1��д���÷�Ӧ�����ӷ���ʽ______��
��2����Ҫ��ȡ���������������Ӧʹ��������ͨ��װ��______��______��ϴ��ƿ��
��3����С���ȡ8.7g��������������10mol?L-1��Ũ���ᷴӦ�������Ͽ��Ƶ��������������״����V1=______L��
��4������С����ȡ��10mol?L-1��Ũ����40mL���������Ķ������̷�Ӧ�������ϲ������������ΪV2����״��������V1______V2���=������������������������ԭ����______��������װ�õ������Լ�Ũ����Ļӷ�����
�ο��𰸣���1������������Ũ�����ڼ��������·�Ӧ�����Ȼ��̡�ˮ����������������塢�������д��ѧʽ�������Ե�ǿ�����д����ʽ����Ӧ�����ӷ���ʽΪMnO2+4H++2C1-?��?.?Mn2++Cl2��+2H2O��
�ʴ�Ϊ��MnO2+4H++2C1-?��?.?Mn2++Cl2��+2H2O��
��2��Ũ�����лӷ��ԣ�Ũ���ᡢˮ�ڼ���ʱ��������壬���������к����Ȼ��⡢ˮ�������Ȼ��⼫������ˮ���ұ���ʳ��ˮ�к��������ӣ������������ܽ⣬���Ա���ʳ��ˮ�������������Ȼ������壻Ũ��������ˮ�ԣ������������dz�ˮ������
�ʴ�Ϊ������ʳ��ˮ��Ũ���
��3���������Ͽ��Ƶ��������������״����V1��
MnO2+4H++2Cl-?��?.?MnCl2+2H2O+Cl2��
87g? 22.4L?
8.7g? V1
���� V1=2.24?L
�ʴ�Ϊ��2.24��
��4��10mol?L-1��Ũ����40mL���������Ķ������̷�Ӧ��ʵ���ϲ������������ΪV2��V1����ΪŨ����Ͷ������̷�Ӧ����������ϡ����Ͷ������̲���Ӧ���������ŷ�Ӧ�Ľ��У�Ũ������ϡ���ᣬ��Ӧ���ٽ��У���V2��V1��
�ʴ�Ϊ���������ŷ�Ӧ���У���Ӧ��Ũ�ȼ�С����Ӧ���ٽ��У�
���������
�����Ѷȣ�һ��
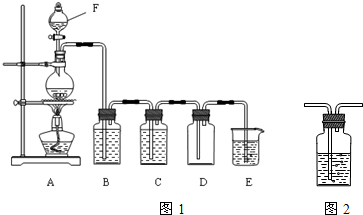
5������� ʵ������ȡ������װ����ͼ1��
��1��װ��F��������______����ͼ��װ��װ�ú�����Ҫ���еIJ����ǣ�______��
��2��װ��B��ʢ�ŵ��Լ���______����������______��װ��C��ʢ�ŵ��Լ���______����������______��
��3��д��E�з�����Ӧ�Ļ�ѧ����ʽ��______��
��4��ͼ2װ����ϴ��ƿ����װ���ڻ�ѧʵ���г�ϴ���⣬���ж�����;������д����һ����;��______��
��5��ʵ������ʱ�ø�����ش���������̣���Ũ���ᷴӦ��ȡ��������Ӧ����ʽ���£�2KMnO4+16HCl=2KCl+2MnCl2+5Cl2��+8H2O
��15.8g?KMnO4��������Ũ�����ַ�Ӧ������______mol?HCl��������ת�Ƶ��ӵ����ʵ���Ϊ______mol��������Cl2�ڱ�״���µ����Ϊ______L��
�ο��𰸣���1��װ��F�������Ƿ�Һ©�����Ʊ�������װ��װ�ú�����Ҫ���еIJ����Ǽ��װ�õ������ԣ�
�ʴ�Ϊ����Һ©�������װ�õ������ԣ�
��2��װ��Bʢ�ű���ʳ��ˮ����ȥHCl���壻װ��C��ʢ��Ũ���ᣬ����ˮ������
�ʴ�Ϊ������ʳ��ˮ����ȥHCl���壻Ũ���ᣬ����ˮ������
��3��װ��Eʢ������������Һ������β���е���������Ӧ����ʽΪ��Cl2+2NaOH�TNaCl+NaClO+H2O��
�ʴ�Ϊ��Cl2+2NaOH�TNaCl+NaClO+H2O��
��4��ͼ2װ�ÿ�������ȫƿ������ƿ�ȣ�
�ʴ�Ϊ����ȫƿ������ƿ��
��5��15.8g?KMnO4�����ʵ���Ϊ15.8g158g/mol=0.1mol����2KMnO4+16HCl=2KCl+2MnCl2+5Cl2��+8H2O��֪���ɵ����������ʵ���Ϊ0.1mol��52=0.25mol����������HCl����������������ԭ���غ���㱻������HClΪ0.25mol��2=0.5mol����Ԫ�ػ��ϼ���-1������Ϊ0���㣬��ת�Ƶ������ʵ���Ϊ0.25mol��2=0.5mol���������������Ϊ0.25mol��22.4L/mol=5.6L��
�ʴ�Ϊ��0.5��0.5��5.6��
���������
�����Ѷȣ�һ��