1、填空题 (2分)配平方程式:? Zn +? HNO3― Zn(NO3)2 +? N2 +? H2O
参考答案: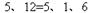
本题解析:略
本题难度:一般
2、选择题 在热的稀硫酸溶液中溶解了12.16gFeSO4,当加入50mL0.4mol?L-1KNO3溶液后,使其中的Fe2+全部转化成Fe3+,KNO3溶液也完全反应,并有NxOy气体逸出,则该NxOy是
A.N2O
B.NO
C.N2O3
D.NO2
参考答案:A
本题解析:n(FeSO4)= 12.16g÷152g/mol=0.08mol。n(NO3-)= 0.4mol/L×0.05L=0.02mol。由于在氧化还原反应中电子转移的物质的量相等,假设在反应后N元素的化合价为+a,0.08mol×1=0.02mol×(5-a)。解得a=+1,所以NxOy是N2O。选项为A。
本题难度:一般
3、简答题 (1)在-50℃时,液氨存在如下电离:2NH3?NH4++NH-2,k=2×10-12,液氨的电离达到平衡时,各微粒的浓度大小关系为______,加入NH4Cl固体,K______2×10-12(填“<”、“>”或“=”)
(2)已知25℃时Ksp(AgCl)=1.8×10--10,在10mL?0.10mol/L?AgNO3溶液中加入10mL0.20mol/LNaCl溶液,充分反应后溶液中的c(Ag+)=______.
(3)配平硫酸亚铁加强热制备铁红和生成硫的两种常见氧化物的化学方程式:
______FeSO4
______Fe2O3+____________+____________
(4)已知氯气能溶于水,溶液呈酸性.如图所示的两个实验装置中,溶液的体积均为200mL,开始时电解质溶液的浓度均为0.1mol/L,工作一段时间后,测得导线中均通过0.02mol电子,若不考虑盐的水解和溶液体积的变化,则下列叙述中正确的是______
A.产生气体的体积:①>②
B.溶液的pH变化:①减小,②增大
C.电极上析出物质的质量:①>②
D.电极反应式:①中阳极?2Cl--2e-?Cl2↑? ②中负极?2H++2e-?H2↑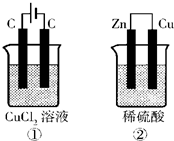
参考答案:解;(1)在液氨中,存在最多的微粒是液氨分子,由液氨电离出的铵根和亚铵根离子浓度一定是相等的,即c(NH3)>c(NH4+)=c(NH2-),
加入氯化铵固体以后,由于温度不变,所以K不变,故答案为:c(NH3)>c(NH4+)=c(NH2);=;
(2)10mL?0.10mol/L?AgNO3溶液中加入10mL0.20mol/LNaCl溶液,反应后剩余氯离子的物质的量浓度为(0.2×0.01)mol-(0.1×0.01)mol0.02L=0.05mol/L,
根据氯化银的Ksp=[Ag+][Cl-],则[Cl-]=Ksp[Ag+]=1.8×10-10mol2/L20.05mol/L=3.6×10-9mol/L,故答案为:3.6×10-9mol/L;
(3)硫的两种常见氧化物是二氧化硫和三氧化硫,根据原子守恒,则2FeSO4=Fe2O3+SO2↑+SO3↑,故答案为:2;1;1;1;
(4)A.①的原理方程式为:CuCl2?通电?.?Cu+Cl2↑,②的原理方程式为:Zn+2H+=Zn2++H2↑,当转移电子为0.02mol时,则①中产生氯气味0.01mol,
②中产生的氢气为0.01mol,产生气体的体积:①=②,故A错误;
B.①氯化铜电解实质是电解物质本身,②消耗氢离子,所以酸性溶液的pH变化:①不变,②增大,故B错误;
C.当转移电子为0.02mol时,①中阴极上析出金属铜为0.01 mol,即0.64g,②电极上析出氢气0.01mol,即0.02g,所以析出物质的质量:①>②,故C正确;
D.电极反应式:①中阳极发生失电子的氧化反应,即2Cl--2e-?Cl2↑,②中负极为金属锌,发生失电子的氧化反应,即Zn-2e-=Zn2+,故D错误.
故选C.
本题解析:
本题难度:一般
4、填空题 (1)写出铝和氧化铁反应的化学方程式,并用双线桥法表示电子的转移情况
(2)写出下列反应的离子方程式
碳酸氢钠溶液与盐酸反应
碳酸氢钠溶液与氢氧化钠反应
氢氧化铝与盐酸反应
氢氧化铝与氢氧化钠反应
(3)写出下列反应的化学方程式Ba2+ + SO42- =BaSO4 ↓
参考答案:(1)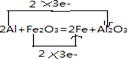
(2)HCO3-+H+= CO2 ↑+H2O HCO3-+OH-=CO32- Al(OH)3 +3H+=Al3++H2O Al(OH)3 +OH-=AlO2-+2H2O
(3)BaCl2 + Na2SO4 = BaSO4 ↓+2NaCl
本题解析:(1)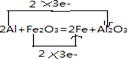
(2)碳酸氢钠溶液与盐酸反应:HCO3-+H+= CO2 ↑+H2O ;碳酸氢钠溶液与氢氧化钠反应:HCO3-+OH-=CO32- + H2O ;氢氧化铝与盐酸反应:Al(OH)3 +3H+=Al3++H2O ;氢氧化铝与氢氧化钠反应:Al(OH)3 +OH-=AlO2-+2H2O
(3)Ba2+ + SO42- =BaSO4 ↓表示可溶性的钡盐和可溶性硫酸盐的反应,化学方程式为BaCl2 + Na2SO4 = BaSO4 ↓+2NaCl
考点:考查氧化还原反应中电子转移,离子方程式的书写等知识。
本题难度:一般
5、选择题 在8NH3+3Cl2====6NH4Cl+N2反应中,若有2 mol N2生成,发生氧化反应的NH3的物质的量是 (? )
A.16 mol
B.8 mol
C.4 mol
D.3 mol
参考答案:C
本题解析:根据反应式可判断,3mol氯气全部是氧化剂,需要得到6mol电子。根据得失电子守恒可知,所以被氧化的氨气是2mol,生成氮气是1mol。因此若有2 mol N2生成,发生氧化反应的NH3的物质的量是4mol。或者利用氮原子守恒,因为氮气是氧化产物,根据氮原子守恒可知,÷被氧化的氨气就越高是4mol。答案选C。
本题难度:一般