|
�߿���ѧ֪ʶ���ܽᡶ����ľ���������������ռ�������Ԥ�⣨2019�����°棩(ʮ)
2019-05-30 03:17:25
�� �� �� ��
|
1��ʵ���� ��8�֣���ʵ�����Ƹ�������ʵ���У��Ʒ�
��1����Ӧԭ��������ʽ��Ϊ����������������������������������������
��2��ʵ��װ����ͼ��ʾ
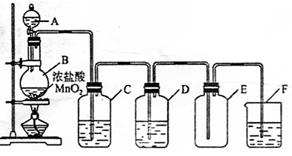
ָ������װ������ʢ�Լ��������ã�
C��???
D��???
F��???
�ο��𰸣�

�����������
�����Ѷȣ���
2��ʵ���� ijУ��ѧѧϰС������֤NO�ܱ�������ԭ���ⶨ��ת���ʣ��������ʵ�飺
�ο�֪ʶ��NO������FeSO4��Һ��Ӧ���ɿ���������������������+2�ۣ���NO+FeSO4=Fe(NO)SO4
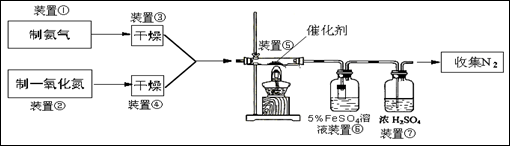
�Իش��������⣺
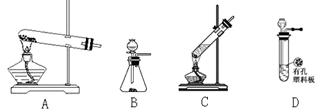
�� ������ͼ��װ��?�����ţ���ѡ�����а�����ʵ�����Ʊ���
Dװ�ÿ���������?�����ţ���ѡ��������Ʊ���
a CO2? b O2? c SO2?d C2H4? e C2H2? f H2?
�� װ�âۡ�������ͬһװ�ã����װ������ʢװ��ҩƷ��?�����ţ�
A���Ȼ���
B��Ũ����
C������������
D����ʯ��
| �� װ�â��У��ֲ�����X������?��װ�âߵ�����?
�� װ�âĹ��ƿ�У�������Fe(NO)SO4�⣬���а�ɫ�������ɣ�д�����ɸó��������ӷ���ʽ?
�� ������װ�âݵ�NOΪ2.688L����״������ͬ������������������ռ���2.016LN2����NO��ת����Ϊ?��
�ο��𰸣���9�֣���1��ABC��2�֣�? af��1�֣�? (2) D��1�֣�
��3����ֹ������1�֣�����ȥδ��Ӧ�İ���������N2��1�֣�
��4��Fe2��+2NH3+2H2O=Fe(OH)2��+2NH4�� ��1�֣�?��5��90��?��2�֣�
�����������1��ʵ�����Ʊ�������������ʯ�����Ȼ�識��ȣ���װ��A��ȷ��Ҳ���Խ���ˮ���뵽��ʯ�һ��ʯ���У���B��ȷ������ֱ�Ӽ���Ũ��ˮ��C���ԣ���ѡABC��Dװ���Ǽ������շ�����������ԭ���Ʊ�������CO2����ѡaf��
��2�������Ǽ������壬���������Ը������Ҳ�������Ȼ��Ƹ��ﰱ�������ѡD��
��3��������������ˮ������װ�â��У��ֲ�����X�����÷�ֹ������Ҫ�ռ�����������Ҫ��ȥ�����еİ���������Ũ����������dz�ȥδ��Ӧ�İ���������N2��
��4����������ˮ���ɰ�ˮ����Һ�Լ��ԣ����������ӷ�Ӧ����������������ɫ��������Ӧ�����ӷ���ʽ��Fe2��+2NH3+2H2O��Fe(OH)2��+2NH4����
��5��NO�����ʵ�����2.688L��22.4L/mol��0.12mol�����������ʵ�����2.016L��22.4L/mol��0.09mol������ݷ�Ӧ�ķ���ʽ4NH3��6NO��5N2��6H2O��֪����NO��0.108mol������NO��ת������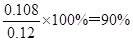 �� ��
�����������Ǹ߿��еij�����������ͣ������е��Ѷ�����Ŀ��飬�����ۺ���ǿ�����ض�ѧ�������������ͽ��ⷽ����ָ����ѵ����ּ�ڿ���ѧ��������û���֪ʶ���ʵ�����������������������ѧ���������������淶�Ͻ���ʵ��������������ѧ����ѧ������������Ĺؼ�����ȷʵ��ԭ�������ܽ��װ��������ü��ɡ�
�����Ѷȣ�����
3��ʵ���� ��10�֣�ij��ȤС��ͬѧ��ͬ�������ͼ��ʾ��ʵ��װ�á���װ�üȿ�������ȡ���壬�ֿ�������֤���ʵ����ʡ�
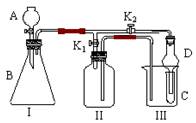
�Ŵ�K1�ر�K2������ȡijЩ���塣
��ͬѧ��Ϊװ��I��������ȡH2��NH3��O2����װ��IIֻ���ռ�H2��NH3�������ռ�O2����������?��
��ͬѧ��Ϊ�ڲ��Ķ�װ��II������ǰ���£���װ��II�����ʵ��Ľ���Ҳ���ռ�O2������Ϊ���ĸĽ�������?��
�ƴ�K2�ر�K1���ܱȽ�һЩ���ʵ����ʡ�
��ͬѧ���ʵ��Ƚ������ԣ�KMnO4��Cl2��Br2����A�м�Ũ�����һ��ʱ�䣬�۲쵽C�е�������?������D�ڸ�װ���е�������?��
��ͬѧ��ʯ��ʯ�����ᡢ�����Ƶ�ҩƷ�������һʵ�顣����ʵ��Ŀ����?��
�ο��𰸣�(1)�������ܶȱȿ�����2�֣�?��װ��II��װ�Mˮ (2��)
(2)��Һ�ʳ�ɫ�ȣ�2�֣�?��ֹ���� (2��)
�Ƚϴ��ᡢ̼��ͱ��ӵ����ԣ�CH3COOH ��H2CO3��C6H5OH��(2��)
(���10�֣����������𰸲��ո���)
�����������
�����Ѷȣ���
4������� ����7��)ijͬѧ�������ͼ��ʾװ�ã��г�����ʡ�ԣ�����ϵ��ʵ�飬ʵ��ʱ��ҩƷA��μ��뵽����B�У����������ʵ��ش����⣺
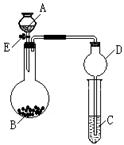
(1����AΪŨ��ˮ��BΪ�����ƣ�C��ʢ��AlCl3��Һ����������E���㹻��ʱ��۲쵽C�е�����Ϊ?��Բ����ƿ�з�����Ӧ�Ļ�ѧ����ʽΪ?��
(2����AΪ30%��H2O2��Һ��BΪ�������̣�C��ʢ���ữ����FeCl2��Һ����������E��C�е�����Ϊ?��Բ����ƿ�з�����Ӧ�Ļ�ѧ����ʽΪ?��
(3)��������װ�û�������֤SO2�Ļ�ѧ����, AΪ��Ũ���ᣬBΪ�������ƣ���C��ʢ��?
?��Һ����֤SO2��������; C��ʢ��?��Һ����֤�仹ԭ��; ��C��ʢ��?��Һ����֤��Ư���ԡ�
�ο��𰸣�1���а�ɫ�������ɣ�CaO+NH3��H2O==Ca��OH��2+ NH3��
(2����ɫ��dz��ɫ��Ϊ�ػ�ɫ? 2H2O2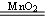 2H2O+ O2�� 2H2O+ O2��
(3��H2S?��ˮ����ˮ�����Ը������?Ʒ��
�����������1��Ũ��ˮ������ʯ�������ɰ����������ķ�Ӧ��CaO+NH3��H2O==Ca��OH��2+ NH3�����������Ȼ�����Ӧ��������������ɫ������
��2��˫��ˮ�ڶ������̵Ĵ������£���������������ʽΪ2H2O2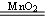 2H2O+ O2���������ܰ����������������������ӣ�����Һ��ɫ��dz��ɫ��Ϊ�ػ�ɫ�� 2H2O+ O2���������ܰ����������������������ӣ�����Һ��ɫ��dz��ɫ��Ϊ�ػ�ɫ��
��3��SO2�ܰ������������ɵ�����Ҳ�ܻ�ԭ��ˮ����ˮ�����Ը��������Һ��SO2Ҳ����Ư���ԣ���ʹƷ����Һ��ɫ��
�����Ѷȣ�һ��
5��ѡ���� �ռ�NO��NO2��������
[? ]
A����������ˮ��?
B��NO����ˮ����NO2������������
C������������������?
D��NO��������������NO2����ˮ��
�ο��𰸣�B
���������
�����Ѷȣ���
|