|
|
|
高考化学试题《原电池原理》高频考点巩固(2019年模拟版)(九)
2019-05-30 03:20:26
【 大 中 小】
|
1、选择题 关于如图装置说法正确的是
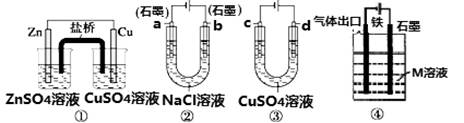
A.装置①中,盐桥中的K+移向ZnSO4溶液
B.装置②工作一段时间后,a极附近溶液的OH-的浓度增大
C.用装置③精炼铜时,c极为粗铜
D.装置④中若M是海水,该装置是通过“牺牲阳极保护法”使铁不被腐蚀
|
2、选择题 控制合适的条件,将反应2 Fe3++2 I- 2 Fe2++ I 2 ?设计成如图所示的原电池。下列判断不正确的是 2 Fe2++ I 2 ?设计成如图所示的原电池。下列判断不正确的是
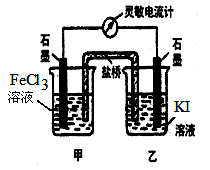
A.反应开始时,乙中石墨电极上发生氧化反应
B.反应开始时,甲中石墨电极上Fe3+被还原
C.电流计 读数为零时,反应达到化学平衡状态 读数为零时,反应达到化学平衡状态
D.电流计读数为零后,在甲中加入FeCl2固体,乙中石墨电极为负极
3、填空题 (10分)(1)为了验证Fe3 +与Cu2+氧化性强弱,下列装置能达到实验目的的是___________
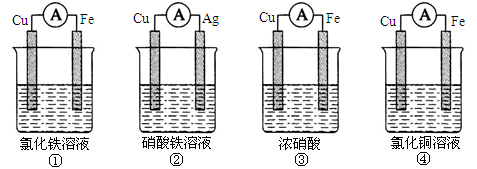
(2)将CH4设计成燃料电池,其利用率更高,装置如图所示(A、B为多孔碳棒)。
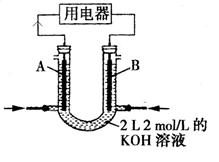
①_______处电极入口通甲烷(填A或B),其电极反应式为_______________________________
_________________________________________
②当消耗甲烷的体积为22.4L(标准状况下)时, 假设电池的能量转化率为100%,则导线中转移电子的物质的量为 ,消耗KOH的物质的量为_____________________。
4、选择题 已知空气―锌电池的电极反应为:
锌片:Zn+2OH
5、填空题 (5分)干电池是一种?的装置。干电池外围的锌皮是电池的?极,发生?(“氧化” 或“还原” )反应;中间碳棒是电池的?极,发生?(“氧化” 或“还原” )反应。
|