1、填空题 某溶液中可能含有H+、Na+、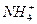 、Mg2+、Fe3+、Al3+、
、Mg2+、Fe3+、Al3+、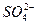 等离子,当向该溶液中加入某浓度的NaOH溶液时,发现生成沉淀的物质的量随NaOH溶液的体积变化如图所示,由此可知,该溶液中肯定含有的阳离子是_____________,且各阳离子的物质的量之比为_____________;肯定不含有的阳离子是_____________;检验可能含有的某种阳离子的实验方法是____________________________________________________。
等离子,当向该溶液中加入某浓度的NaOH溶液时,发现生成沉淀的物质的量随NaOH溶液的体积变化如图所示,由此可知,该溶液中肯定含有的阳离子是_____________,且各阳离子的物质的量之比为_____________;肯定不含有的阳离子是_____________;检验可能含有的某种阳离子的实验方法是____________________________________________________。
参考答案:H+、Al3+、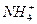 2∶1∶3 Mg2+、Fe3+焰色反应
2∶1∶3 Mg2+、Fe3+焰色反应
本题解析:由图可知,由于起始时加入NaOH时没有沉淀生成,所以溶液中肯定含有H+,且物质的量可以设为2 mol;由于沉淀最终随着NaOH的加入完全消失,所以溶液中肯定不含Mg2+、Fe3+,肯定含有Al3+,物质的量为1 mol;根据图象中的平行线可知溶液中含有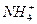 ,且物质的量为3 mol。所以溶液中各阳离子的物质的量之比为2∶1∶3。题意中没有任何现象验证Na+的存在,可以用焰色反应的实验检验是否含有Na+。
,且物质的量为3 mol。所以溶液中各阳离子的物质的量之比为2∶1∶3。题意中没有任何现象验证Na+的存在,可以用焰色反应的实验检验是否含有Na+。
本题难度:简单
2、填空题 (6分)a、b、c、d是HCl、BaCl2、AgNO3、Na2CO3四种溶液中的一种,现将它们两两混合,现象如下表所示:
反应物
| a+b
| c+d
| a+d
| a+c
| b+d
|
现象
| 白色沉淀
| 白色沉淀
| 白色沉淀
| 白色沉淀
| 无色气体
|
(1)请用化学式填写a是?、b是?、c是?、d是?
(2)写出a+c反应的离子方程式?。
参考答案:(1)AgNO3、HCl、BaCl2、Na2CO3(2)Ag++Cl-=AgCl↓
本题解析:根据四种物质可知,硝酸银能和另外3种反应生成白色沉淀,所以a是硝酸银;又因为盐酸能和碳酸钠反应生成CO2气体,所以b、d是盐酸和碳酸钠,则c是氯化钡。由于盐酸和氯化钡不反应,所以b是氯化氢,d是碳酸钠。
点评:进行物质的检验时,要依据物质的特殊性质和特征反应,选择适当的试剂和方法,准确观察反应中的明显现象,如颜色的变化、沉淀的生成和溶解、气体的产生和气味、火焰的颜色等,进行判断、推理。
本题难度:一般
3、选择题 欲配制含有大量下列各离子的溶液,能够实现的是
A.Na+、CO32-、OH-、H+
B.Cu2+、Na+、H+、SO42-
C.Mg2+、K+、Cl-、OH-
D.H+、NO3-、Na+、ClO-
参考答案:B
本题解析:分析:离子之间不能结合生成水、气体、沉淀、弱电解质等,不能发生氧化还原反应等,则离子能够共存,即可实现溶液的配制.
解答:A.因OH-、H+能结合生成水,CO32-、H+结合生成水和气体,则不能共存,即不能实现,故A错误;
B.该组离子之间不反应,可实现溶液的配制,故B正确;
C.因Mg2+、OH-能结合生成沉淀,则不能共存,即不能实现,故C错误;
D.因H+、ClO-能结合生成弱电解质,则不能共存,即不能实现,故D错误;
故选B.
点评:本题以溶液的配制来考查离子的共存问题,题目难度不大,熟悉离子的性质及离子之间的反应即可解答.
本题难度:简单
4、选择题 某无色溶液中含有NH4+、K+、Al3+、SO42ˉ四种离子,进行如下实验:
(1)取10 mL该溶液于试管中并滴加Ba(NO3)2溶液,加稀硝酸酸化后过滤得到0.03 mol白色沉淀;
(2)取10 mL该溶液于试管中,滴加NaOH溶液产生白色沉淀,当沉淀增加到一定量后开始产生气体(必要时可加热),最后沉淀完全溶解。并且随NaOH溶液的加入,沉淀和气体的变化关系如下图所示。
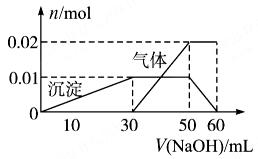
下列说法不符合事实的是(?)
A.根据图所示数据计算实验中使用的NaOH溶液的物质的量浓度为1mol/L
B.根据信息分析该溶液中焰色反应呈现紫色的离子的物质的量浓度为1mol/L
C.另取一定量该溶液滴加一定量的Ba(OH)2溶液,能使Al3+和SO42ˉ同时完全沉淀
D.NH4+、K+、Al3+、SO42ˉ四种离子的物质的量之比为:2:1:1:3
参考答案:C
本题解析:(1)中白色沉淀为硫酸钡沉淀,沉淀量为0.03mol,故溶液中含有硫酸根。且硫酸根的物质的量为0.03mol。(2)另取10mL该溶液于试管中,滴加NaOH溶液产生白色沉淀,则说明溶液中含有Al3+,Al3++3OH-=Al(OH)3↓,结合图象中沉淀的变化关系,知溶液中含有Al3+为0.01mol需OH-为0.03mol;当沉淀增加到一定量后开始产生气体,根据NH4++OH-=NH3↑+H2O结合图象,知溶液中含有NH4+为0.02mol需OH-为0.02mol;最后沉淀完全溶解是由于氢氧化铝与NaOH继续反应,反应的离子方程式为Al(OH)3+OH-=AlO2-+2H2O,结合图象中沉淀的变化关系,需OH-为0.01mol;实验中使用的NaOH溶液的总物质的量为:0.03mol+0.02mol+0.01mol=0.06mol,结合图象中沉淀的变化关系知此时氢氧化钠溶液的体积为60mL,故c(NaOH)=1mol/L。A选项,正确。B选项,由于该溶液中含有K+、NH4+、Al3+、SO42-;根据NH4+为0.02mol,Al3+为0.01mol,SO42-为0.03mol,根据溶液呈电中性溶液中阴阳离子所带的正负电荷总数相等,其中正电荷总数为:0.02mol×1+0.01mol×3+n(K+)×1=0.05mol+n(K+),负电荷总数0.03mol×2=0.06mol,所以n(K+)=0.01mol,故其浓度为1mol/L,正确。C选项,根据上述可知Al3+为0.01mol,硫酸根为0.03mol,弱使其同时完全沉淀,则需Ba2+0.03mol,OH-=0.03mol,无法以加入Ba(OH)2的形式完成。过错误。D选项,正确。
本题难度:一般
5、选择题 向10mL 0.1mol・L-1?NH4Al(SO4)2溶液中,滴加等浓度Ba(OH)2溶液x mL,下列叙述正确的是? (? )
A.x=10时,溶液中有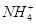 、
、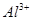 、
、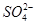 ,且
,且
B.x=10时,溶液中有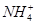 、
、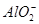 、
、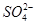 ,且
,且
C.x=30时,溶液中有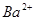 、
、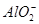 、
、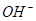 ,且
,且
D.x=30时,溶液中有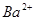 、
、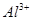 、
、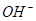 ,且
,且
参考答案:A
本题解析:
为了方便计算,可以把溶液的体积都扩大100倍,1000,mL 0.1mol・L-1?NH4Al(SO4)2溶液中含有0.1molNH4+ ,0.1mmolAL3+,0.2mmolSO42-,1000ml等浓度Ba(OH)2溶液有0.1mol Ba2+,0.2molOH-,混合后硫酸钡沉淀,剩余0.1mol SO42-。氢氧化铝沉淀,剩余AL3+,所以A答案对。由于氢氧根离子的物质的量小于AL3+3倍,所以溶液中还含有AL3+,没有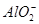 ,故B错
,故B错
同理,当Ba(OH)2体积扩大3倍时,溶液中0.3mol Ba2+,0.6molOH-,混合后,剩余0.1mol Ba2+
,生成了偏铝酸根,故C、D错。3+与OH-反应关系式
点评:本题难度大,但是只要将两种溶液中所含的离子的物质的量全部都计算出来,根据相应的化学方程式序数关系,即可计算出溶液中存在哪些离子。
本题难度:一般