1������� ���г�����������A��B��C������ס��ҡ���������D��E��F��G��H������֮���������ת����ϵ��ͼ����Щ��Ӧ�IJ���ͷ�Ӧ������û��ȫ�������������B�ǵؿ��к����ӵ�һ�Ľ���Ԫ�أ���ش��������⣺

��1��д������B��������Ļ�ѧʽ______��______��
��2��д����Ӧ�ٵĻ�ѧ��Ӧ����ʽ______��
��3��д����Ӧ�����ӷ���ʽ______��
2������� ��ͼ�Dz���Ԫ�صĵ��ʺͻ�����֮����ת����ϵ�����ַ�Ӧ��������û��ȫ���г�����֪ԭ��A��M�����ڽ��������L�������ֳ�����ɵģ�F��Y��Ӧ������һ��ȫ��Ϊ�ǽ���Ԫ������ɵ��Σ�C����ɫ��Ӧ�ʻ�ɫ��M�д��ԣ���Ӧ����B��C�����ʵ���֮��Ϊ3��4��
�ش��������⣺
��1����Ӧ�ڵ���Ҫ��;�ǣ�______����һ�㼴�ɣ�2�֣���Y�Ŀռ乹��Ϊ______��
��2����֪��Ӧ���л���һ����ɫ�������ɣ�д����Ӧ�۵����ӷ���ʽ��______��
��3��L�����ֳ���Ϊ______���û�ѧʽ��ʾ����A�Ļ�ѧʽΪ______��
��4������M����ϡ�����п��γ���ҺZ������Ƽ�ʵ�飬֤��Z��Һ�������Ľ��������ӣ�______��

3������� ����ת����ϵͼ�У�A��B��C��D��E������Ϊ���壬B��E��F��KΪ���ʣ�����FΪ��ɫ���壻C��D����ʹ�����ʯ��ˮ����ǣ�D��E����ʹƷ����Һ��ɫ��I��һ�ֺ���ɫ�����������ش��������⣺
��1��E�ĵ���ʽΪ______��
��2����Ӧ�۵����ӷ���ʽΪ______��
��3��F��G����Һ��Ӧ�Ļ�ѧ����ʽΪ______��
��4��������ҺL�н��������ӵķ�����______��
��5������A���ܶ�Ϊ��ͬ״���������ܶȵ�30������A�к�3�����Ԫ�أ�ͨ�����㡢��������ȷ��A�ķ���ʽΪ______���˷���ʽ��Ԫ�ط�����д����������Ԫ��ԭ����������С�С�˳�����У���A�����и�ԭ�Ӿ���8�����ȶ��ṹ������ṹʽΪ______��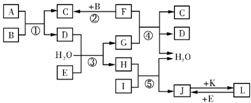
4������� X��Y��Z��W���������������ת����ϵ������X��W���ʣ�Y��ZΪ�����δ�г���Ӧ������
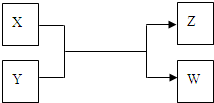
����Z�������г��õĵ�ζƷ��W��������Һ��������
��1�������£�X����ɫ��______��
��2����ҵ��Z�ж�����;���û�ѧ����ʽ��ʾZ��һ����;______��
��3�����������õ�Z�����˵���أ�����X��Y��Һ��Ӧʱ���Եõ�һ�ֵ����Σ��˷�Ӧ�����ӷ���ʽ��______��
����X�ǹ�ҵ���������Ľ������ʣ�Z��һ�־��д��Եĺ�ɫ���壬��
��1��X��Y��Ӧ�Ļ�ѧ����ʽ��______��
��2����������װ��ֻ����Z+W�TX+Y��Ӧ���г�װ��δ��������

����ɴ�ʵ���жಽ���������������ǣ�
a����ȼ�ƾ���
b�������
c���������崿��
�������������Ⱥ�˳����______������ĸ����
��Ϊ��֤ʵ��ɹ�������װ����Ҫ�Ľ��������ǣ�������������______��
��3����3.48g?Z����50mL?4mol/L��ϡHNO3�г�ַ�Ӧ������112mL��NO����״��������Ӧ�����Һ�еμ�NaOH��Һ�ܲ�������������������࣬������Ҫ����2mol/L��NaOH��Һ______mL?����ȷ��0.1����
5������� V��W��X��Y��Z�����ֳ���Ԫ�أ�����V��W��X��Y���ֶ�����Ԫ�������ڱ��е�λ����ͼ1��ʾ��
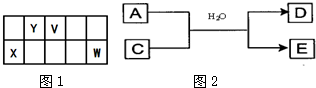
V��W�������̬�⻯��M��N���ʱ�а������ɣ�M��ʹʪ���pH��ֽ������Z������Ѫ�쵰���д��ڵĽ���Ԫ�أ�����д���пհף�
��1��W��ԭ�ӽṹʾ��ͼΪ______��
��2���������ѣ�TiO2����X�ĵ��ʡ�Y�ĵ��ʸ����·�Ӧֻ�������ֻ���������ֻ������������Ԫ����ɣ��䷴Ӧ�Ļ�ѧ��ʽ______��
��3����XԪ�ص�һ�ֻ�����A��Y�����������C֮������ͼ2�ķ�Ӧ��ϵ����EΪ��ɫ��������E���ʵĻ�ѧʽΪ______��
��4����ͬ��̬X��Z�����ӵ���Һ�еμ�NaOH��Һ��X��Z��Ԫ�طֱ������X��OH��n��ȫ������pH��4.7��Z��OH��n��ȫ������pH��2.8����ksp��X��OH��n��______�������������ksp��Z��OH��n����
��5��������N2H4��Ҳ�����£�����Ҫ�Ļ��ȼ�ϣ��Դ���������Һ����M���ܻ���µ�ϡ��Һ���䷴Ӧ�����ӷ���ʽΪ______��ͬ��ͬѹ�£���?a?L?M�����b?L?N����ͨ��ˮ�У���������Һ��pH=7����a______b�������������=������