1、选择题 下列混合溶液中,各离子浓度的大小关系不正确的是(?)
A.物质的量浓度相等CH3COOH和CH3COONa溶液等体积混合:
c(CH3COO-) + c(CH3COOH)=2c(Na+)
B.0.1 mol/L Na2CO3溶液:c(OH-)=c(HCO3-)+c(H+)+c(H2CO3)
C.物质的量浓度相等Na2CO3和NaHCO3溶液等体积混合,离子浓度的大小顺序是
c (Na+)>c (HCO3-)> c(CO32-)>c(OH-)> c(H+)
D.NH4Cl溶液中:c(H+) = c(NH3・H2O) +c(OH-)
参考答案:B
本题解析:A、物质的量浓度相等CH3COOH和CH3COONa溶液等体积混合,根据物料守恒,c(CH3COO-)+ c(CH3COOH)= 2c(Na+),正确;B、0.1 mol/L Na2CO3溶液,根据质子守恒,c(OH-)=c(HCO3-)+c(H+)+2c(H2CO3),错误;C、物质的量浓度相等Na2CO3和NaHCO3溶液等体积混合,离子浓度的大小顺序是碳酸钠水解程度大,碳酸根离子浓度小于碳酸氢根离子,c (Na+)>c (HCO3-)> c(CO32-)>c(OH-)> c(H+),正确;D、NH4Cl溶液中,根据质子守恒,c(H+)= c(NH3・H2O)+ c(OH-),正确。
本题难度:一般
2、选择题 下列叙述正确的是 (?)
A.将过量CO2气体通入水玻璃中可制得硅酸和纯碱
B.标准状况下,2.24L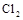 与过量稀NaOH溶液反应,转移电子0.1mol
与过量稀NaOH溶液反应,转移电子0.1mol
C.1L2mol・L-1明矾经水解可得到氢氧化铝胶体粒子数目为2×6.02×1023
D.漂白粉溶于水能导电,故漂白粉是电解质
参考答案:B
本题解析:A、过量CO2气体与硅酸钠溶液反应生成硅酸和碳酸氢钠,错误;B、标准状况下2.24L的氯气的物质的量是0.1mol,与氢氧化钠反应时既作氧化剂又作还原剂,所以转移电子0.1mol,正确;C、水解时可逆的,所以1L2mol・L-1明矾经水解可得到氢氧化铝胶体粒子数目小于2×6.02×1023
,错误;D、电解质属于化合物,而漂白粉是次氯酸钙与氯化钙的混合物,不是电解质,错误,答案选B。
本题难度:一般
3、选择题 下列各离子方程式中,属于水解反应的是
A.HCO3-+H2O  H3O++CO32-
H3O++CO32-
B.NH4++H2O  NH3・H2O+H+
NH3・H2O+H+
C.PO43-+ H3O+ HPO42-+ H2O
HPO42-+ H2O
D.H2O+H2O  H3O++OH-
H3O++OH-
参考答案:B
本题解析:略
本题难度:一般
4、选择题 在一定条件下,Na2CO3溶液存在水解平衡:CO32- + H2O HCO3-+OH-。下列说法错误的是
HCO3-+OH-。下列说法错误的是
A.稀释溶液,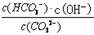 增大
增大
B.通入CO2,溶液PH减小
C.升高温度,水解平衡常数增大
D.加入NaOH固体,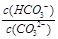 减小
减小
参考答案:A
本题解析:
答案:A
A、不正确,该反应的平衡常数K=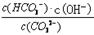 ,只随温度改变而改变,所以稀释溶液,
,只随温度改变而改变,所以稀释溶液,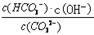 不变。B、正确,通入CO2,平衡正向移动,溶液PH减小;C、正确,升高温度,水解吸热,平衡正向移动,水解平衡常数增大;D、正确,加入NaOH固体,平衡逆向移动,
不变。B、正确,通入CO2,平衡正向移动,溶液PH减小;C、正确,升高温度,水解吸热,平衡正向移动,水解平衡常数增大;D、正确,加入NaOH固体,平衡逆向移动,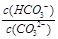 减小。
减小。
本题难度:一般
5、选择题 在蒸发皿中加热蒸干并灼烧,下列物质的溶液,可以得到该固体物质的是
A.氯化铝
B.碳酸氢钠
C.高锰酸钾
D.硫酸铁
参考答案:D
本题解析:A错,热蒸干氯化铝溶液,铝离子会水解生成氢氧化铝,灼烧生成氧化铝;
B错,碳酸氢钠不稳定受热易分解为碳酸钠,加热后得到的固体为碳酸钠;
C错,高锰酸钾受热不稳定易分解为锰酸钾、二氧化锰。
D正确,硫酸铁溶液中虽然+3铁离子要发生水解,但水解后生成的氢氧化铁与硫酸会继续反应,最终得到硫酸铁固体。
本题难度:一般