1、选择题 “嫦娥二号”的制造使用了铝―锂、铝―镁等多种合金材料,火箭推进剂中发生反应:N2O4+2N2H4=3N2+4H2O。下列有关叙述不正确的是
A.锂、铝、镁都属于金属单质
B.火箭推进剂中发生的反应属于氧化还原反应
C.16 g N2H4中含有的H原子数为1.204×1023
D.N2O4属于氧化物
参考答案:C
本题解析:
答案:C
C、不正确,16 g N2H4中含有的H原子数为16g/32g/mol×4NA=6.02×1023
本题难度:一般
2、选择题 NO2与水的反应可表示为:3NO2+H2O=2HNO3+NO,关于此反应中的下列说法正确的是(?)
A.氮元素的化合价没有发生变化
B.NO2只是氧化剂
C.NO2只是还原剂
D.NO2既是氧化剂,又是还原剂
参考答案:D
本题解析:NO2中氮元素的化合价是+4价,变为HNO3中的+5价和NO +2价,所以,NO2既是氧化剂,又是还原剂,选D。
本题难度:简单
3、选择题 下列有关化学用语表示和概念判断叙述正确的是
A.1molH2燃烧放出的热量为H2的燃烧热
B.氢氧根离子的电子式: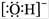
C.氯原子的结构示意图:
D. 和
和 互为同系物
互为同系物
参考答案:B
本题解析:A、在25℃,101 kPa时,1 mol可燃物完全燃烧生成稳定的氧化物时所放出的热量,叫做该物质的燃烧热,单位为kJ・mol-1。1molH2燃烧放出的热量,与状态有关,A错误;B、正确;C、氯原子的结构示意图: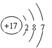 ,C错误;D、
,C错误;D、 属于酚类,和
属于酚类,和 属于醇类,结构不相似,不是互为同系物关系,D错误。选B。
属于醇类,结构不相似,不是互为同系物关系,D错误。选B。
本题难度:一般
4、填空题 (每空1分,共6分)焊接钢铁时常用的焊药为氯化铵,其作用是消除焊接处的铁锈。发生的反应体系中共有六种物质:NH4Cl、FeCl3、N2、Fe2O3、Fe和X。
(1)根据题意,可判断出X是 (写化学式)。
(2)写出并配平该反应的化学方程式: ;
(3)发生氧化反应的物质是 ,反应中4mol的氧化剂能 (填“失去”或“得到”) mol电子;
(4)反应中产生了11.2L(标准状况)的气体时,被还原的物质的质量为 。
参考答案:(每空1分,共6分)(1)H2O (2)6NH4Cl+4Fe2O3=6Fe+2FeCl3+3N2↑+12H2O
(3)NH4Cl;得到;24 (3)80g
本题解析:(1)根据焊药为氯化铵,其作用是消除焊接处的铁锈可知反应物为NH4Cl、Fe2O3,则该反应得生成物为FeCl3、N2、Fe和X,根据元素守恒可知X中含有H、O元素,则X为H2O,故答案为:H2O;
(2)由反应物和生成物可知,NH4Cl+Fe2O3→Fe+FeCl3+N2↑+H2O,该反应Fe元素的化合价由+3价降低为0,N元素的化合价由-3价升高到0,根据电子守恒可知,得电子数=失去电子数=18e-,则6NH4Cl+Fe2O3→6Fe+FeCl3+3N2↑+H2O,再质量守恒定律可知,配平的化学反应为6NH4Cl+4Fe2O3=6Fe+2FeCl3+3N2↑+12H2O,故答案为:6NH4Cl+4Fe2O3=6Fe+2FeCl3+3N2↑+12H2O;
(3)由6NH4Cl+4Fe2O3
本题难度:一般
5、选择题 取一定质量的均匀固体混合物Cu、Cu2O和 CuO,将其分成两等份,取其中一份用足量的氢气还原,测得反应后固体质量减少6.40g,另一份中加入500mL稀硝酸,固体恰好完全溶解,且同时收集到标准状况下NO气体4.48L,则所用硝酸的物质的量浓度为 ( )
A.3.2mol/L
B.2.8mol/L
C.1.8mol/L
D.缺数据无法计算