1��ѡ���� ��һ����̶����ܱ������г���һ������SO2��O2��������Ӧ��2SO2+O2?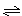 ?2SO3����֪V��SO2��==0.05mol��l-1��min-1����2min��SO3��Ũ��Ϊ��?��
?2SO3����֪V��SO2��==0.05mol��l-1��min-1����2min��SO3��Ũ��Ϊ��?��
A��1mol��l-1
B��0.1mol��l-1
C��0.9mol��l-1
D��0.2mol��l-1
�ο��𰸣�B
�����������Ӧ����ͨ���õ�λʱ����Ũ�ȵı仯������ʾ������2min��SO2��Ũ�ȱ仯����0.05mol��l-1��min-1��2min��0.1mol/L�����ݷ���ʽ��֪�������������Ũ��Ϊ0.1mol/L����ѡB��
�����Ѷȣ���
2��ѡ���� ���淴ӦH2��g��+I2��g���P2HI��g���ﵽ��ʱ�ı�־�ǣ�������
A����������ܶȺ㶨����
B������������ɫ���ٸı�
C��H2��I2��HI��Ũ�����
D���������ѹǿ����
�ο��𰸣�A�����������غ㶨��֪����Ӧǰ�����������ʼ�ղ��䣬���������������䣬������������ܶ�ʼ�ղ��䣬��A����
B���÷�Ӧ�е�����ɫ��������������ɫ������Ӧ�ﵽƽ��״̬ʱ���������ʵ����ʵ�����Ũ�ȵȲ��ٷ����仯�����Ի���������ɫ���ٸı䣬��B��ȷ��
C��ƽ��ʱ�������ʵ�Ũ���뷴Ӧ�ij�ʼŨ�ȡ�ת�����йأ�����H2��I2��HI��Ũ����Ȳ��ǻ�ѧƽ��״̬�ı�־����C����
D���÷�Ӧ�Ƿ�Ӧǰ�������������Ļ�ѧ��Ӧ�����۷�Ӧ�Ƿ�ﵽƽ��״̬�����������ʵ���ʼ�պ㶨���䣬���������ѹǿʼ�ղ��䲻���жϻ�ѧƽ��״̬����D����
��ѡB��
���������
�����Ѷȣ�һ��
3��ѡ���� ��֪��CO2(g) + 3H2(g) 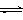 ?CH3OH(g) + H2O(g)? ��H����49.0 kJ?mol��1��һ�������£������Ϊ2 L���ܱ������г���2 mol CO2��6 mol H2�����CO2��CH3OH(g)��Ũ����ʱ��仯������ͼ��ʾ�����������У���ȷ����
?CH3OH(g) + H2O(g)? ��H����49.0 kJ?mol��1��һ�������£������Ϊ2 L���ܱ������г���2 mol CO2��6 mol H2�����CO2��CH3OH(g)��Ũ����ʱ��仯������ͼ��ʾ�����������У���ȷ����

A��10min�������¶���ʹ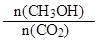 ����
����
B����Ӧ�ﵽƽ��״̬ʱ��CO2��ƽ��ת����Ϊ75%
C��3 minʱ����CO2��Ũ�ȱ�ʾ������Ӧ���ʵ�����CH3OH��Ũ�ȱ�ʾ���淴Ӧ����
D���ӷ�Ӧ��ʼ��ƽ�⣬H2��ƽ����Ӧ���ʦ�(H2)��0.075 mol��L��1?min��1
�ο��𰸣�B
���������A���÷�ӦΪ���ȷ�Ӧ�������¶�ʹƽ�������ƶ�������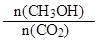 ��С������B��CO2��ת��Ũ��Ϊ1.00mol?L?1-0.25mol?L?1=0.75mol?L?1������ת����Ϊ0.75mol?L?1��1.00mol/L��100%=75%����ȷ��C��3 minʱ����Ӧ��δ�ﵽƽ�⣬������CO2��Ũ�ȱ�ʾ������Ӧ���ʲ�������CH3OH��Ũ�ȱ�ʾ���淴Ӧ���ʣ�����D����(H2)��3��(CO2)=3��0.75mol?L?1��10min=0.225mol��L-1?min-1������
��С������B��CO2��ת��Ũ��Ϊ1.00mol?L?1-0.25mol?L?1=0.75mol?L?1������ת����Ϊ0.75mol?L?1��1.00mol/L��100%=75%����ȷ��C��3 minʱ����Ӧ��δ�ﵽƽ�⣬������CO2��Ũ�ȱ�ʾ������Ӧ���ʲ�������CH3OH��Ũ�ȱ�ʾ���淴Ӧ���ʣ�����D����(H2)��3��(CO2)=3��0.75mol?L?1��10min=0.225mol��L-1?min-1������
�����Ѷȣ�һ��
4������� ��12�֣���ҵ����CO����ȼ�ϼ״���һ�������·�����Ӧ��CO(g)+2H2(g)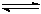
CH3OH(g)��ͼ1��ʾ��Ӧ���й����������ı仯������aδʹ�ô���������bʹ�ô�������ͼ2��ʾһ���¶��£������Ϊ2L���ܱ������м���4mol H2��һ������CO��CO��CH3OH(g)��Ũ����ʱ��仯�����
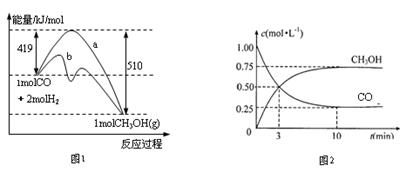
��1������˵����ȷ����______________
A����Ӧ���е�3minʱ�ﵽ��ѧƽ��״̬
B���Ƿ�ʹ�ô����Է�Ӧǰ��������仯û��Ӱ��
C������Ӧ��������һ��ʱ������Ӧ����Һ̬�״��������仯ֵ�����
D��ƽ��ʱ������Ũ��Ϊ1mol/L