1��ѡ���� �߹���Ni/MH(M��ʾ����Ͻ�)����Ѿ����ڻ�϶����������ܷ�Ӧ����ʽ���£�
Ni(OH)2��M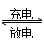 NiOOH��MH������������ȷ����
NiOOH��MH������������ȷ����
A���ŵ�ʱ����������Һ�ļ�����ǿ
B���ŵ�ʱ������ӦΪ��M��H2O��e��===MH��OH��
C���ŵ�ʱ������ӦΪ��NiOOH��H2O��e��===Ni(OH)2��OH��
D���ŵ�ʱÿת��1 mol���ӣ�������1 mol NiOOH������
�ο��𰸣�A
����������ŵ��൱��ԭ��أ�C����ȷ�������ǵõ����ӵģ������ܷ�Ӧʽ��֪��������NiOOH�е�Ni�õ����ӱ���ԭ������Ni(OH)2��������ǿ��A��ȷ��D����ȷ��ԭ����и���ʧȥ���ӣ����ѡ��B����ȷ����ѡA��
�����Ѷȣ�һ��
2������� ��������ȵ�пƬ��ͭƬ�õ�����������500mL?����ͭ��Һ�й�������ͼ��װ�ã���1����װ��Ϊ______����װ���з�����Ӧ�ܵ����ӷ���ʽΪ______��ͭƬ��Χ��Һ�����______������
��2����2min����пƬ��������1.3g�������������ĵ���Ϊ______mo1��
��3����װ�õĵ������Һ��������______?����һ�ּ��ɣ���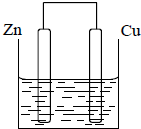
�ο��𰸣���1��װ��û����ӵ�Դ������ԭ��أ����ý���п������������ʧ���ӣ���������ͭ���ӵõ��ӣ�����ͭ�����ڸü������ܶȼ�С��������Ӧ������Ӧ�ϲ���Ϊ�ܵĵ�ط�Ӧ���ʴ�Ϊ��ԭ��أ�Zn+Cu2+�TZn2++Cu����ɫ��dz��
��2����п�������ķ�ӦΪ��Zn-2e-��Zn2+��пƬ��������1.3g��������0.02molʱ��ת�Ƶ���0.04mol���ʴ�Ϊ��0.04��
��3�������ܷ�Ӧ��Zn+Cu2+�TZn2++Cu������ʱ����Ǻ���ͭ���ӵ��Σ��ҵ���еĵ���ʱ�����ǿ����ʣ��ʴ�Ϊ��CuCl2������ͭ���ӵĿ����Ե��μ��ɣ���
���������
�����Ѷȣ�һ��
3��ѡ���� ���������ױȽ����һ��ǿ��������ȷ����
A.��������ԭ��Ӧ�У���ʧ���������Ҷ�
B.ͬ��̬�����ӣ��ױ���������ǿ
C.�����¼�����ŨHNO3��Ӧ���Ҳ���
D.���ס������ԭ���ʱ����Ϊ����
�ο��𰸣�D
���������
�����Ѷȣ�һ��
4��ѡ���� ����ʵ��������Ʒ��;����Ҫ���ʵ�˵��������ȷ���ǣ�������
| ?ѡ�� | ?A | ?B | ?C | ?D
?��Ʒ
?

?

?

?

?��;
?��ѧ��ת��Ϊ����
?����ˮ��
?ȥ������
����ת��Ϊ����?
?��Ҫ����
H2?SO4��aq���ǵ������Һ
?�������������Ҫ�ɷ�
?Ӳ֬��������Ҫ�ɷ�
?SiO2��ת������
|
A��A
B��B
C��C
D��D
�ο��𰸣�A������Ϊ�����Ķ��ε�أ��ŵ�ʱ��ѧ��ת��Ϊ���ܣ�ѡ������Ϊ����ʣ���A��ȷ��
B���轺�������ɶ�Ľṹ��������ˮ�ԣ��������������B��ȷ��
C�������������Ƿ����е�Ӳ֬���������۷������黯���ã���C��ȷ��
D��̫���ܵ�ذ����Ϊ�裬��ʵ�ֹ���ת��Ϊ���ܣ���D����
��ѡD��
���������
�����Ѷȣ�һ��
5��ѡ���� Ϊ̽��ԭ��ص��γ������ͷ�Ӧԭ����ijͬѧ���������ʵ�鲢��¼��������һ��Ũ�ȵ�ϡ�����в���пƬ���������������ɣ���������ϡ�����в���ͭƬ��û�п������������ɣ��۽�пƬ��ͭƬ�϶˽Ӵ�����ס��һ�����ϡ�����У�����ͭƬ�����������ɣ����������ݵ����ʱ�ʵ����п죻����пƬ��ͭƬ�м���ϵ����ƣ��ٽ�пƬ��ͭƬ����ϡ�����У����ֵ�����ָ��ƫת�����й�������ʵ����Ƽ�����ķ���������ȷ���ǣ�������
A��ʵ��١���˵��п����ϡ���ᷴӦ��ͭ����
B��ʵ���˵������ԭ��ط�Ӧʱ��ӿ컯ѧ��Ӧ����
C��ʵ���˵���ڸ�������ͭ������ϡ���ᷴӦ��������
D��ʵ���˵����ԭ�����ͭΪ������пΪ����
�ο��𰸣���пΪ���ý������������ᷢ���û���Ӧ����������
��ͭΪ�������˳�����H�Ժ�Ľ���������ϡ���ᷴӦ��
�۵�п��ͭ���Ӳ���ϡ�����У����γ�ԭ��أ�п�ϻ��ã���ԭ��صĸ������������ϲ������ģ�ͭ�ϲ����ã���ԭ��ص��������缫�������ݲ�������ԭ��ط�Ӧ��һ��Ļ�ѧ��Ӧ���ʽϴ�Ӧ��ʵ������������ͭ���ϵõ��ӱ���ԭ����������
�ܻ����Բ�ͬ��п��ͭ�Լ��������Һ�γɱպϻ�·ʱ���γ�ԭ��أ�����ѧ��ת��Ϊ���ܣ�������ָ��ƫת��
����ȷ��ֻ�Тۣ�
��ѡC��
���������
�����Ѷȣ���