| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高考化学知识点整理《盐类水解的原理》高频考点预测(2019年最新版)(十)
参考答案:B 本题解析:A.明矾溶于水电离出Al3+,Al3+水解生成Al(OH)3胶体,Al(OH)3胶体能吸附水中悬浮物,达到净水的目的,但不能杀菌、消毒,A项错误;B.食醋的主要成分是CH3COOH,能与水垢(主要成分是CaCO3)反应,达到除去水垢的目的,B项错误;C.花香是植物挥发出来的酯的气味,不是醇,C项错误;D.正常雨水的PH因溶解了CO2小于5.6,只有PH<5.6的雨水才是酸雨,D项错误;选B。 本题难度:简单 3、选择题 下列溶液中有关微粒的物质的量浓度关系正确的是( ) 参考答案:D 本题解析:A、混合后的溶液呈中性,则有c(OH-)= c(H+),同时溶液满足电荷守恒,则有c(Cl-)+c(OH-)+c(CH3COO-)= c(H+)+ c(Na+),所以有c(Cl-)+ c(CH3COO-)= c(Na+),根据物料守恒可得c(CH3COOH)+ c(CH3COO-)= c(Na+),所以c(Cl-)= c(CH3COOH),错误;B、等物质的量浓度等体积的硫化钠溶液与硫酸氢钾溶液混合,二者的物质的量相等,所以C(K+)= C(SO42-),则离子浓度的大小关系是C(Na+)> C(K+)= C(SO42-)> C(HS-)> C(OH-)>C(H+),错误;C、二元弱酸的酸式盐NaHA溶液的pH<7,根据电荷守恒和物料守恒得c(H+)+ c(Na+)="2" c(A2-)+c(OH-) +c(HA-),c(Na+)= c(A2-)+c(H2A) +c(HA-),二者结合消去c(Na+),可得c(H+)+ c(H2A)= c(A2-)+c(OH-),错误;D、醋酸是弱酸,溶液越稀越易电离,所以pH=3与pH=2的醋酸溶液中前者溶液的浓度与后者的溶液浓度之比小于1:10,所以中和等物质的量的氢氧化钠时消耗的氢离子的物质的量相等,则消耗醋酸溶液的体积前者体积与后者体积之比大于10:1,Va>10Vb,正确,答案选D。 本题难度:一般 4、填空题 (14分)(Ⅰ)甲醇是重要的化学工业基础原料和清洁液体燃料。工业上可利用CO或CO2来生产燃料甲醇。已知甲醇制备的有关化学反应以及在不同温度下的化学反应平衡常数如下表所示:
(2)在3 L容积可变的密闭容器中发生反应②,已知c(CO)-反应时间t变化曲线Ⅰ如图所示,若在t0时刻分别改变一个条件,曲线Ⅰ变为曲线Ⅱ和曲线Ⅲ。当曲线Ⅰ变为曲线Ⅱ时,改变的条件是 。当曲线Ⅰ变为曲线Ⅲ时,改变的条件是 。 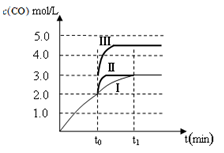 (3)一定条件下甲醇与一氧化碳反应可以合成乙酸。通常状况下,将a mol/L的醋酸与b mol/LBa(OH)2溶液等体积混合,反应平衡时,2c(Ba2+)= c(CH3COO-),用含a和b的代数式表示该混合溶液中醋酸的电离常数为 。 (Ⅱ)已知草酸是一种二元弱酸,草酸氢钠(NaHC2O4)溶液显酸性。 (1)常温下,向10 mL 0.01 mol・L-1 H2C2O4溶液中滴加10mL 0.01mol・L-1 NaOH溶液时,比较溶液中各种离子浓度的大小关系 ; (2)称取6.0g含H2C2O4・2H2O、KHC2O4和K2SO4的试样,加水溶解配成250 mL 溶液。量取两份此溶液各25 mL,分别置于两个锥形瓶中。第一份溶液中加入2滴酚酞试液,滴加0.25mol・L-1 NaOH 溶液至20mL时,溶液由无色变为浅红色。第二份溶液滴加0.10 mol・L-1 酸性KMnO4溶液至16mL时反应完全。则原试样中H2C2O4・2H2O的的质量分数为_______。 参考答案:(Ⅰ)(1)K1・K2(2分); >(2分) 本题解析:(Ⅰ)(1)反应①的平衡常数表达式K1=[CH3OH]/[CO][H2]2,反应②的平衡常数表达式K2="[CO]" [H2O]/[CO2][H2],反应③的平衡常数表达式K3=[CH3OH] [H2O]/[CO2][H2]3,则K3= K1・K2。500℃时反应③的平衡常数K3= K1・K2=2.5,在某时刻,H2(g)、CO2(g)、CH3OH(g)、H2O (g)的浓度(mol/L)分别为0.8、0.1、0.3、0.15, Q=(0.3×0.15)÷(0.8×0.1)=0.5625,Q<K,反应正向进行,则此时V正>V逆。(2)对于反应②:在t0时刻改变一个条件,曲线Ⅰ变为曲线Ⅱ,由图像可知平衡时c(CO)不变,说明平衡没有移动,但缩短了达平衡的时间,改变的条件为加入催化剂;当曲线Ⅰ变为曲线Ⅲ时,CO的平衡浓度由3.0mol/L迅速变为4.5 mol/L,反应在3 L容积可变的密闭容器中发生,且该反应两边气体物质的系数相等,则改变的条件为将容器的体积(快速)压缩至2L。(3)醋酸的电离方程式为CH3COOH 本题难度:困难 5、选择题 常温下,0.2 mol/L CH3COOH溶液与0.1 mol/L NaOH溶液等体积混合后(忽略混合前后溶液体积的变化),溶液的pH<7,则下列有关此溶液的叙述正确的是 | |||||||||||||||||||
参考答案:B
本题解析:混合溶液为0.05mol/L CH3COOH、0.05mol/LCH3COONa,溶液的pH<7,说明
CH3COOH电离程度大于CH3COO-的水解程度,C 错误;
溶液中离子浓度的大小关系为: c(CH3COO-)>c(Na+)>c(H+)>c(OH-) D 错误。
醋酸电离抑制了水的电离,溶液中由水电离产生的H+浓度小于1×10-7 mol/L,A 错误。
c(CH3COO-)+c(CH3COOH)="0.1" mol/L,c(Na+)=0.05 mol/L,c(CH3COO-)+c(CH3COOH)-c(Na+)=0.05 mol/L,B 正确。
本题难度:一般
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | |
| 下一篇:高考化学知识点归纳《影响化学反.. | |