1、选择题 下列各组中的离子能够一定能大量共存的是
[? ]
A.H+、Na+、CO32-、Cl-
B.Cl-、Ba2+、SO42-、K+
C.H+、OH-、SO42-、Cl-
D.H+、Ag+、NO3-、Na+
2、简答题 某混合物的水溶液中,只可能含有以下离子中的若干种:K+、Mg2+、Fe3+、Al3+、NH4+、Cl-、CO32-和SO42-.现每次取100.00mL进行实验:(已知NH4++OH-?NH3↑+H2O)
①第一份加入AgNO3溶液有沉淀产生;
②第二份加入足量NaOH后,整个过程没有沉淀产生,加热,收集到气体0.896L(标准状况下)
②第三份加入足量BaCl2溶液后得干燥沉淀6.27g,沉淀经足量盐酸洗涤,干燥后剩余2.33g.
请回答:
(1)c(CO32-)=?;
(2)K+是否存在??;若存在,浓度至少是?(若不存在,则不必回答第(2)问);
(3)根据以上实验,不能判断哪种离子是否存在??若存在,这种离子如何进行检验??.
3、填空题 化学学科中的化学平衡、电离平衡、水解平衡和溶解平衡均符合勒夏特列原理。请回答下列问题:
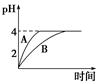
(1)常温下,取pH=2的盐酸和醋酸溶液各100 mL,向其中分别加入适量的Zn粒,反应过程中两溶液的pH变化如图所示。则图中表示醋酸溶液中pH变化曲线的是________(填“A”或“B”)。设盐酸中参加反应的Zn粒质量为m1,醋酸溶液中参加反应的Zn粒质量为m2,则m1________m2(选填“<”、“=”或“>”)。
(2)已知常温下Cu(OH)2的Ksp=2×10-20。又知常温下某CuSO4溶液里c(Cu2+)=0.02 mol・L-1,如果要生成Cu(OH)2沉淀,则应调整溶液pH大于________;要使0.2 mol・L-1的CuSO4溶液中Cu2+沉淀较为完全(使Cu2+浓度降至原来的千分之一),则应向溶液里加NaOH溶液,使溶液pH为________。
(3)10 ℃时加热NaHCO3饱和溶液,测得该溶液的pH发生如下变化:
温度/℃
| 10
| 20
| 30
| 加热煮沸后冷却到50 ℃
|
pH
| 8.3
| 8.4
| 8.5
| 8.8
|
?
在分析该溶液pH增大的原因时,甲同学认为是升高温度HCO3-的水解程度增大所致;乙同学认为是溶液中升高温度NaHCO3受热分解生成Na2CO3,CO32-水解程度大于HCO3-所致。请你设计一个简单的实验方案给甲和乙两位同学的说法以评判(包括操作、现象和结论)________________________________________________________________________。
4、选择题 某同学对一无色透明溶液进行分析,得出该溶液中含有下列某组离子,你认为该组离子应是
A.Al3+、NO3ˉ、K+、SO42ˉ
B.Ca2+、H+、HCO3ˉ、Na+
C.OHˉ、CO32-、Ca2+、SO42 ˉ
ˉ
D.Fe3+、Mg2+、NO3ˉ、Clˉ
5、选择题 氯化钡有剧毒,致死量为0.3g,万一不慎误服,应大量吞服
鸡蛋清及适量解毒剂,此解毒剂是()
A AgNO3 B CuSO4 C MgSO4 D NA2CO3