1、填空题 欲探究氯气与碘单质的氧化性强弱,某同学设计了如下装置(用浓盐酸和KMnO4固体反应制取氯气)。
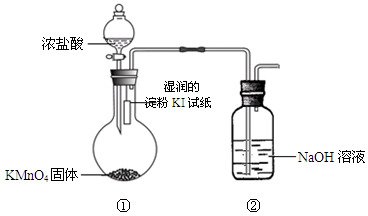
请回答:
(1)实验中观察到湿润的淀粉KI试纸?,写出其中发生的置换反应的离子方程式: ?。
(2)实验结论:氯单质的非金属性比碘单质的?(填“强”或“弱”)。从原子结构角度解释:氯和碘位于周期表中?族,该族元素从上到下,?,得电子能力减弱。
(3)装置②的作用是?。
写出相应的化学方程式:?
参考答案:(12分)(1)试纸 变蓝,Cl2 +2 I-=I2+ 2Cl-
(2) 强, ⅦA族,原子半径逐渐增大
(3)尾气吸收装置,吸收多余的氯气。Cl2+2NaOH=NaCl+NaClO+H2O
本题解析:(1)装置①中可以生成氯气,氯气具有强氧化性,能把碘化钾氧化生成单质碘,碘遇淀粉显蓝色,反应的离子方程式是Cl2 +2 I-=I2+ 2Cl-。
(2)根据强者可以置换弱者可知,氯单质的非金属性比碘单质的强。这是由于氯和碘位于周期表中的第ⅦA族,该族元素从上到下,原子半径逐渐增大,得电子能力减弱。
(3)氯气有毒,所以装置②的作用是尾气吸收装置,吸收多余的氯气,反应的化学方程式是Cl2+2NaOH = NaCl+NaClO+H2O。
点评:该题是基础性实验题的考查,侧重对学生基础知识的巩固和训练,意在培养学生规范的实验设计能力,有利于调动学生的学习兴趣,激发学生的学习积极性。该类试题主要是以常见仪器的选用、实验基本操作为中心,通过是什么、为什么和怎样做重点考查实验基本操作的规范性和准确及灵活运用知识解决实际问题的能力。
本题难度:一般
2、实验题 某化学兴趣小组欲在实验室探究氯气的性质及模拟工业制取漂白粉,设计了如下装置进行实验(实验室制取氯气的反应为MnO2 + 4 HCI(浓) MnCl2?+ C12↑+ 2 H2O):
MnCl2?+ C12↑+ 2 H2O):
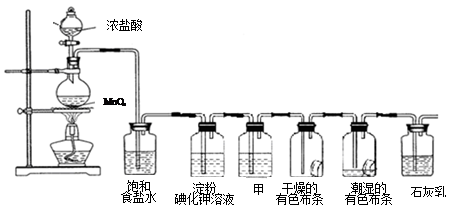
请按要求回答下列问题:
(1)淀粉碘化钾溶液中观察到的现象是_________,反应的离子方程式____________。
(2)若干燥的有色布条不褪色,湿润的有色布条褪色,则甲中盛放________(填名称)。
(3)C12与石灰乳反应制取漂白粉的化学方程式为___________________。
(4)该兴趣小组用8.7g MnO2与足量的浓盐酸制备氯气,则理论上最多可制得标准状况下的Cl2______________L。
参考答案:(1)溶液变蓝色? Cl2+2I-=2Cl-+I2
(2)浓硫酸
(3)2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O
(4)2.24
本题解析:(1)MnO2与浓盐酸混合加热发生反应制取Cl2,由于HCl有挥发性,实验在Cl2中含有杂质HCl,用饱和NaCl溶液来除去HCl杂质有可以减少Cl2的消耗。由于Cl2有氧化性,会与KI发生反应:Cl2+2KI=2KCl+I2。I2遇淀粉变蓝色。反应的离子方程式为Cl2+2I-=2Cl-+I2。(2)若干燥的有色布条不褪色,湿润的有色布条褪色,则甲中盛放浓硫酸。(3)C12与石灰乳反应制取漂白粉的化学方程式为2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O。(4)n(MnO2)=8.7g÷87g/mol="0.1mol." 由于HCl过量。所以放出的气体由MnO2决定。根据方程式MnO2 + 4 HCI(浓) MnCl2?+ C12↑+ 2 H2O可得放出的C12的物质的量为0.1mol.在标准状况下,其体积为2.24L。2的实验室制法及有关的性质、现象及有关气体摩尔体积的计算的知识。
MnCl2?+ C12↑+ 2 H2O可得放出的C12的物质的量为0.1mol.在标准状况下,其体积为2.24L。2的实验室制法及有关的性质、现象及有关气体摩尔体积的计算的知识。
本题难度:一般
3、选择题 原子X转移一个电子给原子Y,形成化合物HY,下列说法正确的是(?)
A.X被氧化了
B.X是氧化剂
C.X发生还原反应
D.Y在反应中表现了氧化性
参考答案:A
本题解析:X失电子,被氧化,发生氧化反应,是还原剂,表现还原性。A正确,B、C错。Y在反应中作氧化剂,表现氧化性,D错。
本题难度:简单
4、选择题 氟、氯、溴、碘的单质中,与氢气混合后在暗处就能发生剧烈反应的是(填写化学式,下同)?;常温下为深红棕色液体的是?;能使淀粉溶液变蓝的是?。
参考答案: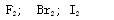
本题解析:略
本题难度:简单
5、选择题 制备纯净、干燥的氯气,并试验它与金属的反应。每个虚线框表示一个单元装置,其中有错误的是( )
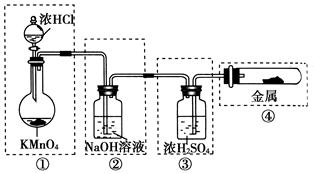
A.①②
B.②
C.②③
D.②③④
参考答案:D
本题解析:KMnO4与浓盐酸常温下即可反应,①是正确的;制得的Cl2中含有HCl气体和水蒸气,显然不能用NaOH溶液来吸收HCl,因为它同时也吸收Cl2,②是错误的;在用浓H2SO4干燥Cl2时,应是“长管进、短管出”,③是错误的;Cl2与金属的反应,若用图示中的装置,应将导管伸入试管底部,金属也应置于试管底部,且试管口不应加橡胶塞,更好的方法是用两端开口的硬质玻璃管,在右端连接盛NaOH溶液的尾气吸收装置,因而④也是错误的。
点拨:本题考查实验室制备氯气,考查考生实验动手的能力。难度中等。
本题难度:一般