1、选择题 T℃时,某一气态平衡体系中含有X(g)、Y(g)、Z(g)、W(g)四种物质,此温度下发生反应的平衡常数表达式为: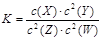 ,有关该平衡体系的说法正确的是
,有关该平衡体系的说法正确的是
A.该反应可表示为X(g) + 2Y(g) 2Z(g) + 2W(g)
2Z(g) + 2W(g)
B.减小X浓度,平衡向逆反应方向移动,平衡常数K减小
C.增大反应容器的压强,该反应速率一定增大
D.升高温度,W(g)体积分数增加,则正反应是放热反应
参考答案:D
本题解析:A.由于化学平衡常数是可逆反应达到平衡状态时各生成物浓度幂指数的乘积与各反应物浓度幂指数乘积的比。所以该反应可表示为2Z(g) + 2W(g)  X(g) + 2Y(g)。错误。B. 减小X浓度,平衡向正反应方向移动,但是由于反应的温度不变,所以化学平衡常数K不变。错误。C.若容器的容积不变,向容器内冲入与体系无关的气体而增大反应容器的压强,由于各物质的浓度没变,所以该反应速率不变;若缩小容器的容积,使物质的浓度增大,则化学反应速率加快。错误。D.根据平衡移动原理:升高温度,化学平衡向吸热反应方向移动。由于W(g)体积分数增加,则升高温度平衡逆向移动逆反应为吸热反应。则正反应是放热反应。正确。
X(g) + 2Y(g)。错误。B. 减小X浓度,平衡向正反应方向移动,但是由于反应的温度不变,所以化学平衡常数K不变。错误。C.若容器的容积不变,向容器内冲入与体系无关的气体而增大反应容器的压强,由于各物质的浓度没变,所以该反应速率不变;若缩小容器的容积,使物质的浓度增大,则化学反应速率加快。错误。D.根据平衡移动原理:升高温度,化学平衡向吸热反应方向移动。由于W(g)体积分数增加,则升高温度平衡逆向移动逆反应为吸热反应。则正反应是放热反应。正确。
本题难度:一般
2、计算题 在某温度下,将H2和I2各0. 10 mol的气态混合物充入10L的密闭容器中,充分反应达到平衡后,测得c(H2)= 0.008 0mol・L-1。
(1)求该反应的平衡常数。
(2)在上述温度下,该容器中若通入H2和I2蒸气各0. 20 mol,试求达到化学平衡状态时各物质的浓度。
参考答案:(1)平衡常数为0.25。
(2)c( H2)=c(I2)=0.016 mol/L,c( HI)=0.008 0mol/L。
本题解析:
本题难度:一般
3、选择题 在一定温度下,CO和水蒸气分别为1 mol、3 mol,在密闭容器中发生反应CO+H2O(g) CO2+H2,达平衡后测得CO2为0.75 mol再通入6 mol水蒸气,达到新的平衡后,CO2和H2的物质的量之和可能为
CO2+H2,达平衡后测得CO2为0.75 mol再通入6 mol水蒸气,达到新的平衡后,CO2和H2的物质的量之和可能为
A.1.2 mol
B.1.5 mol
C.1.8 mol
D.2.5 mol
参考答案:C
本题解析:略
本题难度:简单
4、填空题 在一定温度下,将2mol?A和2mol?B两种气体相混合于体积为2L的某密闭容器中(容积不变),发生如下反应:3A(g)+B(g)
xC(g)+2D(g),△H<0,到2min末反应达到平衡状态(温度不变),生成了0.8mol?D,并测得C的浓度为0.4mol?L-1,请填写下列空白:
(1)x的值等于______.
(2)该反应的化学平衡常数K=______,升高温度时K值将______(选填“增大”、“减小”或“不变”).
(3)A物质的转化率为______.
(4)若维持温度不变,在原平衡混合物的容器中再充入3mol?C和3mol?D,欲使达到新的平衡时,各物质的物质的量分数与原平衡相同,则至少应再充入B的物质的量为______?mol.
参考答案:(1)平衡时C的浓度为0.4mol/L,故生成C的物质的量为0.4mol/L×2L=0.8mol,物质的量之比等于化学计量数之比,故0.8mol:0.8mol=x:2,解得x=2,
故答案为:2;
(2)平衡时C的浓度为0.4mol/L,则:
? 3A(g)+B(g)?2C(g)+2D(g)
开始(mol/L):1? 1? 0? 0
变化(mol/L):0.6? 0.2? 0.4? 0.4
平衡(mol/L):0.4? 0.8? 0.4? 0.4
故带温度下,该反应的平衡常数k=c2(C)?c2(D)c3(A)?c(B)=0.42×0.420.43×0.8=0.5,
平衡常数只受温度影响,该反应正反应是放热反应,升高温度平衡向逆反应移动,平衡常数减小;
故答案为:0.5,减小;
(3)平衡时生成0.8molD,由方程式3A(g)+B(g)?2C(g)+2D(g)可知,参加反应的A的物质的量为0.8mol×32=1.2mol,故A的转化率为1.2mol2mol×100%=60%,
故答案为:60%;
(4)该反应前后气体的物质的量不变,恒温恒容下,按化学计量数转化到左边,满足n(A):n(B)=2mol:2mol=1:1即可,开始加入C和D各3mol,由化学方程式3A(g)+B(g)?2C(g)+2D(g)可知转化到左边,可以得到A为3mol×32=4.5mol,得到B为3mol×12=1.5mol,故还需要加入B,加入B的物质的量为4.5mol-1.5mol=3mol,
故答案为:B,3mol.
本题解析:
本题难度:简单
5、选择题 在2A+B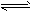 3C+4D中,表示该反应速率最快的是
3C+4D中,表示该反应速率最快的是
[? ]
A.υ(A) = 0.5mol・L-1・S-1
B.υ(B) = 0.3 mol・L-1・S-1
C.υ(C) = 0.8mol・L-1・S-1
D.υ(D)= 1 mol・L-1・S-1
参考答案:B
本题解析:
本题难度:简单