1、选择题 已知常温下:Ksp〔Mg(OH)2〕=1.8×10-11,Ksp(AgCl)=1.8×10-10,Ksp(Ag2CrO4)=1.9×10-12 ,
Ksp(CH3COOAg)=2.3×10-3。下列叙述正确的是
[? ]
A.等体积混合浓度均为0.2 mol・L-1的AgNO3溶液和CH3COONa溶液一定产生CH3COOAg沉淀
B.将0.001 mol・L-1的AgNO3溶液滴入0.001 mol・L-1的KCl和0.001 mol・L-1的K2CrO4溶液中,先产生Ag2CrO4沉淀
C.在Mg2+为0.121 mol・L-1的溶液中要产生Mg(OH)2沉淀,溶液的pH至少要控制在9以上
D.向饱和AgCl水溶液中加入NaCl溶液,Ksp(AgCl)变大
2、填空题 (8分)重晶石(主要成分是BaSO4)是制备钡化合物的重要原料,但BaSO4不溶于水也不溶于酸,这给转化为其他钡盐带来了困难,工业上用饱和Na2CO3溶液处理BaSO4沉淀,待达到平衡后,移走上层清夜,重复多次操作,将其转化为易溶于酸的BaCO3,再由BaCO3制备其它钡盐。
Ksp(BaSO4)=1.0×10-10? Ksp(BaCO3)=5.0×10-10
(1)写出沉淀转化的方程式:?,此反应平衡常数K的值为?。
(2)要实现该转化C(CO32-)不低于??mol/L
(3)必须更换Na2CO3溶液的原因是什么??
3、选择题 已知AgCl(s)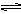 Ag+ + Cl-,平衡时,c(Ag+)・c(C-)="Ksp" ,过量氯化银分别投入①100 mL水?②24 mL 0.1 mol・L-1NaCl?③10 mL 0.1 mol・L-1MgCl2?④30 mL 0.1 mol・L-1AgNO3溶液中,溶液中c(Ag+)大小顺序为
Ag+ + Cl-,平衡时,c(Ag+)・c(C-)="Ksp" ,过量氯化银分别投入①100 mL水?②24 mL 0.1 mol・L-1NaCl?③10 mL 0.1 mol・L-1MgCl2?④30 mL 0.1 mol・L-1AgNO3溶液中,溶液中c(Ag+)大小顺序为
A.③①②④
B.④①②③
C.①②③④
D.④③②①
4、简答题 以黄铁矿为原料制硫酸产生的废渣中含Fe2O3、SiO2、Al2O3、CaO、MgO等.现以此废渣制备铁红(Fe2O3)的过程如下.此浓度时,部分阳离子以氢氧化物形式沉淀时溶液的pH由见表.
| 沉淀物 | 开始沉淀pH | 沉淀完全pH
Al(OH)3
3.0
5.2
Fe(OH)3
1.5
2.8
Fe(OH)2
7.6
9.7
Mg(OH)2
8.0
12.4
|
(1)酸溶过程中Fe2O3与稀硫酸反应的化学方程式是______.
(2)还原过程中加入FeS2是将溶液中的Fe3+还原为Fe2+,而本身被氧化为SO42-,写出有关的离子方程式:______.
(3)氧化过程中通入空气和加入NaOH是为了将溶液中的铁元素充分转化为沉淀而析出,写出有关的离子方程式:______.
(4)为了确保铁红的质量,氧化过程需要调节溶液pH的范围为______≤pH<______.
(5)若NaOH加入过量,所的铁红产品中有其它杂质,但可能无Al2O3,其原因是(用离子方程式表示):______.
5、选择题 已知25℃时,Ka(HF)=3.6×10-4,Ksp(CaF2)=1.46×10-10。现向1 L 0.2 mol・L-1 HF溶液
中加入1 L 0.2 mol・L-1 CaCl2溶液,则下列说法中,正确的是? ( ? )
A.25℃时,0.1 mol・L-1 HF溶液中pH=1
B.Ksp(CaF2)随温度和浓度的变化而变化
C.该体系中没有沉淀产生
D.该体系中HF与CaCl2反应产生沉淀