1���ƶ��� A��J���ճ������г��������ֽ����������ֽ�����NaOH��Һ���ԭ��أ�A��������?F�����������壬�����������µ�ת����ϵ�����ֲ��P������ȥ����?

��ش��������⣺? ?
��1��д��ԭ��صĸ�����Ӧ����ʽ________________
��2������ʱpH��12��C��Һ�У����ʵ������������ʵ�������Ũ��֮��Ϊ_____________��д������ʽ������ͬ�����£���Ũ�ȵ�C��Һ��CH3COONa��Һ�У�C����������CH3COO-Ũ�ȵĴ�С��ϵ��ǰ��___________?���ߣ��á�������������������ʾ���� ?
��3��д���ڵĻ�ѧ����ʽ_____________?
��4����AԪ�ص�ij��X������ˮ����X����ɫ��Ӧʱ������ɫ���ܲ����۲�������ɫ��
��X��ˮ��Һ��NaHCO3��Һ��ϣ���Ӧ�����ӷ���ʽΪ_________
��500mLX����Һ��Ba��OH��2��Ӧ���ɳ��������������Ba��OH��2���ʵ����Ĺ�ϵ��ͼ��?
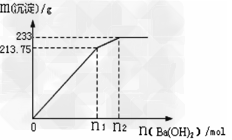
��ش�X���������Ϊ___________������Һ�����ʵ���Ũ��Ϊ__________?mol/L��
2��ѡ���� ���ڳ���ʱΪ���Ӿ��壬��X��Y����Ԫ����ɣ��ڼ���Xm+��Yn�C�ĵ��Ӳ�ṹ��ͬ���ס��ҡ�����������֮�������·�Ӧ��ϵ���� ?��
 �ټ�+H2O? H2��+��+����?
�ټ�+H2O? H2��+��+����?
 ��H2 + ��?�������壩?
��H2 + ��?�������壩?
 ����+��?��+��+H2O
����+��?��+��+H2O
 ����+��?��+�������ԣ�����ס��졢��������
����+��?��+�������ԣ�����ס��졢��������
A��NaCl��NaClO��HClO
B��Na2S��Na2SO3��H2SO3
C��CaCl2��Ca(ClO)2��HClO
D��K2S��K2SO3��H2SO4
3������� ��15�֣���ͼΪ��ѧ��ѧ�м��ֳ�������֮���ת����ϵ����֪����1��A��C��D�dz��������嵥�ʣ���2��F���弫������ˮ����Һ̬���������������3��GΪ�����Ե��Σ�EΪ��ɫ��������4��HΪ��ɫҺ�廯���
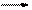
 ��1��д��G�ĵ���ʽ?��
��1��д��G�ĵ���ʽ?��
��2������G�������ӵ�ʵ�鷽��������___________________________?_��
��3����Ӧ�ڵ����ӷ���ʽ?��
��4����Ӧ�۵Ļ�ѧ����ʽ?��
��5���������ʵ�����F��G����ˮ��������ҺpH>7�������Һ�и�������Ũ�ȴ�С˳��Ϊ��?��
4������� A��F����ѧ��ѧ�г������ʣ�������A��C��E��FΪ���壬B��DΪҺ�壬����B�ķ���Ϊ4ԭ�ӷ��ӣ�D�ڳ����²����лӷ��ԣ�F��Ũ��Һ��X����ͨ������ʵ�����Ʊ�����C��X��һ�ֺ�ɫ��ĩ����Щ����֮����������ͼ��ʾ��ת����ϵ��ͼ�в�������������ȥ��

��1��д���������ʵĻ�ѧʽ��A______��F______��
��2��B�ĵ���ʽ��______������ͼ����Ϣ��B��C��X����������ǿ������˳����______���û�ѧʽ��ʾ����
��3����Ӧ�����ӷ���ʽ��______��
��4���ڷ�Ӧ���У�F���ֵ�������______��������0.75molCʱ���������Ļ�ԭ�������ʵ�����______��
5���ƶ��� ����A��G����ͼ��ʾת����ϵ(���ַ�Ӧ�������û���г�)������AΪij���������Ҫ�ɷ֣�����һϵ�з�Ӧ�ɵõ�B��C������C����E��Ũ��Һ������Ӧ��GΪש��ɫ������

��ش��������⣺
(1)д���������ʵĻ�ѧʽ��B________��E________��G?________��
(2)���õ����ᴿC���ʣ��ڸõ�ⷴӦ������������________������������______���������Һ��_____________��
(3)��Ӧ�ڵĻ�ѧ����ʽ��__________________________________��
(4)��0.23?mol?B��0.11?mol���������ݻ�Ϊ1L���ܱ������У�������Ӧ�٣���һ���¶��£���Ӧ�ﵽƽ�⣬�õ�0.12?mol?D����Ӧ��ƽ�ⳣ��K��________�����¶Ȳ��䣬�ټ���?0.50?mol���������´ﵽƽ�⣬��B��ƽ��Ũ��________(����� �����䡱��С��)��������ת����________(����ߡ��������䡱���͡�)��D���������________(����������䡱��С��)��